Clear Sky Science · pt
Perda de DIAPH3 acelera a gênese de gliomas em camundongos
Por que este estudo cerebral é importante
O glioblastoma é um dos cânceres cerebrais mais letais e, apesar de cirurgia, radiação e quimioterapia, a maioria dos pacientes sobrevive pouco mais de um ano. Este estudo coloca uma pergunta básica, porém crucial: quais mudanças iniciais dentro das células cerebrais as empurram para se tornarem tumores tão agressivos, e por que esses tumores são tão difíceis de eliminar com radiação? Ao acompanhar uma única proteína estrutural em células cerebrais de camundongos, os pesquisadores revelam como sua perda desestabiliza os cromossomos, acelera o aparecimento de tumores e ajuda células com características de células-tronco cancerígenas a resistir à radiação que deveria destruí-las.
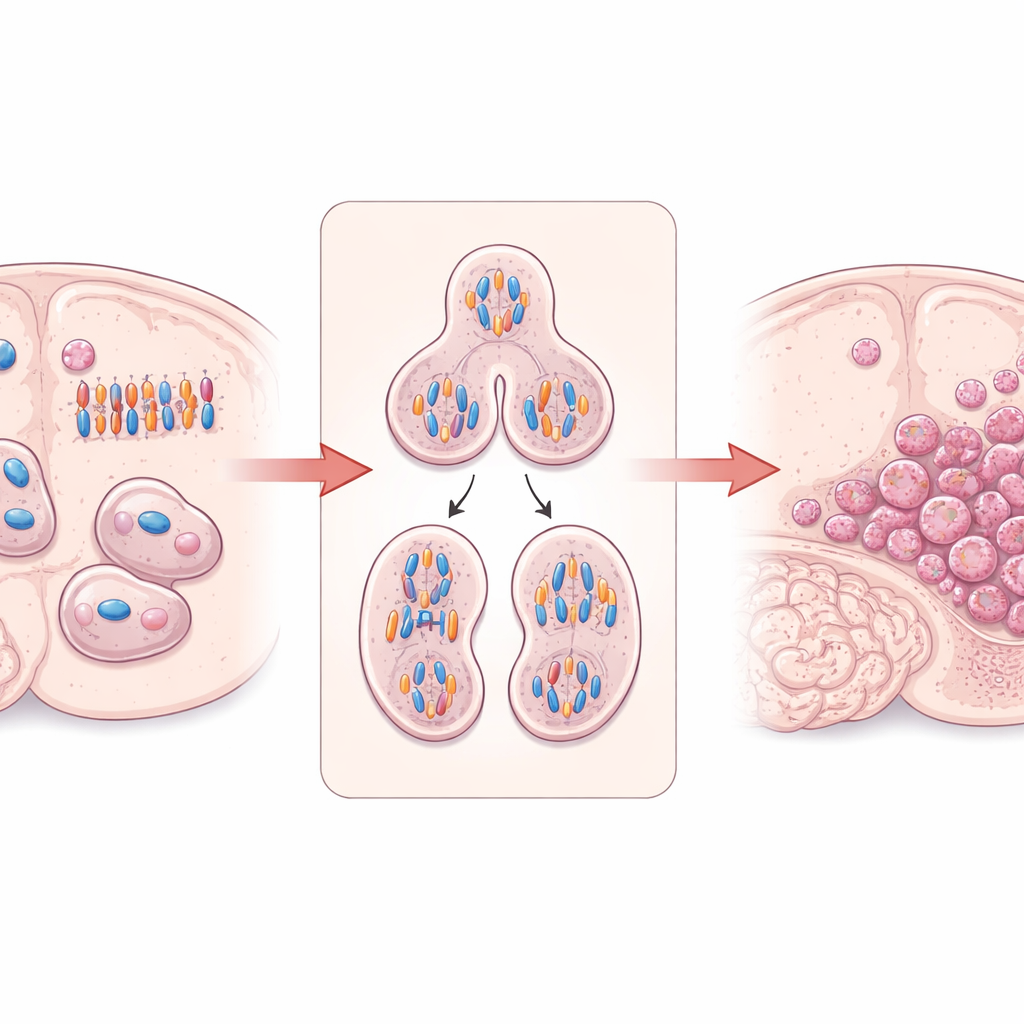
Um “construtor” celular que mantém a divisão sob controle
O trabalho foca na DIAPH3, uma proteína que ajuda a construir e organizar o arcabouço interno da célula feito de filamentos de actina e microtúbulos. Em células-tronco cerebrais em divisão, a DIAPH3 é vital para formar um fuso adequado — a estrutura que separa os cromossomos duplicados — e para dividir uma célula em duas. Pesquisas anteriores mostraram que, quando a DIAPH3 falta em cérebros de camundongos em desenvolvimento, células em divisão frequentemente manuseiam mal os cromossomos, levando a números cromossômicos anormais (aneuploidia), ciclos celulares interrompidos e morte celular. Curiosamente, uma pequena região do cromossomo 13 humano que contém o gene DIAPH3 é frequentemente deletada em glioblastoma, e níveis mais altos de DIAPH3 têm sido associados a melhor sobrevida em alguns pacientes, sugerindo que essa proteína pode agir como supressor tumoral no cérebro.
Engenharia de cérebros de camundongo para crescer tumores
Para testar se a perda de DIAPH3 realmente promove câncer cerebral, a equipe criou camundongos nos quais dois genes podiam ser deletados seletivamente em células-tronco formadoras do córtex: Diaph3 e Trp53, este último codificando o bem conhecido guardião do genoma, p53. Camundongos sem apenas Diaph3 nessa região não desenvolveram tumores mesmo após dois anos, o que implica que p53 ainda pode eliminar células fortemente anormais. Em contraste, camundongos sem Trp53 isoladamente, ou ambos Trp53 e Diaph3, eventualmente formaram gliomas difusos de alto grau que se assemelhavam muito à doença humana ao microscópio. Usando ressonâncias magnéticas repetidas de ultra‑alto campo, os pesquisadores mostraram que animais faltando ambos os genes desenvolveram tumores detectáveis mais cedo e, na meia‑idade, apresentavam com mais frequência grandes gliomas, particularmente nos bulbos olfatórios, do que camundongos sem apenas Trp53. A taxa de crescimento tumoral, uma vez iniciada, foi semelhante entre os grupos — o que mudou foi quão cedo os tumores apareceram.
Caos cromossômico e atividade gênica reprogramada
Para entender por que a perda de DIAPH3 acelera o início do tumor, a equipe examinou a atividade gênica nos bulbos olfatórios de camundongos jovens antes de quaisquer tumores serem visíveis. Em animais sem Diaph3 e Trp53, 126 genes foram expressos em níveis diferentes em comparação com mutantes apenas para Trp53, e quase metade desses já tinha ligação com câncer. Muitas mudanças se concentraram em vias que impulsionam crescimento celular, migração e formação de vasos sanguíneos, incluindo sinalizações VEGF, MAPK, RAS, Rap1 e cAMP, além de redes acopladas a receptores de proteína G. Esse panorama molecular alterado sugeriu que as células estavam sendo empurradas para um estado semelhante ao cancerígeno mais cedo. A análise de número de cópias do genoma completo de tumores totalmente formados revelou que a deficiência de DIAPH3 não aumentou muito mudanças pequenas e focais no DNA, mas sim elevou ganhos e perdas em larga escala de cromossomos inteiros — exatamente a aneuploidia esperada de uma segregação cromossômica defeituosa.
Dano de DNA incorporado e células‑tronco tumorais mais resistentes
Células tumorais aneuploides apresentaram mais danos internos ao DNA, detectados por níveis elevados do marcador de quebras de DNA γ‑H2AX espalhados pelos núcleos celulares. Ainda assim, esses tumores cresceram, o que implica que adquiriram maneiras de tolerar esse estresse. Comparando a expressão gênica em tumores estabelecidos, os pesquisadores encontraram centenas de genes alterados pela perda de DIAPH3, incluindo notável amplificação e superprodução do receptor de fator de crescimento FGFR2 em muitos tumores duplamente mutantes. Sabe‑se que FGFR2 impulsiona a maquinaria de reparo do DNA em células de glioblastoma, e sua ativação tem sido ligada à resistência à radiação. A equipe isolou células de tipo tronco de glioma a partir de tumores de camundongo e testou sua resposta a uma dose clinicamente relevante de radiação ionizante. Antes do tratamento, a frequência de células com fenótipo de tronco era similar em ambos os genótipos, mas após a irradiação, culturas de tumores deficientes em DIAPH3 retiveram aproximadamente o dobro de células-tronco ativas em comparação com aquelas de tumores somente com Trp53, demonstrando maior radioresistência.
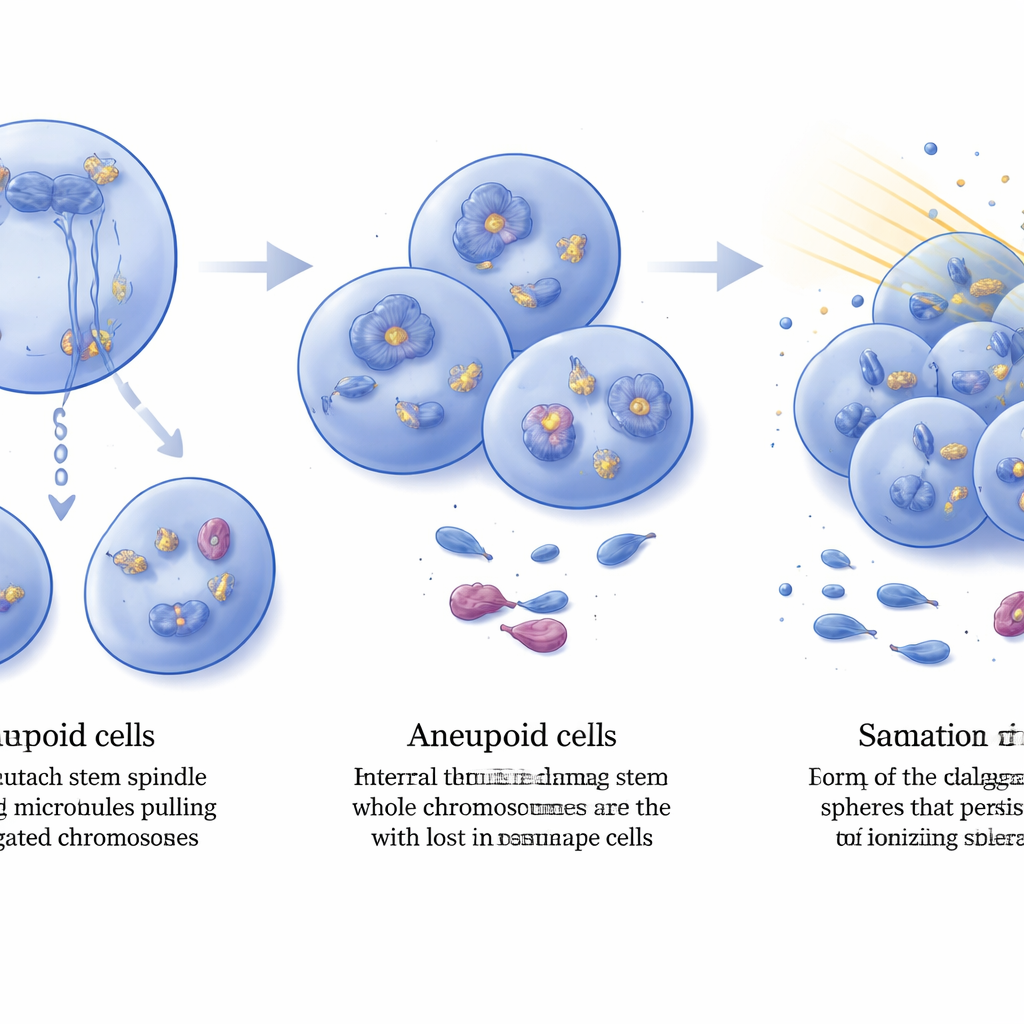
O que isso significa para o câncer cerebral
Em conjunto, o estudo pinta a DIAPH3 como um guardião que ajuda células-tronco cerebrais a se dividirem com o número correto de cromossomos. Quando tanto DIAPH3 quanto p53 estão ausentes, a divisão celular torna‑se propensa a erros, cromossomos inteiros são perdidos ou ganhos, e o dano ao DNA se acumula. Em vez de morrer, algumas células se adaptam amplificando fatores ligados ao reparo, como FGFR2, transformando‑se em gliomas aneuploides de alto grau cujas células com características de tronco são incomumente resistentes à radiação. Embora modelos murinos não capturem todas as características do glioblastoma humano, esses achados apoiam a DIAPH3 tanto como um potencial biomarcador prognóstico quanto como um ponto na rede de processos que controlam a iniciação tumoral, a estabilidade genômica e a resposta ao tratamento — abrindo novas vias para terapias que, um dia, possam tornar esse devastador câncer cerebral mais vulnerável aos tratamentos existentes.
Citação: Chehade, G., Durá, I., Ruiz-Reig, N. et al. Loss of DIAPH3 accelerates glioma genesis in mice. Cell Death Dis 17, 342 (2026). https://doi.org/10.1038/s41419-026-08652-x
Palavras-chave: glioblastoma, instabilidade cromossômica, células-tronco de tumor cerebral, resistência à radiação, genes supressores de tumor