Clear Sky Science · pt
Orquestração metabólica mediada por GGCT: desviando glutamina para biossíntese de glutationa enquanto aumenta a anaplerose da glicose para a proliferação tumoral
Por que isso importa para o tratamento do câncer
As células cancerosas proliferam rapidamente e, para isso, consomem enormes quantidades de combustível e precisam continuamente se proteger dos subprodutos tóxicos do próprio metabolismo. Este estudo revela como uma enzima pouco conhecida, GGCT, ajuda tumores de fígado e próstata a redirecionar de forma inteligente dois nutrientes comuns — glutamina e glicose — para simultaneamente alimentar o crescimento e controlar moléculas danosas chamadas espécies reativas de oxigênio. Compreender esse malabarismo metabólico pode abrir novas maneiras de privar tumores de combustível ou sobrecarregar suas defesas.
Como as células tumorais equilibram combustível e proteção
As células tumorais dependem fortemente da glutamina, um aminoácido com papel duplo: pode ser degradado para abastecer o ciclo central de produção de energia da célula e também fornece blocos de construção para a glutationa, um potente antioxidante que neutraliza espécies reativas de oxigênio. Os autores primeiro confirmaram que os níveis de glutamina são maiores em tumores hepáticos do que no tecido saudável adjacente, e que células cancerosas cultivadas com mais glutamina dividem-se mais rapidamente, tanto em cultura quanto em camundongos. Quando a glutamina é escassa, as células desaceleram, proteínas-chave do ciclo celular diminuem, e tumores em animais encolhem — em parte porque as defesas antioxidantes enfraquecem e as espécies reativas de oxigênio se acumulam.
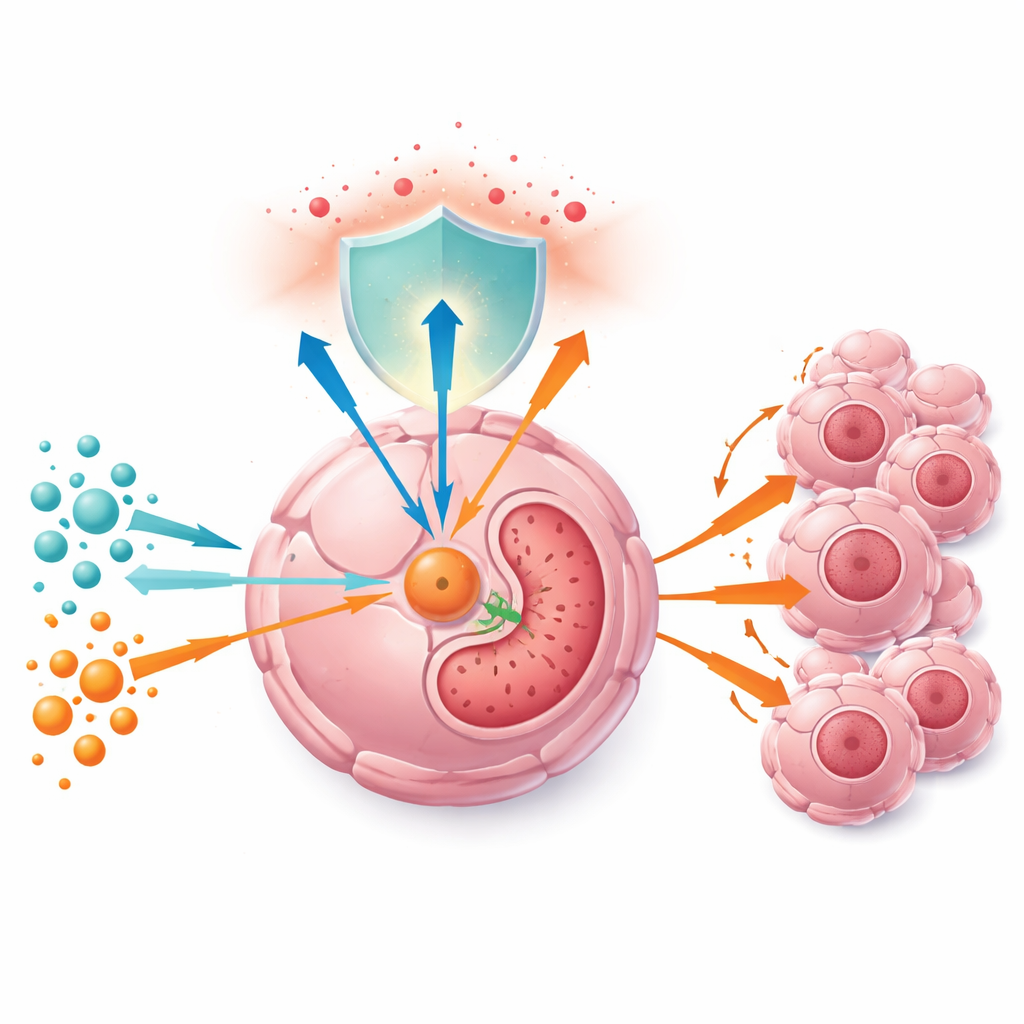
Um interruptor metabólico à vista de todos
Analisando amostras de pacientes e grandes bases de dados de câncer, a equipe descobriu que a enzima GGCT está consistentemente mais abundante em tumores de fígado e próstata do que em tecidos normais, e níveis mais altos de GGCT preveem piores desfechos. Tanto em amostras tumorais quanto em células cultivadas, os níveis de GGCT aumentam em consonância com a concentração de glutamina, sugerindo que os tumores “leem” a disponibilidade de glutamina por meio dessa proteína. Os pesquisadores delinearam uma cadeia de controle: a glutamina mantém o fator pró-crescimento c‑Myc ativo, o qual suprime um pequeno RNA regulador chamado miR‑29b‑3p; quando o miR‑29b‑3p está baixo, o GGCT é liberado de sua restrição e se acumula. Na falta de glutamina, essa cadeia se inverte, o miR‑29b‑3p aumenta, as mensagens de GGCT são degradadas mais rapidamente e o nível da enzima cai.
Redirecionando a glutamina e recrutando mais glicose
Para entender o que o GGCT faz dentro da célula, os autores reduziram ou aumentaram seus níveis e mediram tanto o comportamento celular quanto centenas de metabólitos. Silenciar o GGCT bloqueou as células no ciclo de divisão, encolheu suas colônias e reduziu drasticamente a glutationa enquanto aumentava as espécies reativas de oxigênio; adicionar um antioxidante químico resgatou parcialmente o crescimento. Ao microscópio, as mitocôndrias tornaram-se anormalmente alongadas e menos eficientes no consumo de oxigênio, mesmo quando as células tentavam compensar intensificando a glicólise, a primeira etapa da degradação da glicose. Perfis metabólicos detalhados mostraram que intermediários do ciclo energético central diminuíram quando o GGCT foi perdido e aumentaram quando foi superexpresso.
Rastreando o caminho dos átomos de carbono
A equipe então seguiu átomos marcados de glutamina e glicose enquanto fluíam pelo metabolismo tumoral. Quando o GGCT foi superexpresso, menos glutamina marcada acabou no ciclo de energia e mais foi direcionada para a glutationa recém-sintetizada, apoiando as defesas antioxidantes. Ao mesmo tempo, a glicose marcada contribuiu com mais força para o ciclo, compensando a glutamina desviada. Uma forma mutante de GGCT sem atividade enzimática normal não conseguiu promover essas mudanças nem estimular a proliferação, mostrando que a função catalítica do GGCT é crucial. Importante, fornecer piruvato extra ou ajustar a entrada no ciclo energético restaurou os níveis de energia celular, mas não reduziu as espécies reativas de oxigênio, indicando que o GGCT controla principalmente o equilíbrio redox por meio da glutationa, não por simples alterações no suprimento de energia.
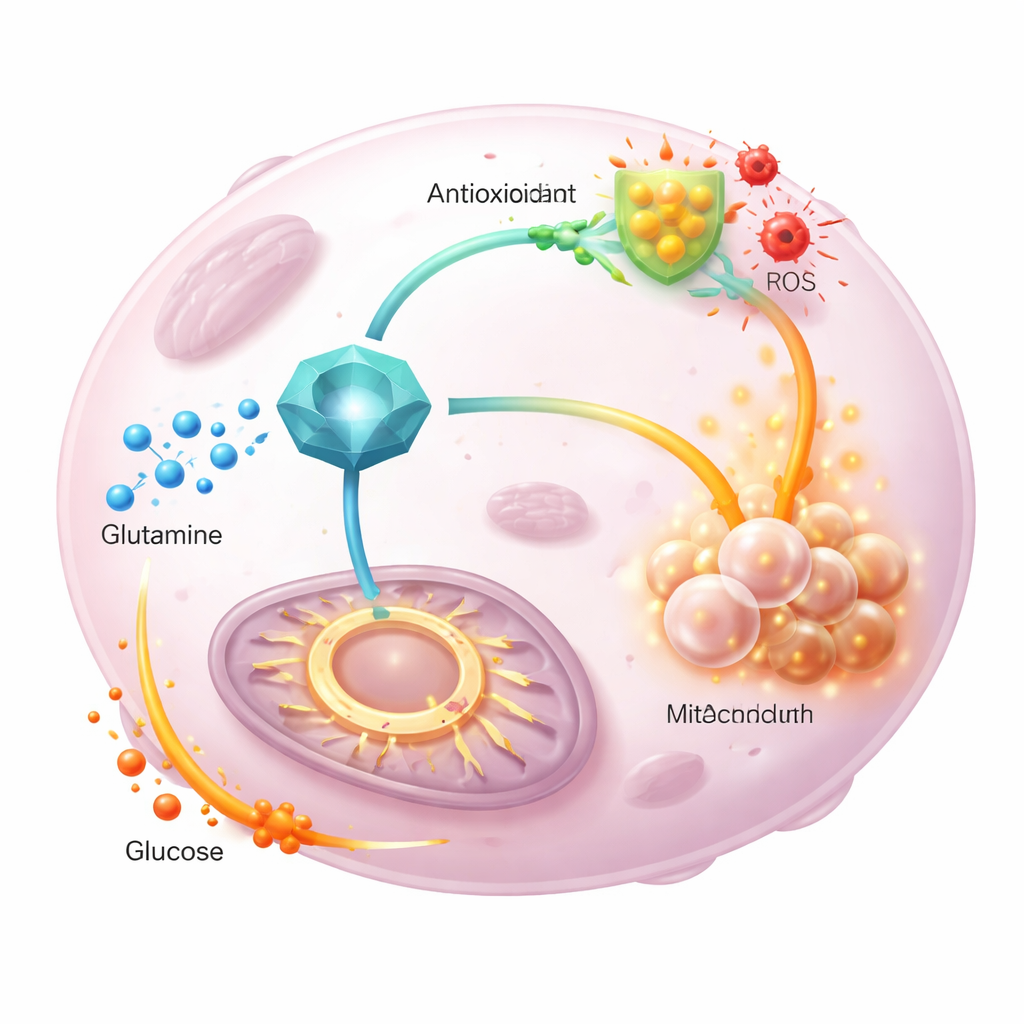
O que isso significa para terapias futuras
Em conjunto, os achados posicionam o GGCT como um coordenador central que permite aos tumores dividir as funções da glutamina: direciona mais desse nutriente à produção de antioxidantes enquanto encaminha a glicose para o ciclo energético para manter a divisão celular em andamento. Em modelos animais, reduzir o GGCT retardou o crescimento tumoral, diminuiu a glutationa e aumentou o estresse oxidativo, e esses efeitos puderam ser parcialmente revertidos com um fármaco antioxidante. Para um observador leigo, a mensagem é que alguns cânceres sobrevivem usando o GGCT como um painel de controle metabólico; drogas que desativem esse interruptor podem enfraquecer simultaneamente as defesas do tumor contra danos oxidativos e perturbar sua utilização flexível de nutrientes, tornando os tratamentos padrão mais eficazes.
Citação: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Palavras-chave: metabolismo do câncer, glutamina, glutationa, estresse oxidativo, enzima GGCT