Clear Sky Science · pt
Transdiferenciação adipogênica reprograma células PDAC com alto EMT para um estado pós-mitótico semelhante a adipócitos e limita metástases
Transformando células cancerígenas agressivas em gordura inofensiva
O câncer de pâncreas é um dos mais letais, em grande parte porque se espalha precocemente e resiste aos tratamentos padrão. Este estudo investiga uma ideia notavelmente diferente: em vez de tentar envenenar ou privar as células tumorais, e se pudéssemos induzir as células de câncer pancreático mais perigosas a se transformarem em células semelhantes a gordura que não se dividem nem migram pelo corpo? O trabalho descreve como pesquisadores direcionaram células de câncer pancreático altamente agressivas para um estado estável, semelhante a adipócitos, que retardou o crescimento tumoral e reduziu a disseminação em camundongos, sugerindo uma nova forma de controlar essa doença devastadora.
Por que o câncer de pâncreas é tão difícil de deter
O adenocarcinoma ductal pancreático, a principal forma de câncer de pâncreas, tem um prognóstico muito ruim: apenas cerca de um em cada oito pacientes está vivo cinco anos após o diagnóstico. Parte do problema é que muitas células tumorais nesse câncer vivem em um estado mutável chamado EMT, que as torna mais móveis, invasivas e resistentes a medicamentos. Tentativas de bloquear os muitos sinais que conduzem esse estado trouxeram benefícios limitados. Ao mesmo tempo, o pâncreas e seus tumores exibem uma tendência surpreendente a acumular células de gordura, suscitando a pergunta de se essa flexibilidade oculta na identidade celular poderia ser aproveitada. Os autores raciocinaram que, se as células de câncer pancreático ricas em EMT já estão preparadas para mudar, talvez pudessem ser redirecionadas para uma identidade silenciosa, semelhante à de adipócitos, em vez de uma invasiva.
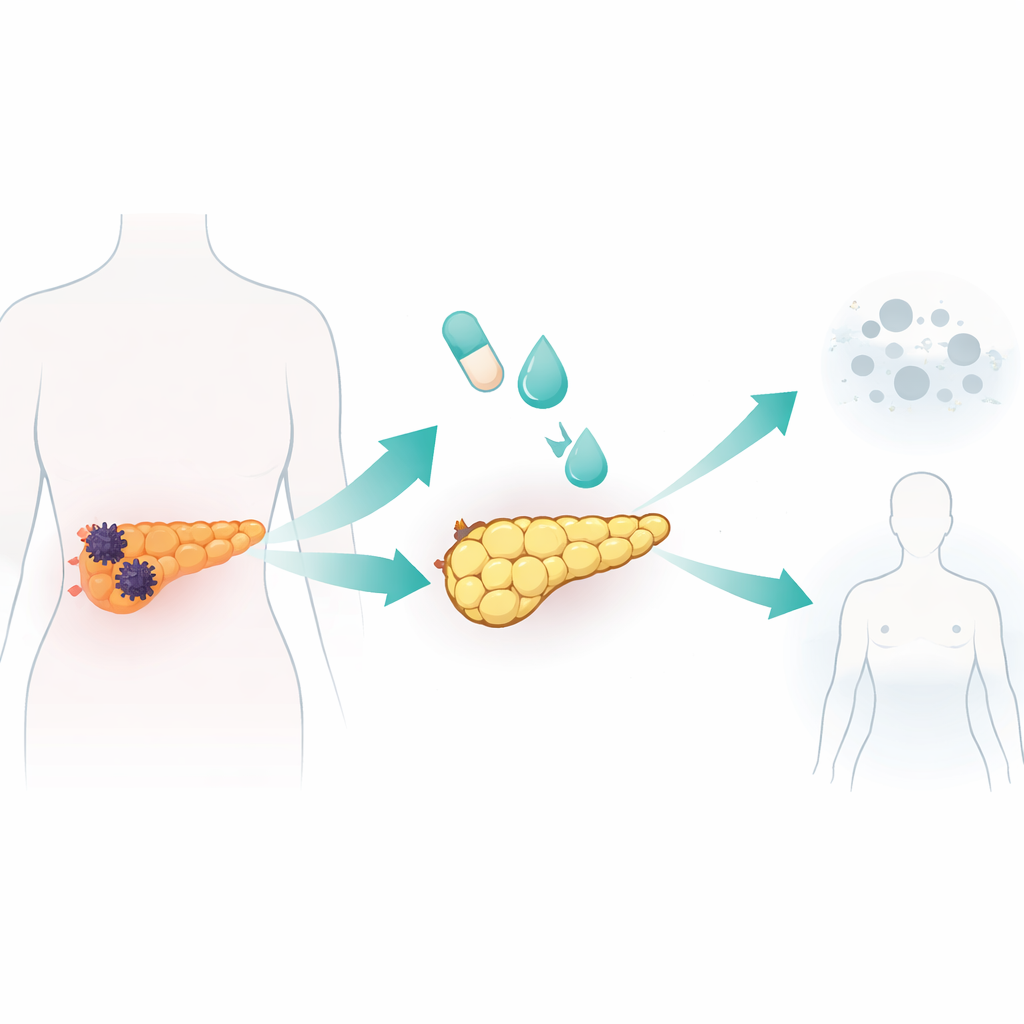
Reprogramando células cancerígenas em células semelhantes a gordura no laboratório
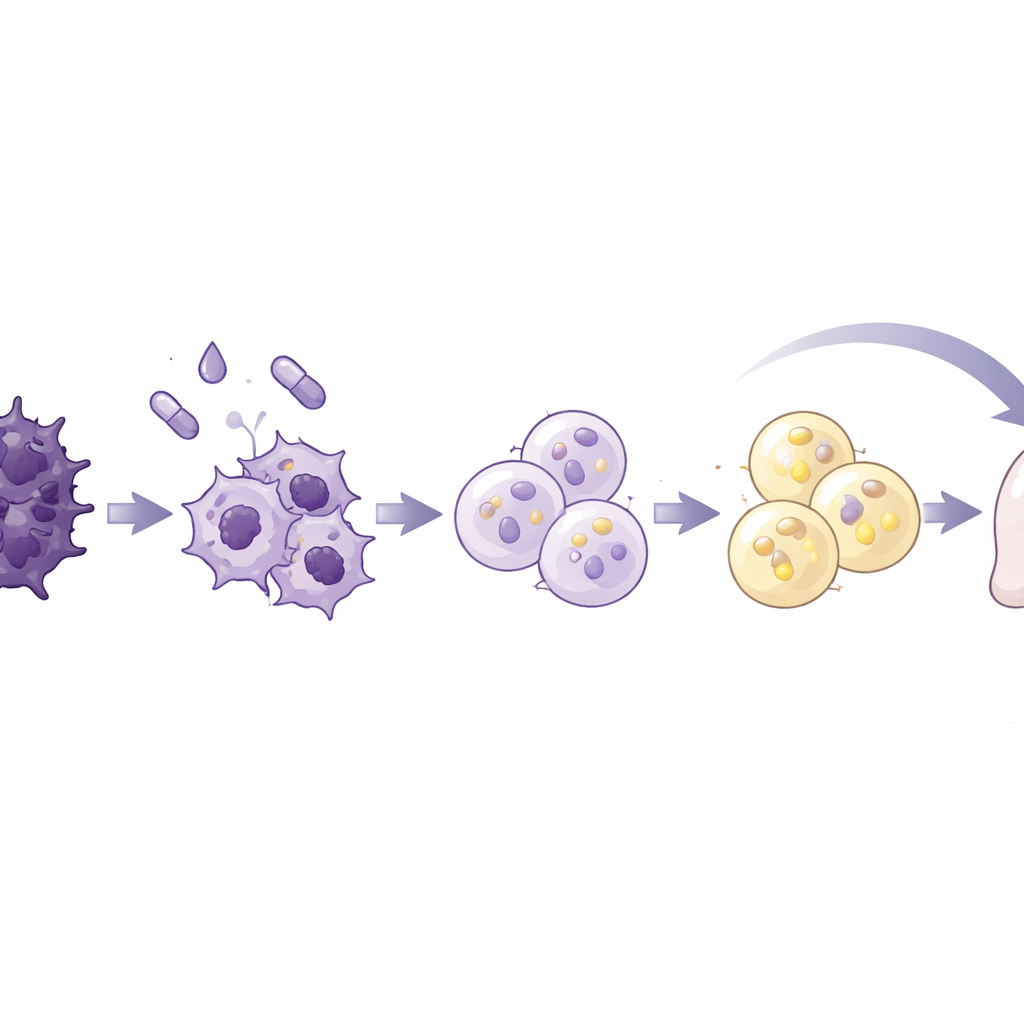
A equipe testou um coquetel padrão para formação de adipócitos, usado em estudos anteriores de biologia da gordura e câncer de mama, em sete linhagens humanas de câncer de pâncreas e em uma linhagem de células pancreáticas normais. A mistura combinava insulina e um esteroide com rosiglitazona, um fármaco que ativa um regulador mestre da adipogênese, além de uma proteína de sinalização chamada BMP2 para destravar a plasticidade celular. Uma linhagem cancerígena, chamada AsPC-1, foi especialmente responsiva. Ao longo de dez dias, essas células tornaram-se maiores e mais arredondadas e se encheram de gotículas lipídicas, marcas de adipócitos. Elas ativaram genes e proteínas típicos de adipócitos maduros e mostraram metabolismo lipídico robusto, incluindo secreção de adiponectina e quebra de gordura armazenada quando estimuladas. Crucialmente, essas células convertidas cessaram de proliferar, ficaram presas na fase inicial do ciclo celular e migraram e invadiram muito menos do que as células cancerígenas não tratadas.
Desligando o programa cancerígeno profundamente na célula
Para ver o que ocorria em nível molecular, os pesquisadores perfilaram o empacotamento do DNA e a atividade gênica das células convertidas. Eles encontraram um estreitamento amplo da cromatina, o complexo DNA–proteína que controla o acesso aos genes, juntamente com uma queda global na expressão gênica, ambas características de células não divisoras. Genes que sustentam EMT, invasão e metástase, incluindo enzimas que degradam a matriz e reguladores-chave de EMT, foram fortemente reprimidos, enquanto genes relacionados à gordura foram aumentados. A assinatura gênica geral mudou de uma identidade mesenquimal, altamente móvel, para uma que se assemelhava de perto a adipócitos maduros. Sinais ligados ao crescimento celular e à resposta a um importante indutor de EMT, TGF-beta, foram atenuados, enquanto vias relacionadas ao manejo de lipídios e adesão celular foram reforçadas. Essas mudanças sugerem que as células não foram apenas desaceleradas, mas fundamentalmente reespecificadas.
Avaliando a estratégia em camundongos
Os cientistas perguntaram em seguida se essa conversão forçada em células semelhantes a gordura poderia ajudar a controlar tumores em animais vivos. Eles implantaram células humanas de câncer de pâncreas no pâncreas ou no baço de camundongos para modelar tumores primários e metástases hepáticas. Camundongos tratados com rosiglitazona e BMP2 desenvolveram tumores pancreáticos menores e exibiram gotículas lipídicas mais abundantes e marcadores de adipócitos dentro dos tumores, junto com níveis mais baixos de genes de EMT e invasão. No modelo de metástase, o tratamento não alterou o assentamento inicial de tumores, mas ao longo do tempo desacelerou a expansão da carga tumoral no fígado em comparação com animais não tratados. Importante, o tecido pancreático normal adjacente não mostrou conversão óbvia em células adiposas, e o estado semelhante a gordura nos tumores persistiu por pelo menos um mês após a suspensão dos fármacos, sugerindo um grau de durabilidade e especificidade.
O que isso pode significar para os cuidados futuros com câncer
Este estudo apoia um conceito provocador: para cânceres pancreáticos altamente plásticos e ricos em EMT, pode ser possível “converter em vez de matar”, redirecionando células tumorais perigosas e errantes para adipócitos estáveis e não divisores que têm menor capacidade de se espalhar. Embora seja trabalho em estágio inicial em células e modelos de camundongo, e nem todos os cânceres de pâncreas respondam igualmente, isso abre uma nova via terapêutica que age mudando a identidade celular em vez de apenas bloquear sinais de crescimento. No futuro, tais abordagens de transdiferenciação poderiam ser combinadas com drogas direcionadas ou imunoterapias para manter o câncer de pâncreas em um estado mais tranquilo e controlável e reduzir o risco de metástase letal.
Citação: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Palavras-chave: câncer de pâncreas, plasticidade celular, transdiferenciação, transição epitélio-mesênquima, células semelhantes a adipócitos