Clear Sky Science · pt
Inibição da quinase relacionada à vaccinia 2 revela vulnerabilidade no metabolismo do glutationa no câncer de pâncreas
Por que isso importa para o câncer de pâncreas
O câncer de pâncreas está entre os mais letais, em parte porque os tratamentos padrão frequentemente falham. Este estudo revela uma fraqueza oculta em certos tumores pancreáticos: a dependência de um “escudo” celular contra subprodutos tóxicos do oxigênio. Ao entender quando esse escudo é frágil e como um gene do câncer chamado VRK2 o fortalece, os pesquisadores indicam novas maneiras de envenenar seletivamente as células cancerosas preservando o tecido saudável.
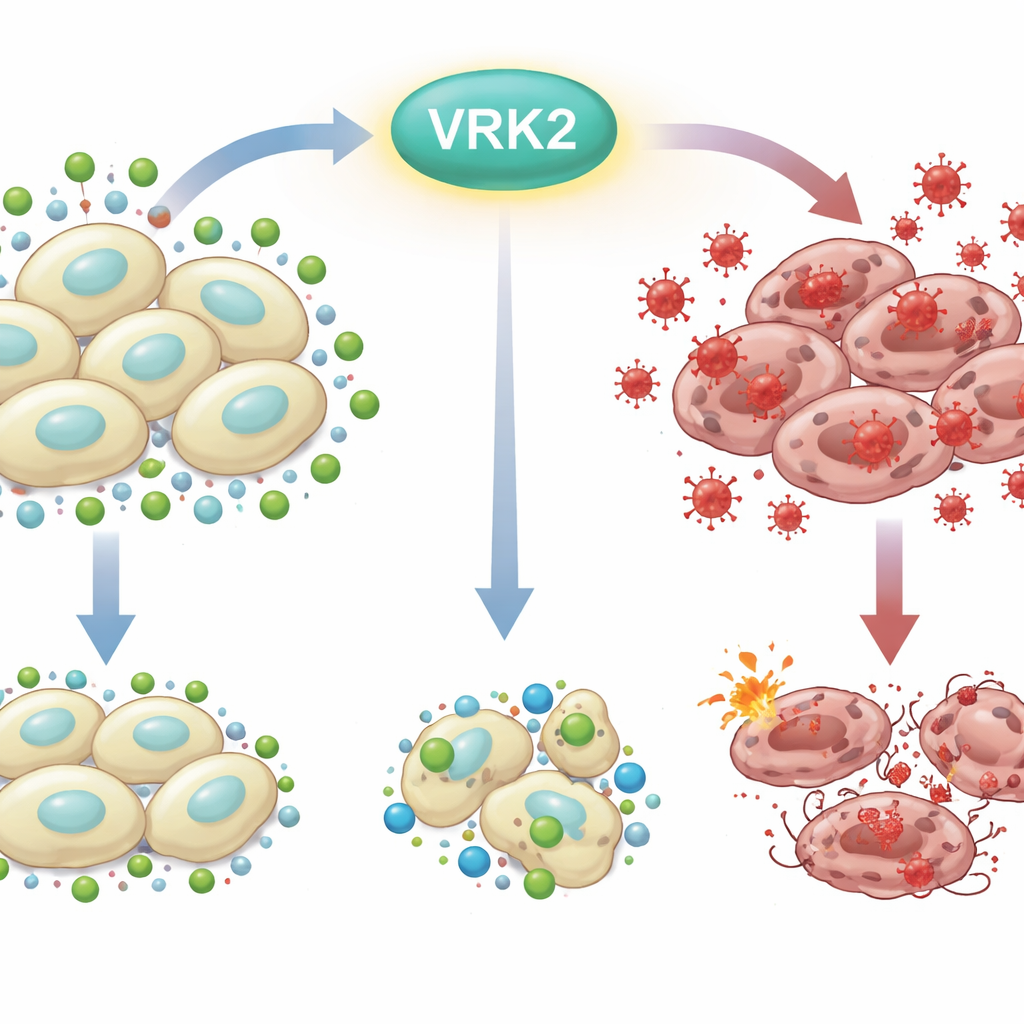
O problema da “ferrugem” celular
Cada célula combate constantemente a “ferrugem interna” causada por espécies reativas de oxigênio — formas altamente reativas de oxigênio que podem danificar DNA, lipídios e proteínas. Para sobreviver, as células usam defesas químicas, com o glutationa atuando como um dos escudos mais importantes. Células de câncer de pâncreas, que vivem em condições adversas e crescem rapidamente, dependem fortemente de artifícios metabólicos para manter quantidade suficiente de glutationa. Desestabilizar esse equilíbrio entre oxidantes danosos e antioxidantes protetores pode levar as células cancerosas ao limite e induzir sua morte.
Encontrando um ponto fraco oculto
Os pesquisadores começaram inativando VRK2, um gene que promove o câncer e que já havia sido associado a prognósticos piores no câncer de pâncreas, e então testaram 281 compostos que atuam no metabolismo. Descobriram que células sem VRK2 eram extraordinariamente sensíveis a fármacos que bloqueiam a produção de glutationa. Nessas células deficientes em VRK2, os níveis de glutationa caíram enquanto as espécies reativas de oxigênio aumentaram, levando à morte celular. Suprir antioxidantes extras ou moléculas semelhantes à glutationa resgatou essas células, confirmando que a vulnerabilidade chave residia precisamente na incapacidade de desintoxicar o estresse oxidativo.
Como VRK2 ajuda as células cancerosas a se armarem
Em seguida, a equipe investigou por que VRK2 altera o metabolismo do glutationa. Eles focaram em uma proteína transportadora chamada SLC7A11, que fica na membrana externa da célula e traz cistina, um bloco de construção necessário para sintetizar glutationa. Surpreendentemente, VRK2 não mudou quanto SLC7A11 a célula produzia no total; em vez disso, controlou se esse transportador alcançava com sucesso a superfície celular. Em células com VRK2 ativado, SLC7A11 trafega do retículo endoplasmático para o complexo de Golgi e depois para a membrana. VRK2 potencializa esse tráfego ao modificar quimicamente uma proteína de seleção de carga chamada Sec24C, que ajuda a carregar SLC7A11 em vesículas de transporte. Quando VRK2 está ausente ou bloqueado, SLC7A11 fica retido dentro da célula, menos transportadores chegam à superfície e o escudo de glutationa enfraquece.
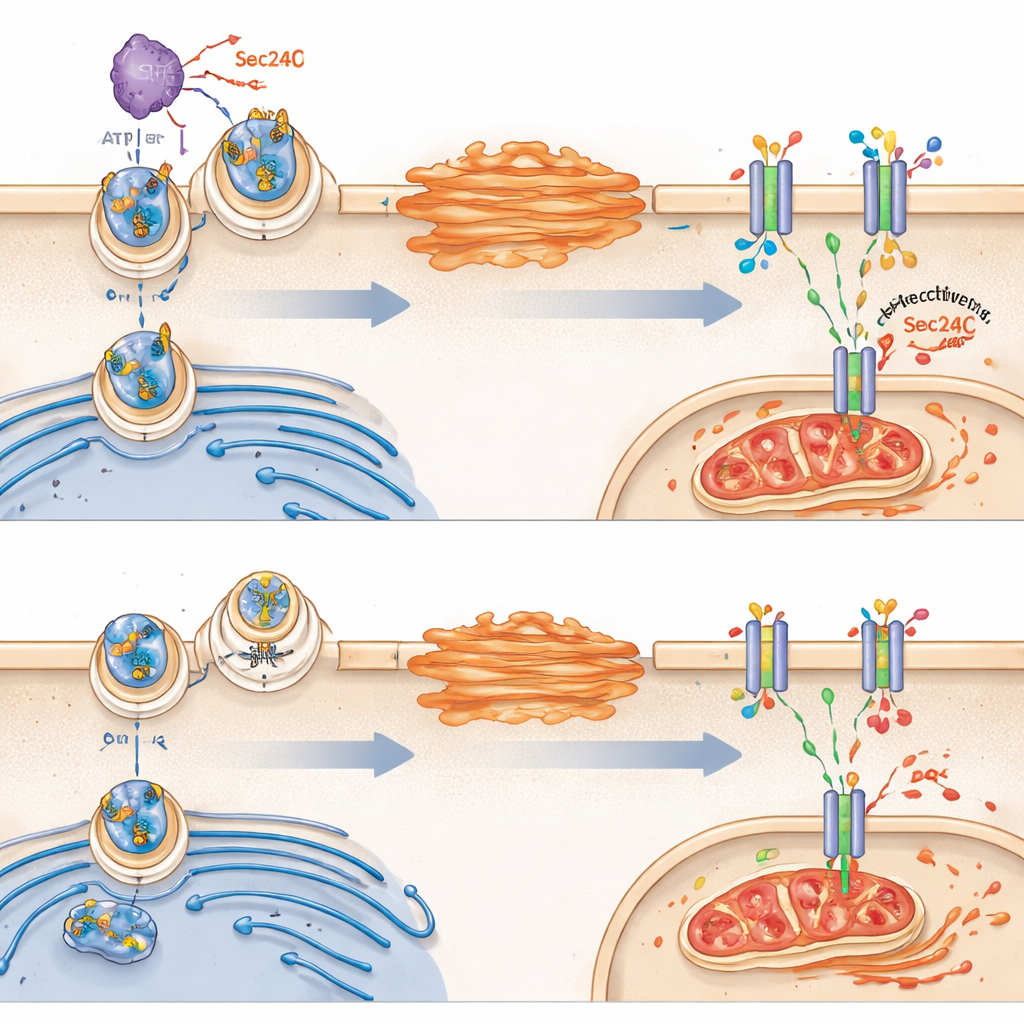
Do escudo rompido à ferroptose
Sem SLC7A11 suficiente na membrana, células deficientes em VRK2 têm dificuldade em importar cistina e manter o glutationa. Isso as deixa especialmente vulneráveis a uma forma de morte celular dependente de ferro chamada ferroptose, caracterizada por oxidação descontrolada dos lipídios da membrana celular e dano mitocondrial. O estudo mostrou que fármacos que cortam a síntese de glutationa desencadearam sinais de ferroptose em células sem VRK2, incluindo mitocôndrias distorcidas e acúmulo de produtos de oxidação lipídica. Bloquear a ferroptose, mas não outros tipos de morte celular, protegeu essas células, ressaltando que o calcanhar de Aquiles delas é a incapacidade de conter o dano oxidativo.
Guiando escolhas de tratamento personalizadas
Por fim, os pesquisadores avançaram para modelos animais e células recém-derivadas de pacientes. Tumores com baixos níveis de VRK2 encolheram quando tratados com um fármaco que mira o glutationa, enquanto tumores com alta expressão de VRK2 foram em grande parte resistentes. No entanto, quando tumores com VRK2 alto também receberam um composto que bloqueia VRK2, eles voltaram a ficar sensíveis à inibição do glutationa. Isso sugere que os níveis de VRK2 podem classificar pacientes em grupos: aqueles cujos tumores são naturalmente vulneráveis à terapia direcionada ao glutationa e aqueles que poderiam se beneficiar de uma estratégia em duas frentes que primeiro desabilite VRK2 e depois ataque o metabolismo do glutationa.
O que isso significa para os pacientes
Em termos simples, este trabalho mostra que alguns cânceres de pâncreas sobrevivem usando VRK2 para manter seu escudo antioxidante forte. Retire o VRK2, e esse escudo enfraquece; retire o glutationa além disso, e as células cancerosas colapsam sob o estresse oxidativo. Medir VRK2 nos tumores pode, portanto, ajudar os médicos a decidir quem tem maior probabilidade de se beneficiar de fármacos que perturbam o metabolismo do glutationa e quem pode precisar primeiro de uma etapa de terapia direcionada a VRK2. Embora sejam necessários mais testes em humanos, o estudo delineia um caminho claro rumo a terapias mais personalizadas, baseadas no metabolismo, para um câncer que necessita urgentemente de melhores opções.
Citação: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Palavras-chave: câncer de pâncreas, metabolismo do glutationa, VRK2, ferroptose, SLC7A11