Clear Sky Science · pt
Repressão do EGFR pelo novo biguanida 4C potencializou o câncer de ovário aos inibidores de PARP por meio da redução de BRCA2 e Rad51
Por que esta pesquisa importa
Para muitas pessoas diagnosticadas com câncer de ovário, os medicamentos direcionados atuais funcionam apenas para uma pequena minoria cujos tumores apresentam defeitos genéticos específicos. Este estudo investiga uma forma de ampliar os benefícios de uma classe importante de fármacos, os inibidores de PARP, para o grupo muito maior de pacientes cujos tumores não têm essas mutações. Ao combinar um novo composto experimental com medicamentos já existentes, os pesquisadores demonstram uma estratégia para empurrar células cancerosas a um beco sem saída letal ao mesmo tempo em que preservam o tecido saudável.
Um obstáculo no tratamento atual do câncer de ovário
O câncer de ovário é frequentemente descoberto tardiamente e continua sendo um dos cânceres mais letais que afetam mulheres. Inibidores de PARP, como o olaparibe, podem ser notavelmente eficazes, mas principalmente em pacientes cujos tumores já apresentam defeitos numa via de reparo de DNA associada aos genes BRCA1 e BRCA2. A maioria dos tumores, porém, ainda tem a maquinaria de reparo intacta e consegue consertar os danos ao DNA causados por esses medicamentos, permitindo que as células cancerosas sobrevivam. Uma parte central dessa equipe de reparo envolve duas proteínas, BRCA2 e Rad51, que ajudam a consertar as fitas de DNA rompidas por meio de um processo chamado recombinação homóloga. Encontrar maneiras de enfraquecer seletivamente essa via de reparo nas células tumorais poderia tornar os inibidores de PARP úteis para muito mais pacientes.
O papel de um conhecido interruptor de crescimento
A equipe concentrou-se em uma molécula ligada ao câncer bem conhecida, o receptor do fator de crescimento epidérmico (EGFR), que fica na superfície de muitas células tumorais e impulsiona seu crescimento. Eles descobriram que o EGFR faz mais do que enviar sinais de crescimento: em células de câncer de ovário com BRCA normais, altos níveis de EGFR foram associados a pior sobrevida dos pacientes e resistência aos inibidores de PARP. Quando o EGFR foi reduzido ou desligado em culturas celulares e em camundongos, os tumores se tornaram muito mais vulneráveis ao olaparibe. Os pesquisadores mostraram que o EGFR ajuda a transportar BRCA2 e Rad51 para o núcleo celular após danos ao DNA, onde elas podem reparar quebras e mitigar o impacto do tratamento. Bloquear simplesmente a atividade enzimática do EGFR não foi suficiente; a quantidade total de proteína EGFR teve de ser reduzida para atrapalhar significativamente essa via de reparo.
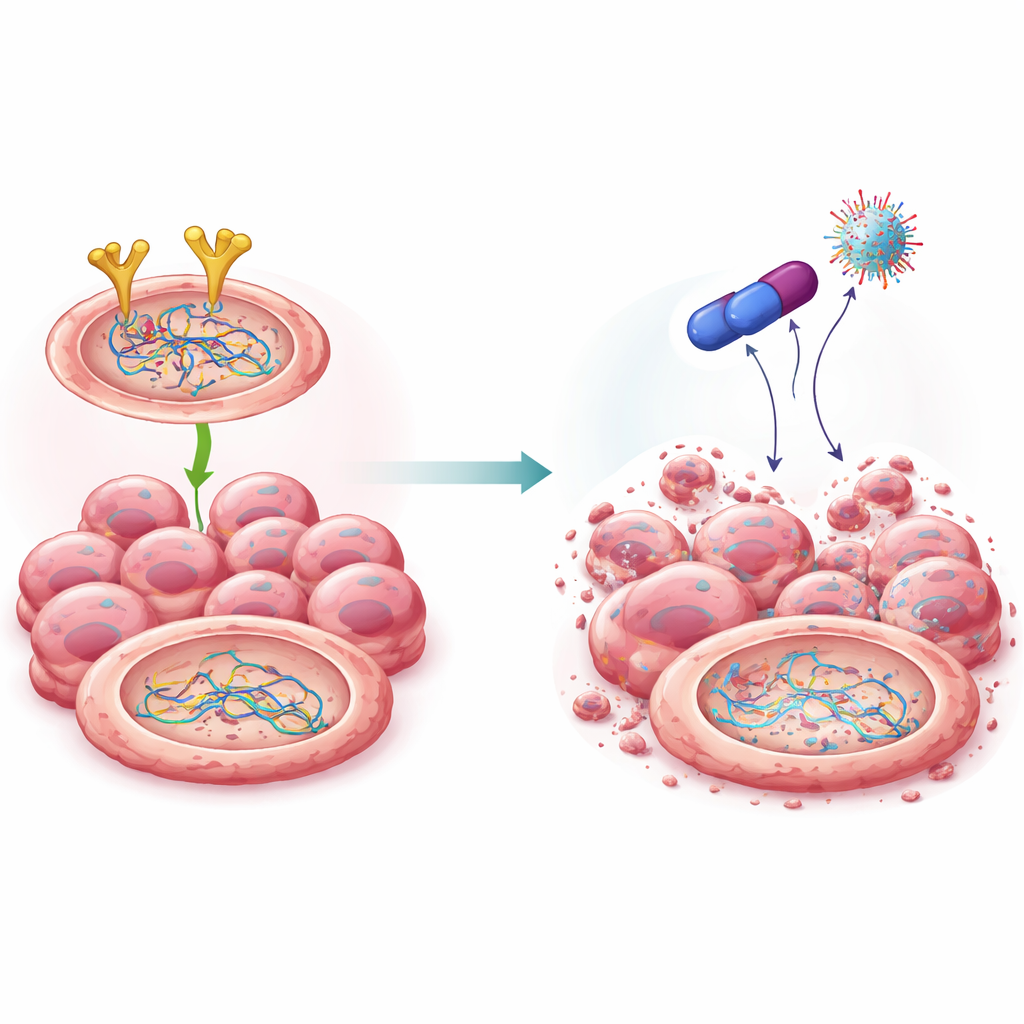
Um novo composto que desarma a equipe de reparo
Com base em trabalhos anteriores com uma família de drogas conhecidas como biguanidas, os cientistas sintetizaram vários congêneres químicos e identificaram uma molécula de destaque, chamada 4C. Este composto foi fortemente tóxico para células de câncer de ovário e relativamente suave para células normais. Modelagem computacional e testes de laboratório indicaram que o 4C se liga diretamente ao EGFR e o marca para destruição na maquinaria de degradação de proteínas da célula. Diferentemente de alguns medicamentos de EGFR existentes, o 4C reduziu a quantidade global de EGFR em vez de apenas silenciar sua atividade. À medida que os níveis de EGFR caíram, a estabilidade de BRCA2 e Rad51 também diminuiu: elas foram marcadas para descarte, degradadas e deixaram de suportar um reparo eficiente do DNA. Importante, essa poda ocorreu ao nível proteico sem alterar os genes subjacentes.
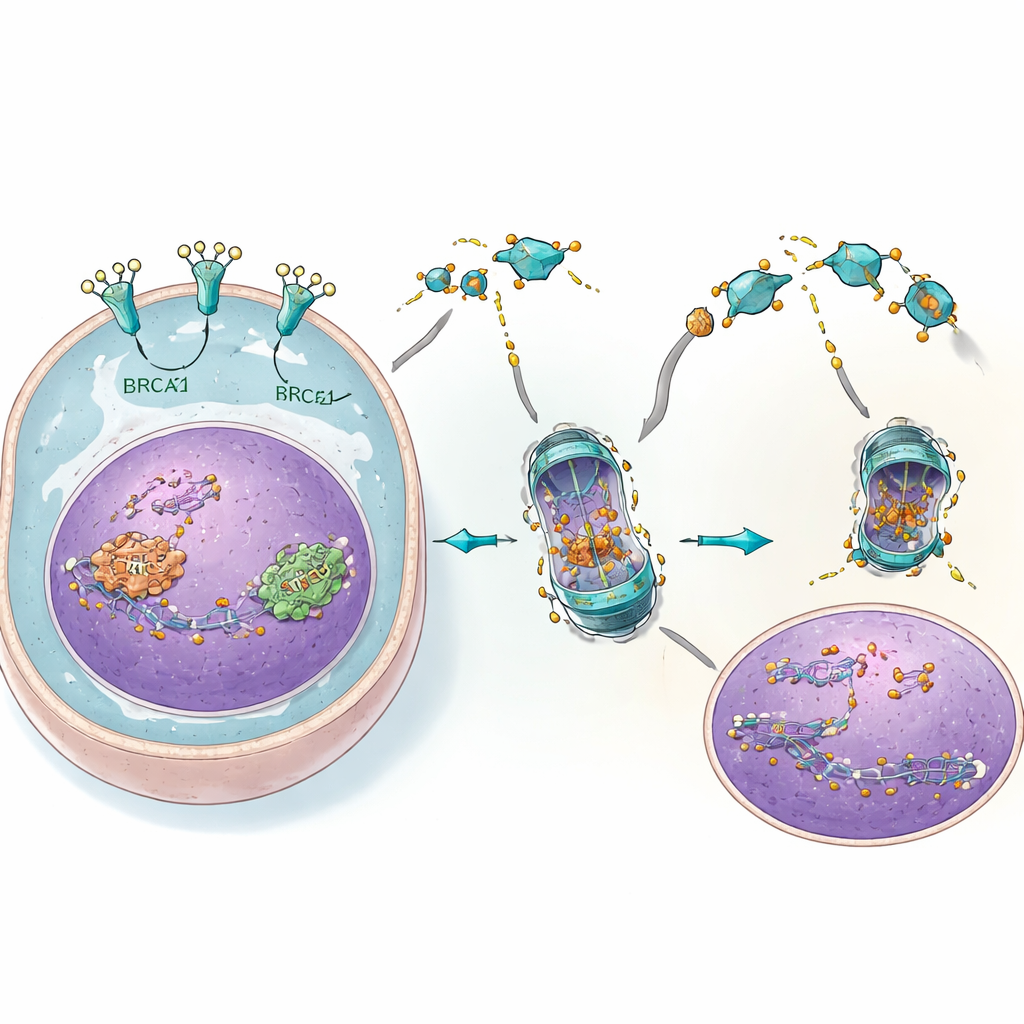
Bloqueando uma rota de resgate dentro da célula
O estudo revelou uma cadeia de eventos mais detalhada que conecta o dano ao DNA à sobrevivência tumoral. Após os inibidores de PARP lesionarem o DNA, outra proteína sensor chamada ATM envia uma mensagem do núcleo para o corpo celular. Em resposta, o EGFR se associa a BRCA2 e Rad51 e ajuda sua translocação para o núcleo, onde reparos ocorrem. Os pesquisadores descobriram que uma terceira proteína, c-Cbl, normalmente atua como um tipo de marcador de descarte para BRCA2 e Rad51. O EGFR compete com c-Cbl pelo acesso a essas proteínas de reparo, protegendo-as de serem marcadas para destruição. Quando o 4C reduz os níveis de EGFR, o c-Cbl pode se ligar mais facilmente a BRCA2 e Rad51, levando à marcação, degradação e perda dessas proteínas. Com menos proteínas de reparo no núcleo, lesões de DNA se acumulam e as células cancerosas ficam muito mais sensíveis aos inibidores de PARP.
Das células aos animais: uma combinação potente
Tanto em células cultivadas quanto em modelos murinos, a combinação de 4C com inibidores de PARP produziu um duplo golpe poderoso. Tumores com genes BRCA normais que resistiam a cada fármaco isoladamente encolheram dramaticamente ou cessaram de crescer quando expostos a ambos em conjunto. Marcadores de dano ao DNA aumentaram de forma acentuada, consistente com a ideia de que o reparo estava sendo sobrecarregado. Ao mesmo tempo, células normais e órgãos-chave, como fígado e rins, mostraram pouca evidência de dano, provavelmente porque têm níveis muito mais baixos de EGFR e dependem menos desse atalho de reparo específico. Os benefícios da combinação também se estenderam à redução da disseminação de células de câncer de ovário pelo corpo.
O que isso pode significar para pacientes
Este trabalho propõe uma maneira de transformar a força de uma célula cancerosa em fraqueza. Ao direcionar o EGFR com o novo composto 4C, os pesquisadores removem a proteção que BRCA2 e Rad51 oferecem, fazendo com que tumores com reparo de DNA aparentemente normal se comportem mais como cânceres com mutação em BRCA em sua resposta aos inibidores de PARP. Essa vulnerabilidade forçada, conhecida como "letalidade sintética", poderia expandir o alcance de medicamentos existentes a muitas mais mulheres com câncer de ovário, mantendo os efeitos colaterais manejáveis. Embora o 4C ainda seja experimental e exija testes extensivos em modelos mais avançados e em ensaios clínicos, o estudo oferece um roteiro claro de como desmantelar ajudantes específicos do reparo em células tumorais pode melhorar os desfechos do tratamento.
Citação: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Palavras-chave: câncer de ovário, inibidores de PARP, EGFR, reparo de DNA, terapia direcionada