Clear Sky Science · pt
Perda de PRKACB facilita metástase do câncer gástrico de tipo difuso por meio da ativação da sinalização RhoA
Por que este estudo importa para o câncer de estômago
O câncer gástrico de tipo difuso é uma forma particularmente agressiva de câncer de estômago que frequentemente se espalha amplamente dentro do abdome, tornando o tratamento difícil e as taxas de mortalidade altas. Este estudo investiga por que esses tumores têm tanta propensão a se disseminar, revelando um sistema molecular de freio que normalmente restringe as células cancerosas de se dispersarem — e mostrando o que ocorre quando esse freio falha. Compreender esse interruptor de controle oculto pode abrir novos caminhos para prever quais pacientes têm maior risco e para desenvolver fármacos que retardem ou impeçam a disseminação perigosa.
Uma forma perigosa de câncer de estômago
Nem todos os cânceres de estômago se comportam da mesma forma. Tumores do tipo intestinal tendem a formar massas mais estruturadas, enquanto o câncer gástrico de tipo difuso (CGD) é composto por células dispersas que se desprendem com facilidade do tumor primário. Pacientes com CGD têm risco de morte maior do que aqueles com doença do tipo intestinal, em parte porque seus tumores semeiam com mais facilidade novos focos por toda a cavidade abdominal. Estudos genéticos anteriores já associaram o CGD a alterações recorrentes no gene RHOA, que influencia como as células se movem e mudam de forma. Mas não estava claro como essas alterações se conectavam às redes de sinalização mais amplas que controlam se as células cancerosas permanecem no lugar ou migram.
Encontrando um freio ausente em amostras tumorais
Os pesquisadores concentraram-se em uma proteína chamada PRKACB, uma subunidade catalítica da conhecida enzima protein quinase A, que ajusta muitos comportamentos celulares adicionando grupos fosfato a outras proteínas. Uma pesquisa proteômica anterior havia sugerido que os níveis de PRKACB estavam anormalmente baixos em CGD agressivos. Para testar isso, a equipe examinou amostras de tumor de 376 pacientes, comparando cânceres de tipo difuso e tipo intestinal e seus tecidos não cancerosos próximos. Eles descobriram que os níveis de PRKACB estavam marcadamente reduzidos em tumores de tipo difuso, especialmente em estágios avançados, mas não em cânceres do tipo intestinal. Pacientes cujos tumores apresentavam pouco PRKACB tiveram sobrevida global significativamente pior, mesmo após ajustar por outros fatores clínicos, sugerindo que PRKACB funciona como um supressor tumoral nesse contexto.
Como níveis baixos de PRKACB impulsionam a fuga celular
Para entender o papel de PRKACB dentro das células cancerosas, a equipe usou linhas celulares em cultura que modelam o câncer gástrico de tipo difuso. Quando reduziram artificialmente o PRKACB, as células tornaram-se mais móveis e invasivas em testes de laboratório, passando com mais facilidade por barreiras e formando projeções em forma de dedo chamadas pseudópodes, que ajudam as células a rastejar. Essas células também mudaram de um estado epitelial mais ordenado para um estado mais frouxo, semelhante ao mesenquimal, associado à metástase, perdendo a molécula de adesão E‑cadherina que normalmente ajuda as células a se manterem juntas. Por outro lado, aumentar os níveis de PRKACB tornou as células menos migratórias e menos invasivas. Importante, essas mudanças não alteraram a velocidade de multiplicação celular, apontando para um papel específico do PRKACB na promoção da disseminação, não do crescimento.
Focalizando o interruptor de sinalização RhoA
Os pesquisadores então perguntaram como o PRKACB exerce esse efeito antimetastático. Usando métodos de interação proteína–proteína e modelagem estrutural, mostraram que o PRKACB se liga diretamente à RhoA, um interruptor molecular que alterna entre formas inativas e ativas para governar a forma e o movimento celular. O PRKACB adiciona um grupo fosfato em uma posição específica da RhoA (serina 188), o que inibe a RhoA e reduz as vias downstream ROCK e FAK que promovem o rearranjo do citoesqueleto e a motilidade celular. Quando o PRKACB foi reduzido, a RhoA ficou menos fosforilada, mais ativa, e a sinalização ROCK/FAK intensificou-se, levando a um movimento celular mais agressivo. Em modelos de camundongos nos quais tumores semelhantes aos humanos foram implantados na parede do estômago, a diminuição de PRKACB causou nódulos metastáticos abdominais mais numerosos e maiores e início mais precoce da disseminação visível, novamente sem alterar a rapidez com que as metástases estabelecidas cresciam.
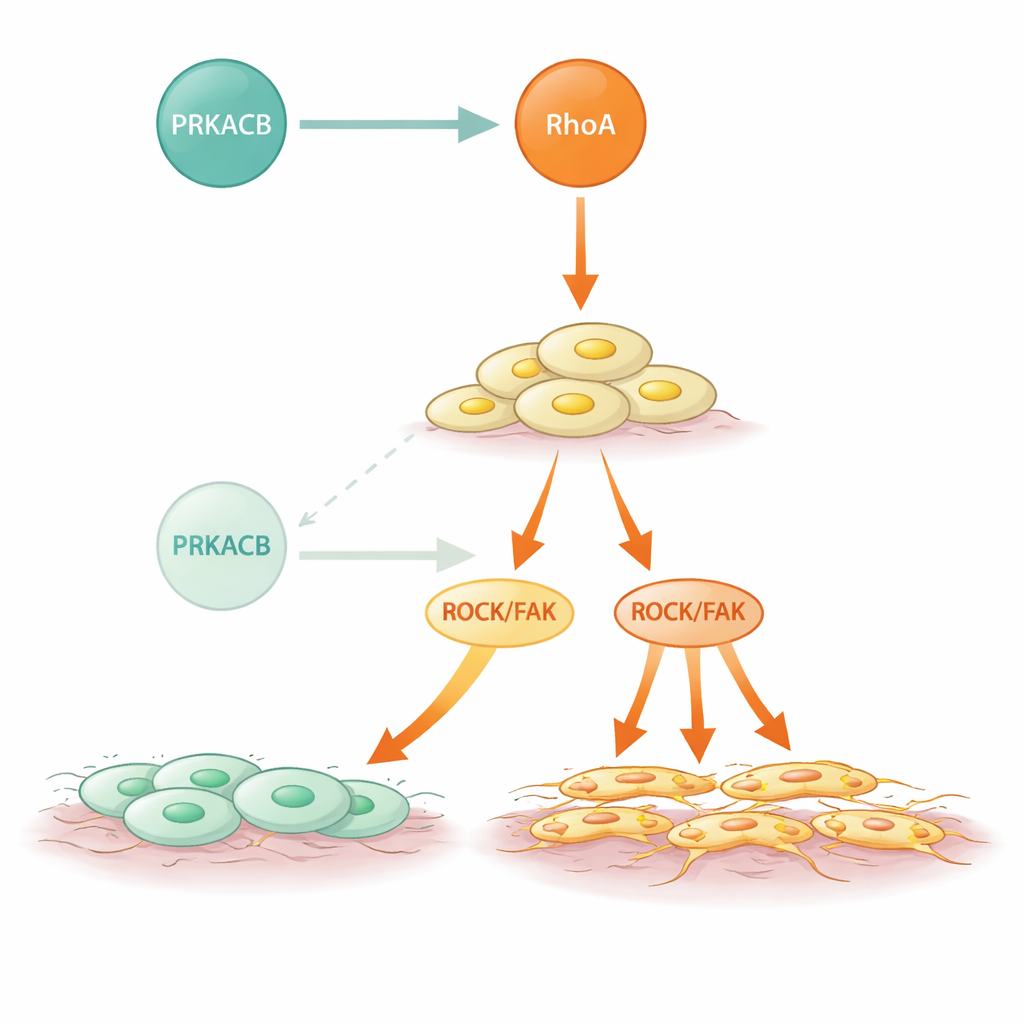
Sinalização mutante e uma possível forma de intervenção
Os cânceres gástricos de tipo difuso frequentemente apresentam mutações em RHOA, e este estudo mostra como algumas dessas alterações ampliam o problema. Várias mutações frequentes associadas ao CGD na RhoA enfraqueceram ou aboliram sua ligação ao PRKACB, mas não prejudicaram a capacidade da RhoA de ativar seus parceiros downstream. Como resultado, essas formas mutantes escaparam da fosforilação inibidora pelo PRKACB e exibiram atividade ROCK elevada e comportamento invasivo mais forte. De maneira marcante, quando os pesquisadores trataram células e camundongos com um composto bloqueador da RhoA, a metástase extra causada pela baixa expressão de PRKACB foi em grande parte revertida. Isso sugere que mesmo em tumores onde o freio natural é fraco ou ausente, mirar a via RhoA hiperativa diretamente pode conter a disseminação.
O que isso significa para pacientes e terapias futuras
Em termos simples, este trabalho identifica o PRKACB como parte chave de um circuito interno “anti-migração” no câncer gástrico de tipo difuso. Quando os níveis de PRKACB caem, ou quando a RhoA é mutada de modo que o PRKACB não possa se ligar e modificá‑la, a sinalização RhoA fica mais ativa, e as células cancerosas tornam-se mais aptas a se desprender e colonizar a cavidade abdominal. Medir o status de PRKACB e RhoA nos tumores pode ajudar os médicos a avaliar a probabilidade de metástase de um câncer e quem pode se beneficiar mais de drogas que inibam a via RhoA–ROCK–FAK. Embora esses tratamentos exijam mais desenvolvimento e testes clínicos, o estudo mapeia uma via molecular clara que vai de um freio ausente até a disseminação letal — e aponta novas formas de retardar essa jornada.
Citação: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Palavras-chave: câncer gástrico de tipo difuso, metástase, PRKACB, sinalização RhoA, via ROCK FAK