Clear Sky Science · pt
Miossina Nuclear 1 liga a arquitetura genômica à remodelação do tecido adiposo, inflamação metabólica e obesidade em camundongos
Por que o esqueleto da célula importa para a gordura corporal
A obesidade costuma ser atribuída ao que comemos e a quanto nos movimentamos, mas no interior das células a forma como o DNA é compactado e lido também pode desequilibrar as coisas. Este estudo revela que uma pequena proteína motora, a miossina nuclear 1 (NM1), que ajuda a organizar o DNA dentro do núcleo celular, desempenha um papel surpreendente na formação de adipócitos, no armazenamento de energia e no desencadeamento da inflamação. Ao estudar camundongos sem essa proteína, os pesquisadores descobriram uma ligação direta entre a arquitetura física dos nossos genes e o desenvolvimento de gordura visceral prejudicial e problemas metabólicos.
De células-tronco a adipócitos
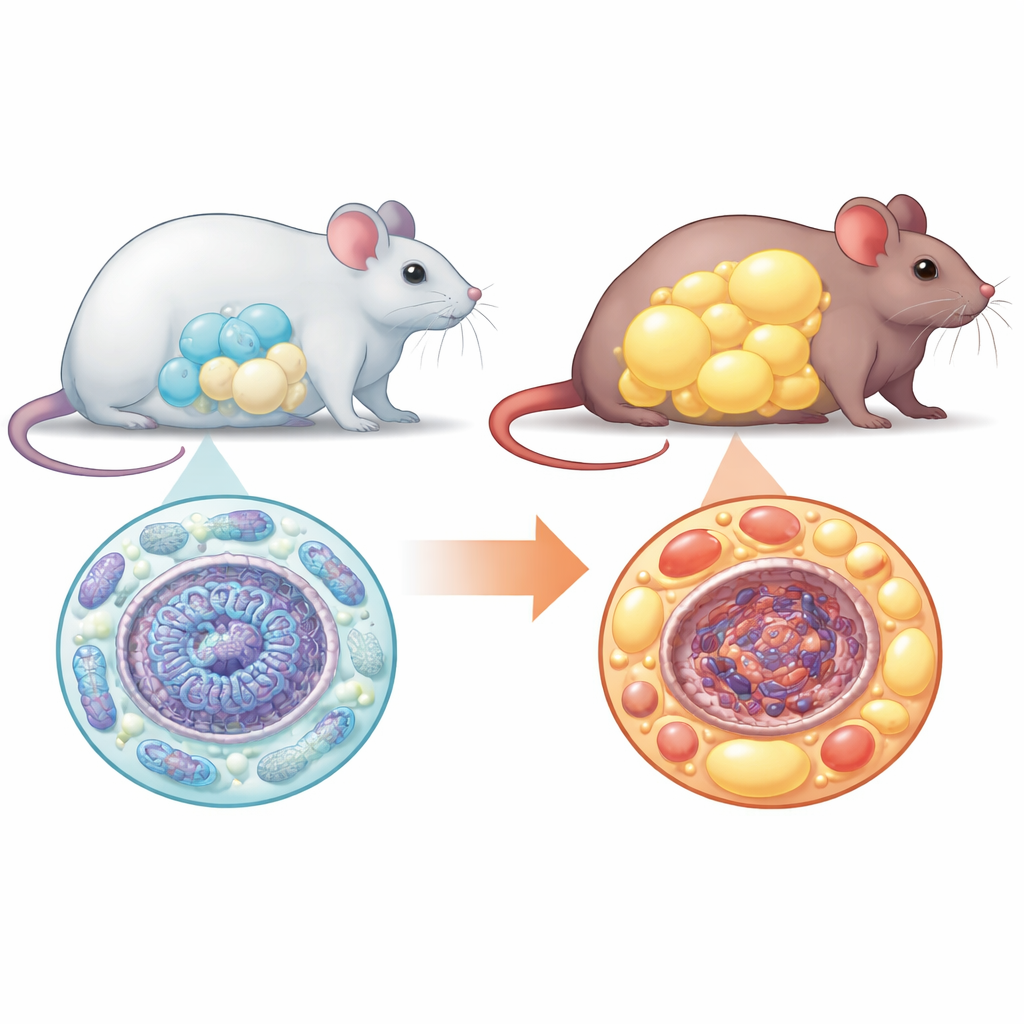
Os adipócitos se desenvolvem a partir de precursores versáteis chamados células-tronco mesenquimais. Normalmente, esses precursores se multiplicam, mudam seu uso de energia e amadurecem em muitas células de gordura pequenas e bem funcionantes que armazenam calorias em excesso com segurança. A equipe descobriu que, sem NM1, esse processo ordenado se desregula. Quando cultivaram células-tronco de camundongos normais e sem NM1 no laboratório e as induziram a se diferenciarem em adipócitos, muito menos células completaram a transição na ausência de NM1. As células que amadureceram eram visivelmente maiores que o normal, repletas de lipídios, mas sem as assinaturas gênicas e proteicas típicas de adipócitos saudáveis. Esse padrão — menos células, porém cada uma aumentada — é uma característica de tecido adiposo prejudicial.
Como o empacotamento do gene molda o comportamento do adipócito
A NM1 atua no núcleo, onde ajuda a manter trechos de DNA acessíveis para que genes importantes possam ser ativados. Para entender como sua perda altera o comportamento celular, os pesquisadores sobrepuseram mapas de regiões abertas do DNA com medidas de atividade gênica em células com e sem NM1. Eles observaram que muitos genes necessários para a formação de adipócitos, o manejo de gotas de gordura e a manutenção mitocondrial perderam tanto acessibilidade quanto atividade na ausência de NM1. Ao mesmo tempo, outros genes ligados a vias de crescimento e sinalização tornaram-se mais acessíveis e mais ativos. Isso aponta a NM1 como um controlador de tráfego essencial: ela ajuda a manter um equilíbrio entre regiões de DNA abertas e fechadas para que as redes gênicas corretas conduzam o desenvolvimento saudável dos adipócitos e do metabolismo.
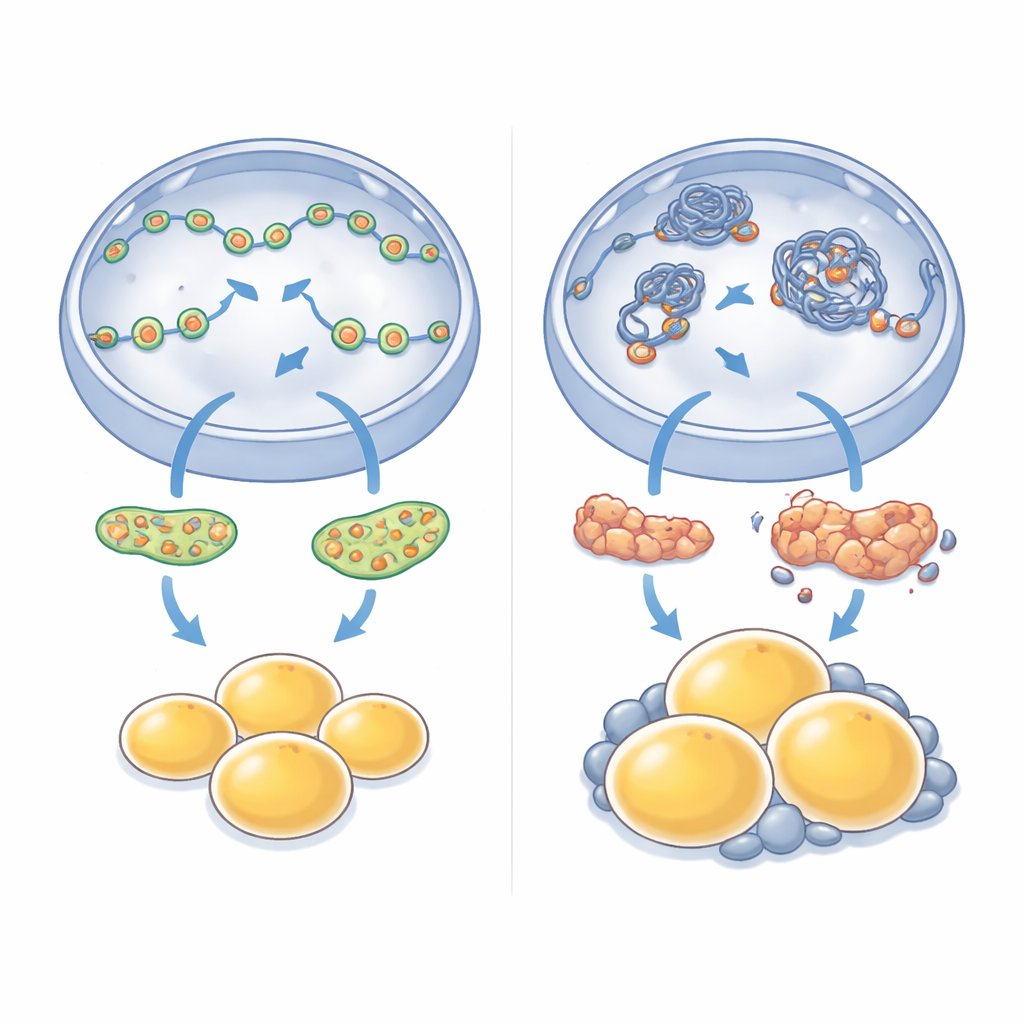
Quando mudanças locais viram ganho de peso no organismo
As consequências da perda dessa única motorina nuclear não ficaram confinadas às células em cultura. Camundongos sem NM1 gradualmente ficaram mais pesados que seus irmãos normais, embora não comessem mais alimento. Exames por imagem e análises de tecido mostraram um acúmulo claro de gordura, especialmente ao redor dos órgãos internos do abdome, e as células adiposas individuais nessas áreas estavam nitidamente aumentadas. Ao medir quais genes estavam mais ou menos expressos nessa gordura visceral, os pesquisadores encontraram mudanças abrangentes: vias envolvidas no uso de energia, sinalização da insulina e remodelamento tecidual foram reprogramadas. Genes associados ao crescimento e à expansão do tecido adiposo frequentemente estavam aumentados, enquanto vários controladores centrais da formação saudável de adipócitos estavam suprimidos, espelhando os defeitos observados em células-tronco cultivadas.
Tecido adiposo inflamado e motores de energia perturbados
Além do tamanho, o tecido adiposo em camundongos sem NM1 mostrou sinais de inflamação e estresse metabólico. Uma análise detalhada de vias destacou forte ativação de sinais imunes impulsionados por moléculas como interferon-gama e fator de necrose tumoral, conhecidas por contribuir para resistência à insulina e doenças metabólicas. Ao mesmo tempo, reguladores que promovem um tecido adiposo calmo e energeticamente eficiente foram suprimidos. O estudo também conectou a perda de NM1 a mitocôndrias perturbadas — os motores de energia da célula. Genes que normalmente supervisionam o controle de qualidade mitocondrial e a alternância entre produção eficiente de energia e energia rápida glicolítica foram desregulados, sugerindo que, na ausência de NM1, os adipócitos adotam uma estratégia energética menos eficiente e mais propensa ao estresse.
Sinais compartilhados entre camundongos e humanos
Para avaliar se essa via da motorina nuclear poderia importar em humanos, os autores examinaram grandes conjuntos de dados genéticos de gordura visceral humana. Eles se concentraram em um parente humano da NM1 chamado MYO1C e analisaram redes de variantes que modulam a atividade de genes próximos. Encontraram muitos dos mesmos temas vistos em camundongos — controle do citoesqueleto, sinalização imune e regulação metabólica — nas redes gênicas humanas centradas em MYO1C. Vários genes alterados na gordura de camundongos sem NM1 também estavam inseridos nessas redes humanas e já foram associados ao remodelamento do tecido adiposo e ao metabolismo. Essa sobreposição entre espécies sugere que mecanismos nucleares semelhantes podem influenciar o risco de obesidade em humanos.
O que isso significa para obesidade e saúde metabólica
Em conjunto, o trabalho mostra que a NM1 é muito mais do que um ajudante nuclear; é um hub central que liga a organização do DNA a como os adipócitos crescem, armazenam energia e se comunicam com o sistema imunológico. Quando a NM1 falta, os interruptores gênicos nos precursores adiposos ficam mal ajustados, as mitocôndrias funcionam mal, os adipócitos aumentam em tamanho em vez de se multiplicarem e a gordura visceral fica inflamada — uma combinação que se assemelha ao tecido adiposo prejudicial observado na obesidade e na resistência à insulina. Para o leitor leigo, a mensagem é que o arranjo físico do DNA e de suas proteínas auxiliares dentro do núcleo pode predispor os tecidos a uma expansão de gordura saudável ou prejudicial. Proteínas como a NM1 e sua contraparte humana MYO1C podem um dia tornar-se alvos para terapias que visem remodelar o tecido adiposo de dentro para fora, oferecendo uma forma mais precisa de enfrentar doenças relacionadas à obesidade.
Citação: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Palavras-chave: adipogênese, cromatina, mitocôndrias, gordura visceral, inflamação metabólica