Clear Sky Science · pt
Trimetilação da lisina 36 da histona H3 por SETD2 molda um panorama epigenético em células-tronco intestinais para orquestrar o metabolismo lipídico e atenuar a senescência celular
Por que as células-tronco intestinais importam à medida que envelhecemos
Nas camadas internas do revestimento intestinal, pequenas células-tronco trabalham sem parar para renovar o tecido que nos ajuda a digerir alimentos e absorver nutrientes. À medida que envelhecemos, essas células-tronco se cansam, deixando o intestino mais vulnerável a doenças e mais lento na reparação. Este estudo investiga como marcas químicas sutis nas proteínas que organizam o DNA mantêm as células-tronco intestinais jovens, como a perda dessas marcas perturba a queima de gordura dentro das células e como drogas selecionadas podem, no futuro, retardar esse declínio.
Células envelhecendo em um ambiente exigente
A superfície interna do intestino é um dos tecidos de renovação mais rápida do corpo. Células-tronco aninhadas na base de pequenos bolsões, chamados criptas, se dividem para repor bilhões de células a cada poucos dias. Esse trabalho constante exige um suprimento de energia estável, boa parte proveniente da degradação de gorduras. Ao mesmo tempo, essas células-tronco são controladas por um código “epigenético” — marcas químicas nas histonas que ajudam a determinar quais genes estão ativos ou silenciosos. Os autores focaram em uma dessas marcas, conhecida como trimetilação de H3K36, gerada por uma enzima chamada SETD2, e investigaram se alterações nessa marca poderiam explicar por que as células-tronco intestinais perdem vigor com a idade.
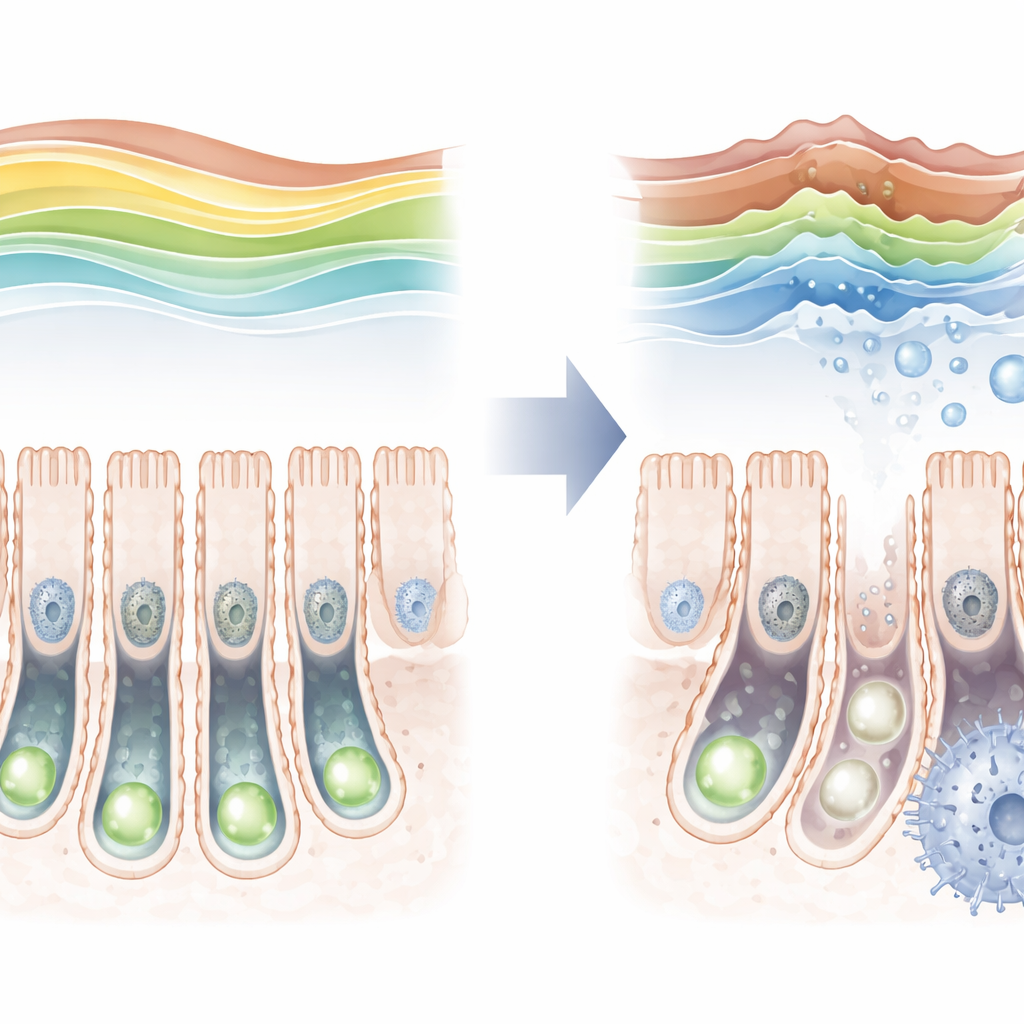
Uma marca protetora que enfraquece com a idade
Ao examinar intestinos de camundongos ao longo da vida, os pesquisadores descobriram que a marca de trimetilação de H3K36 não é estática. Ela é relativamente baixa logo após o nascimento, aumenta até um pico na fase adulta jovem e depois cai novamente na velhice. Conforme essa marca declinava em animais mais velhos, marcadores de envelhecimento celular aumentavam nas células-tronco, sugerindo uma relação entre os dois. Para testar isso de forma mais direta, a equipe criou camundongos em que SETD2 podia ser removida apenas nas células-tronco intestinais. Quando essa enzima foi deletada, a marca protetora praticamente desapareceu, as células-tronco se dividiram com menos frequência e tiveram dificuldade em gerar a gama completa de tipos celulares especializados do intestino.
Como mudanças epigenéticas atrapalham a queima de gordura
A perda dessa única marca de histona desencadeou uma cascata de alterações dentro das células-tronco. Medições de atividade gênica mostraram que muitos genes envolvidos no ciclo celular e na cópia do DNA foram reprimir, enquanto genes ligados ao estresse e ao envelhecimento foram ativados. De forma marcante, o sinal mais forte apontou para um manejo lipídico perturbado: genes que normalmente sustentam a oxidação de ácidos graxos — a queima controlada de gorduras para obter energia — foram reduzidos, e lipídios começaram a se acumular dentro das criptas. Perfis de metabólitos confirmaram que ácidos graxos de cadeia longa se acumulavam, sinal de que as vias habituais de processamento de gordura estavam falhando. Ao mesmo tempo, o empacotamento físico do DNA no núcleo mudou, com muitas regiões tornando-se mais expostas ou mais fechadas, remodelando quais genes a célula poderia usar com facilidade.
Remodeladores de cromatina e a marcha rumo à senescência
Para entender como essas mudanças no empacotamento do DNA ocorrem, os autores mapearam tanto regiões de cromatina aberta quanto um conjunto de outras marcas de histonas pelo genoma. Quando a trimetilação de H3K36 foi perdida, grandes trechos de DNA ganharam marcas “ativas” e tornaram-se mais acessíveis, especialmente perto de genes ligados ao metabolismo e ao envelhecimento. Um ator-chave nessa transição foi o complexo remodelador de cromatina SWI/SNF, impulsionado por uma subunidade central chamada SMARCA4. Em células-tronco sem SETD2, os níveis de SMARCA4 aumentaram, e o complexo aparentemente ajudou a abrir regiões que promovem programas de senescência. Quando os pesquisadores reduziram a atividade de SMARCA4 geneticamente ou com um inibidor específico, as células-tronco recuperaram parte da capacidade de formar mini-intestinos saudáveis em cultura, e os marcadores de envelhecimento diminuíram — sugerindo que o remodelamento excessivo empurra essas células para um estado cansado e senescente.
Reacendendo vias energéticas para resgatar células-tronco
Como a perturbação da queima de gorduras surgiu como problema central, a equipe testou se reforçar essa via poderia contrabalançar o envelhecimento das células-tronco. Eles usaram uma droga que ativa PPARα, um regulador mestre da oxidação de ácidos graxos. Em organoides derivados de células-tronco deficientes em SETD2, esse tratamento aumentou o crescimento, restaurou as estruturas budentes características de células-tronco vigorosas e reduziu o acúmulo de lipídios. Em camundongos vivos, a mesma intervenção repôs parcialmente o reservatório de células-tronco, diminuiu marcadores de senescência e normalizou o acúmulo lipídico nas criptas intestinais. Esses achados colocam a oxidação de ácidos graxos como um elo crucial entre o controle epigenético e a saúde das células-tronco.
O que isso significa para um envelhecimento saudável
Em conjunto, o trabalho mostra que uma marca específica de histona, depositada por SETD2, ajuda a manter um panorama epigenético equilibrado nas células-tronco intestinais. Quando essa marca enfraquece, a cromatina sofre remodelamento anômalo, as vias de queima de gordura falham, lipídios se acumulam e as células derivam para a senescência, comprometendo o sistema de reparo do intestino. Ao reduzir a maquinaria de remodelamento hiperativa ou restaurar o metabolismo lipídico com drogas direcionadas, pode ser possível preservar a função das células-tronco e a saúde intestinal em idades avançadas. Embora esses achados provenham de camundongos, eles ecoam padrões vistos em distúrbios intestinais humanos, abrindo a possibilidade de que terapias metabólicas cuidadosamente ajustadas possam um dia ajudar a contrariar o declínio relacionado à idade nas nossas próprias células-tronco intestinais.
Citação: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Palavras-chave: células-tronco intestinais, epigenética, oxidação de ácidos graxos, senescência celular, SETD2