Clear Sky Science · pt
Um RNA associado à Lamp2a secretado por ADSCs previne o feedback ENO1–lactilação–glicólise e o comportamento maligno celular no câncer de mama triplo-negativo
Por que isso importa para os pacientes
O câncer de mama triplo-negativo é uma das formas mais agressivas de câncer de mama e não possui os alvos hormonais ou de fatores de crescimento que tornam outros subtipos mais tratáveis. Este estudo revela como esses tumores reconfiguram seu uso de energia para sobreviver em ambientes com baixo oxigênio e descreve uma maneira inovadora de atacar essa reconfiguração. Para o leitor, oferece uma visão de como entender o metabolismo do câncer pode levar a novas terapias altamente direcionadas, diferentes da quimioterapia tradicional.
Como esses tumores se abastecem
Muitos cânceres dependem fortemente de uma via rápida, porém ineficiente, de produção de energia chamada glicólise, que transforma açúcar no subproduto lactato. Ao examinar amostras de pacientes, bancos públicos de genes e várias linhas celulares de câncer de mama, os pesquisadores mostram que os tumores triplo-negativos dependem ainda mais da glicólise do que outros cânceres de mama. Uma enzima chave nessa via, ENO1, está presente em níveis especialmente altos nesses tumores e se associa a pior sobrevida. Quando os níveis de ENO1 foram reduzidos em células triplo-negativas cultivadas em laboratório, as células migraram da glicólise para uma produção de energia mais normal nas mitocôndrias, cresceram mais lentamente e tiveram menor capacidade de invadir ou formar colônias.
Um ciclo de feedback perigoso dentro das células cancerosas
Ao aprofundar, a equipe descobriu que o próprio lactato fortalece a ENO1 e aprisiona as células cancerosas em um ciclo vicioso. O lactato pode modificar quimicamente proteínas em um processo chamado lactilação. Em células triplo-negativas, o excesso de lactato aumentou a lactilação da ENO1, o que, por sua vez, elevou a atividade e a estabilidade da enzima, acelerando ainda mais a glicólise e produzindo mais lactato. Em condições de baixo oxigênio — típicas de tumores sólidos — esse ciclo se intensificou, ajudando as células cancerosas a resistir à morte celular e continuar proliferando. Bloquear a atividade da ENO1 com um inibidor de pequena molécula, ou reduzir a produção de lactato, enfraqueceu esse ciclo, conteve a glicólise e retardou o crescimento tumoral em camundongos.
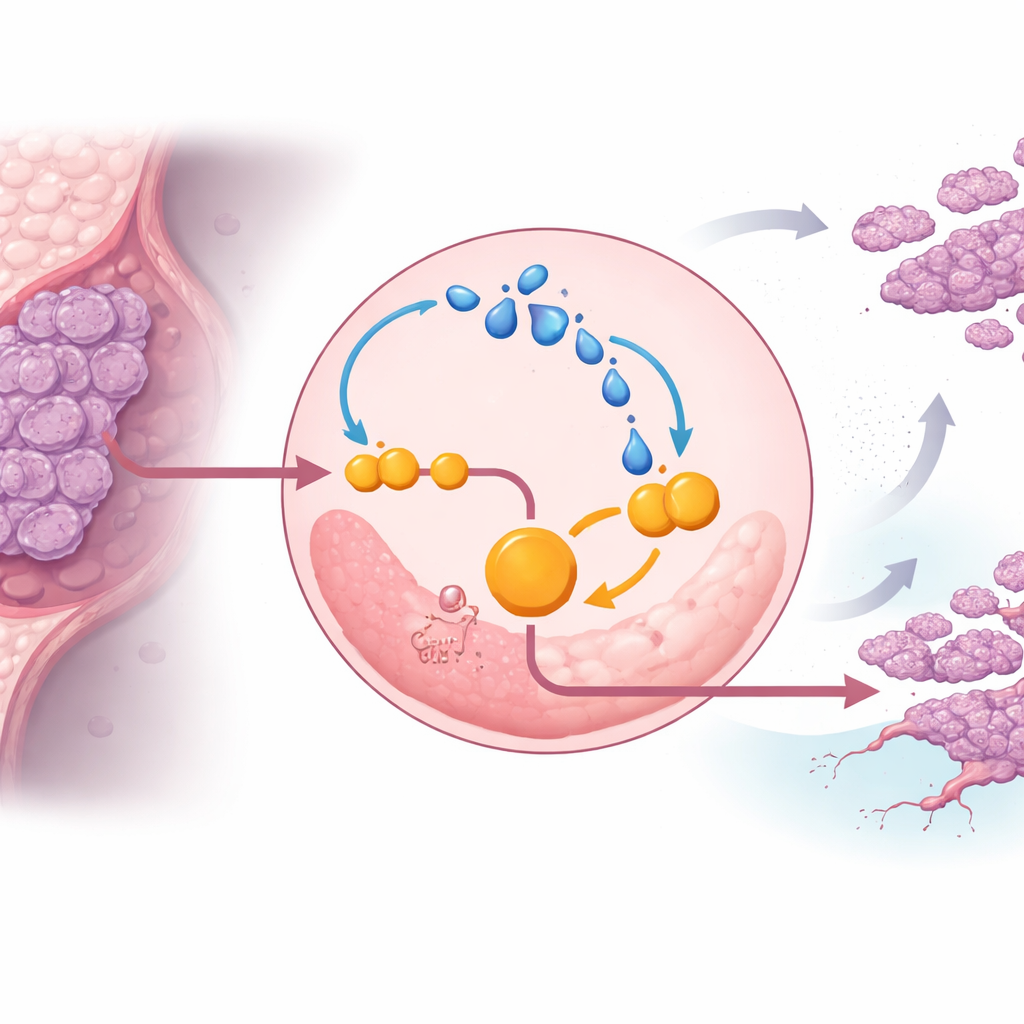
O interruptor molecular que protege a ENO1
O estudo identificou um ponto de controle específico na ENO1 que torna esse ciclo possível. Uma proteína conhecida como EP300 adiciona marcas baseadas em lactato a vários sítios de lisina na ENO1, sendo que um sítio, denominado K262, mostrou-se crucial. Quando esse sítio foi mutado de modo a não poder mais ser lactilado, a ENO1 foi rapidamente direcionada aos centros de reciclagem da célula, os lisossomos, e degradada. Sem essa marca protetora, as células triplo-negativas perderam grande parte de seu impulso glicolítico e da capacidade de formar tumores e metástases em modelos animais. Isso destaca a lactilação da ENO1 em K262 como um interruptor molecular que protege a enzima da destruição e mantém o metabolismo alterado do câncer.
Uma nova maneira de marcar a ENO1 para destruição
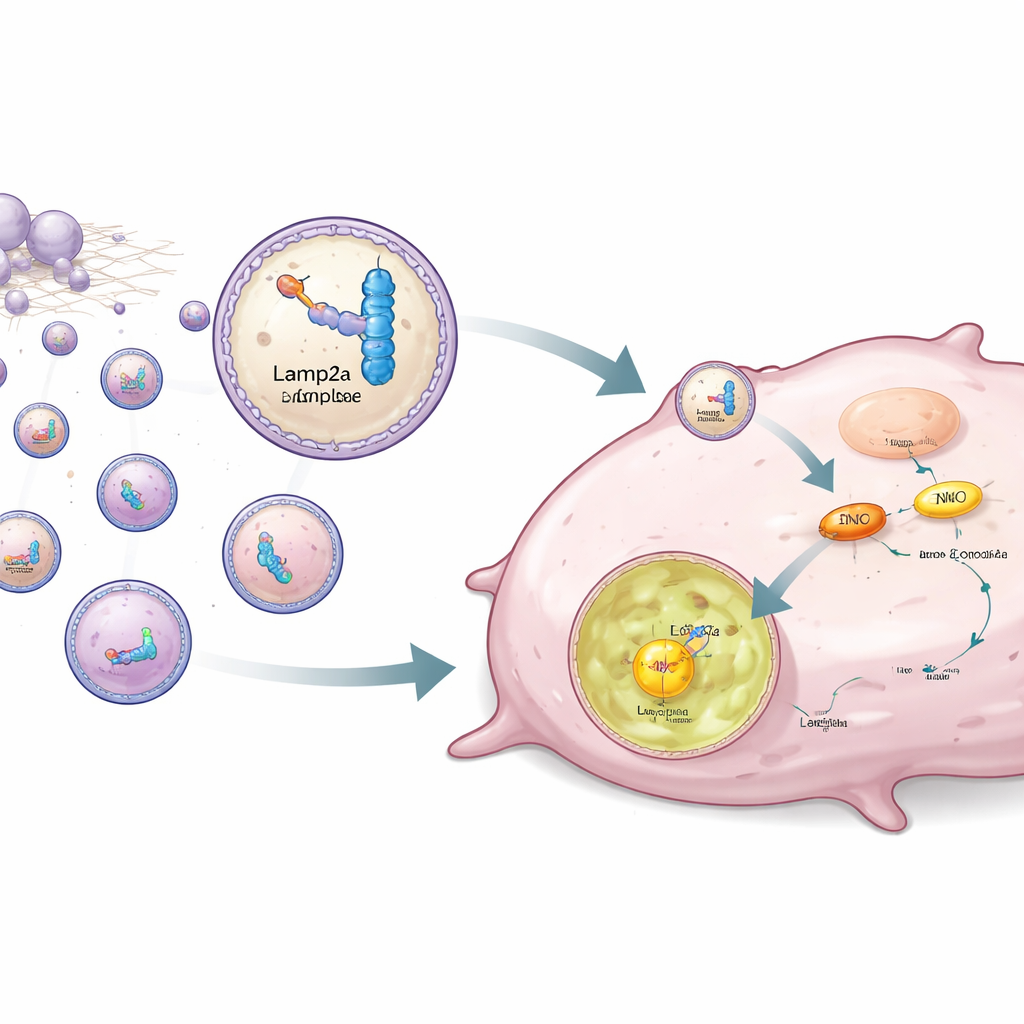
Em vez de apenas bloquear a ENO1, os autores desenharam uma estratégia para removê-la seletivamente das células cancerosas. A ENO1 também atua como proteína de ligação a RNA, reconhecendo sequências curtas específicas de RNA. A equipe projetou fragmentos de RNA sintéticos que se ligam fortemente à ENO1 e então os vinculou à Lamp2a, uma proteína de membrana lisossômica envolvida na degradação proteica direcionada. Células-tronco derivadas de tecido adiposo humano foram modificadas geneticamente para produzir esse par RNA–Lamp2a e empacotá-lo em pequenas vesículas chamadas exossomos. Quando esses exossomos modificados foram adicionados a células triplo-negativas, a porção de RNA se prendeu à ENO1, enquanto a parte Lamp2a guiou todo o complexo para os lisossomos, onde a ENO1 foi degradada, mesmo que carregasse a marca de lactilação estabilizadora.
Testando a abordagem de degradação direcionada em animais
Para aproximar essa ideia de uma terapia prática, os pesquisadores cultivaram as células-tronco modificadas em uma matriz biodegradável e implantaram esse construto sob a pele de camundongos, perto de tumores triplo-negativos. Desse local, as células-tronco liberaram continuamente exossomos carregando os complexos direcionados à ENO1. Os tumores desses animais mostraram níveis de proteína ENO1 marcadamente mais baixos, redução da glicólise, menos células em divisão e mais sinais de morte celular em comparação com os controles. Os tumores cresceram mais lentamente e seu comportamento maligno foi claramente atenuado, demonstrando que direcionar a ENO1 para os lisossomos pode efetivamente privar o câncer de sua via de combustível preferida.
O que isso pode significar para tratamentos futuros
Para um público não especializado, a mensagem principal é que este trabalho revela tanto uma vulnerabilidade quanto um novo ângulo terapêutico potencial para o câncer de mama triplo-negativo. A vulnerabilidade é a dependência do tumor em um ciclo de energia auto-reforçador centrado na ENO1 e no lactato, especialmente em regiões com baixo oxigênio. O ângulo terapêutico é um sistema de degradação proteica direcionada que usa RNA personalizado e exossomos derivados de células-tronco para arrastar a ENO1 para a maquinaria de descarte da célula. Embora esteja longe do uso clínico, essa abordagem ilustra como compreender profundamente os truques metabólicos do câncer pode inspirar terapias precisas que visam desarmar, em vez de simplesmente envenenar, as células malignas.
Citação: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Palavras-chave: câncer de mama triplo-negativo, metabolismo do câncer, sinalização por lactato, degradação proteica direcionada, enzima ENO1