Clear Sky Science · pt
A fosfatase Shp1 regula a estabilidade da proteína CXCR2 e a invasividade mediada por IL8 no câncer de mama
Por que esta pesquisa importa para o câncer de mama
O câncer de mama continua sendo uma das principais causas de morte por câncer em mulheres, em grande parte porque alguns tumores se tornam invasivos e se espalham para órgãos distantes. Este estudo desvenda como um sinal inflamatório comum nos tumores, chamado IL8, comunica-se com células de câncer de mama e como um "freio" molecular denominado Shp1 ajuda a decidir se essas células permanecem no lugar ou se tornam mais agressivas. Compreender essa disputa molecular pode abrir novas formas de retardar ou impedir a disseminação de cânceres de mama de difícil tratamento, especialmente a doença triplo-negativa.
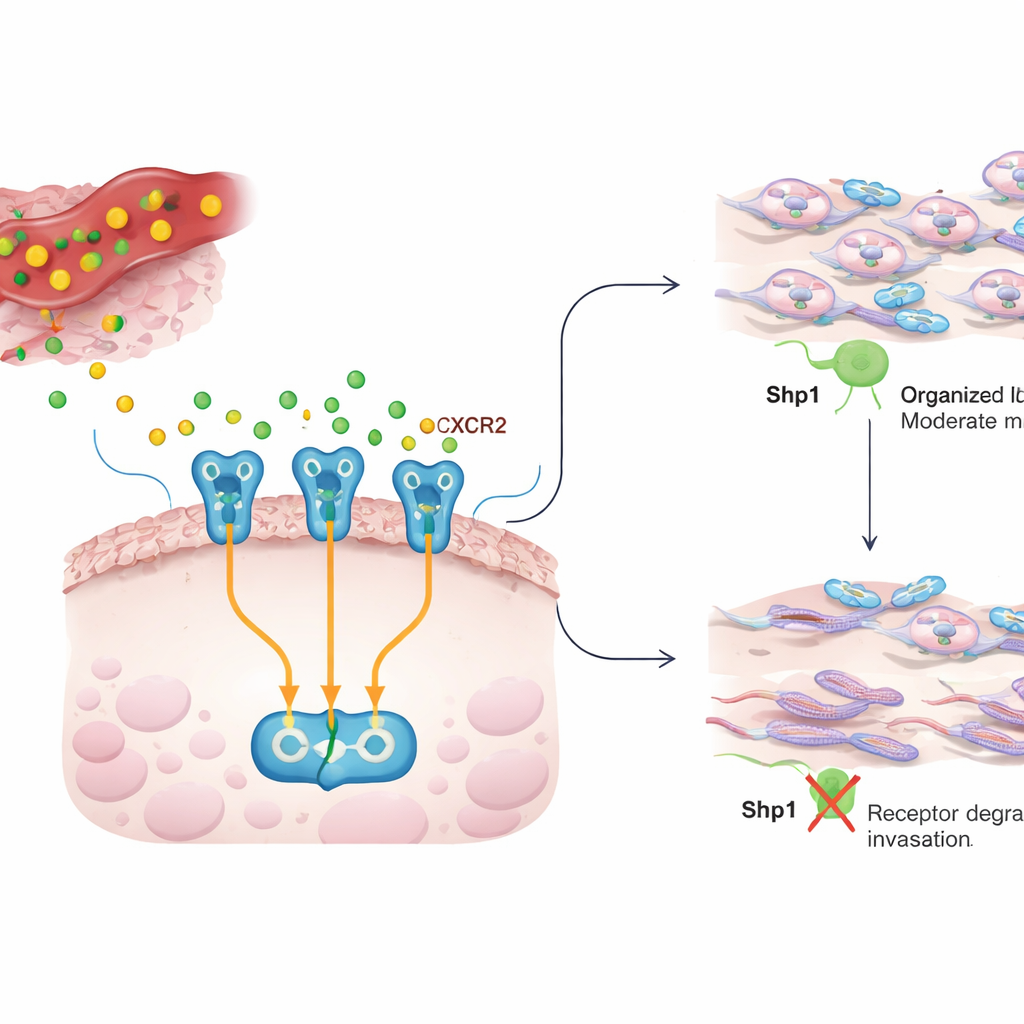
Uma conversa entre inflamação e células tumorais
No interior de um tumor, as células cancerosas estão cercadas por células imunes e de suporte que liberam mensageiros químicos, ou citocinas. A IL8 é um desses mensageiros e costuma estar presente em altos níveis em muitos cânceres, onde alimenta o crescimento, a formação de vasos sanguíneos e a capacidade das células tumorais de se mover e invadir. A IL8 sinaliza por meio de um receptor na superfície da célula tumoral chamado CXCR2. Quando a IL8 se liga ao CXCR2, ela ativa vários circuitos internos que reorganizam o esqueleto da célula, ajudando as células a rastejar pelo tecido e se espalhar. O trabalho atual investiga como essa conversa IL8–CXCR2 é mantida sob controle, e se a Shp1, uma enzima normalmente vista como um freio supressor de tumor em sinais de crescimento, também molda esse comportamento invasivo.
O papel oculto da Shp1 no movimento celular
Os pesquisadores primeiro removeram ou bloquearam quimicamente a Shp1 em uma linhagem de câncer de mama luminal amplamente usada (MCF7) e mediram quão bem as células podiam migrar e invadir através de um gel que imita o tecido. Sem Shp1, as células tumorais fecharam feridas mais rápido e passaram pelo gel com eficiência duas a três vezes maior, revelando que a Shp1 normalmente restringe o movimento. Usando dados de pacientes, eles também descobriram que mulheres cujos tumores expressavam menos Shp1 apresentaram pior sobrevida e tempo mais curto até a recidiva. Juntos, esses resultados sugerem que a Shp1 limita o comportamento agressivo das células de câncer de mama e que perder esse freio está ligado a resultados piores.
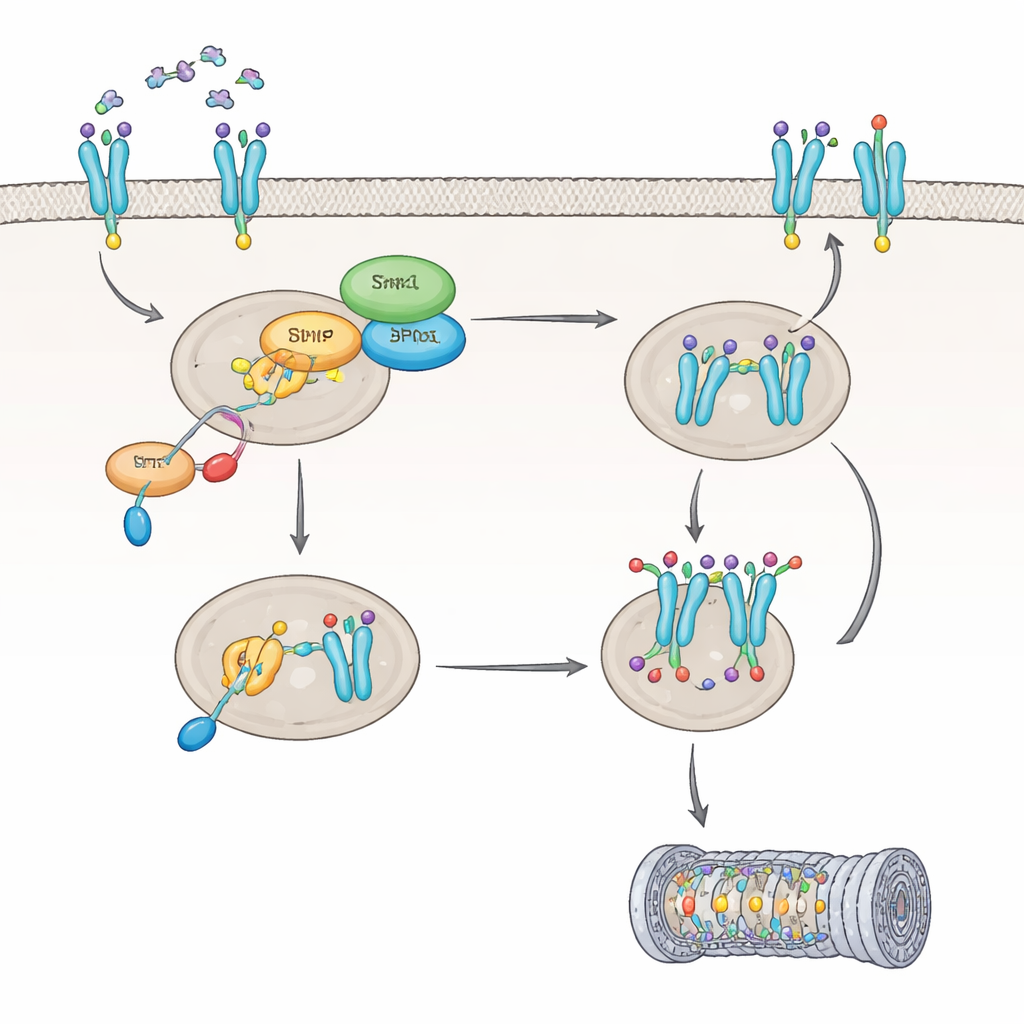
Como a IL8 desliga a Shp1 e reprograma um receptor-chave
Em seguida, a equipe explorou como a IL8 afeta a própria Shp1. Eles descobriram que a IL8 ativa uma proteína chamada PKC, que marca a Shp1 em um sítio específico, reduzindo sua atividade enzimática em cerca de 60%. Quando a Shp1 é atenuada dessa maneira, outra enzima, a PP2A, fica menos ativa, e o receptor CXCR2 permanece em um estado altamente modificado que altera seu destino dentro da célula. Em vez de ser limpo e reciclado de volta à superfície celular, o CXCR2 passa a ser marcado para destruição, principalmente via a maquinaria de degradação de proteínas da célula, o proteassoma. Uma modificação particular no CXCR2, no aminoácido Ser347, mostrou-se crucial para a fixação dessas marcas de degradação. Em células sem Shp1, o CXCR2 foi mais intensamente marcado e degradado mais rapidamente, levando a menos receptores na superfície celular e a uma resposta atenuada à IL8 ao longo do tempo.
Diversos tipos de câncer de mama, diferentes conexões
O câncer de mama não é uma única doença; os tumores são agrupados em subtipos luminal, HER2-positivo e triplo-negativo com base em seus padrões de receptores. Os pesquisadores testaram o circuito IL8–CXCR2–Shp1 em várias linhagens celulares representando cada subtipo. Em células luminais e triplo-negativas, a IL8 ativou a cascata Shp1–PP2A–CXCR2, e o bloqueio de Shp1 tanto aumentou a invasividade basal quanto eliminou o efeito pró-invasivo habitual da IL8. Em contraste, células HER2-positivas ainda respondiam à IL8, mas o bloqueio de Shp1 mal alterou seu comportamento, sugerindo que nesses tumores a Shp1 está ocupada por outros sinais, como o HER2, e menos disponível para regular o CXCR2. Análises em larga escala de expressão gênica apoiaram esse quadro: linhagens triplo-negativas tendiam a ter menor Shp1, sinalização relacionada a GPCR alterada e níveis maiores de IL8, consistente com um perfil mais agressivo e dirigido pela inflamação.
O que isso significa para tratamentos futuros
Para um público não especializado, a mensagem central é que a enzima Shp1 atua como um controlador de tráfego para o receptor de IL8, CXCR2, determinando se o receptor é reutilizado ou destruído e, por sua vez, o quão fortemente as células de câncer de mama podem responder a sinais inflamatórios. Em tumores luminais e triplo-negativos, esse ponto de controle parece especialmente importante: quando os níveis de Shp1 são baixos ou sua atividade é bloqueada, as células ficam mais invasivas e os desfechos dos pacientes pioram. Como a Shp1 pode ser aumentada ou modulada por certos fármacos existentes, mirar o eixo Shp1–CXCR2, possivelmente em combinação com bloqueadores de IL8 ou CXCR2, pode oferecer uma nova estratégia para limitar a invasão e a metastização em subtipos agressivos de câncer de mama.
Citação: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Palavras-chave: invasão do câncer de mama, sinalização IL8, receptor CXCR2, fosfatase Shp1, câncer de mama triplo-negativo