Clear Sky Science · pt
CRMP2 inibe a formação de metástases ao prejudicar a estabilização dependente de ILF3 do mRNA de CXCL10 no câncer de mama
Por que impedir a disseminação do câncer é importante
A maioria das mortes por câncer de mama não ocorre por causa do tumor original, mas porque células cancerosas migram para órgãos vitais, como os pulmões, e formam novos crescimentos. Este estudo revela uma proteína protetora intrínseca nas células do câncer de mama que pode retardar ou mesmo bloquear essa disseminação ao alterar o “tapete de boas‑vindas” que órgãos distantes preparam para as células cancerosas errantes. Entender esse interruptor de segurança oculto pode abrir caminho para novos tratamentos que impeçam o câncer de se estabelecer em outras partes do corpo.
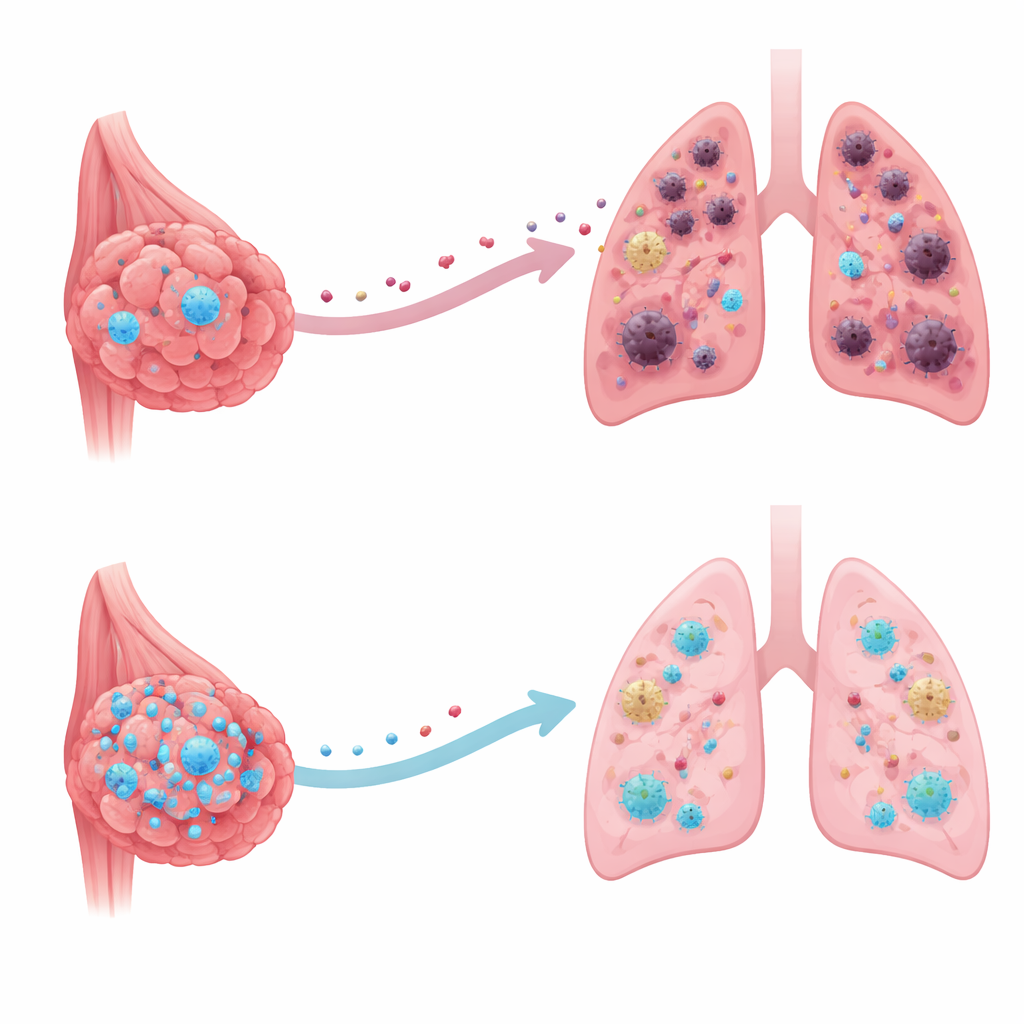
Um defensor discreto dentro das células tumorais
Os pesquisadores concentraram‑se em uma proteína chamada CRMP2, mais conhecida por ajudar neurônios a crescer e manter seu esqueleto interno. Ao examinar grandes bancos de dados públicos de câncer e amostras de tumores de pacientes, eles descobriram que os níveis de CRMP2 eram incomumente baixos em tumores de mama, especialmente em cânceres que já haviam metastizado. Pacientes cujos tumores apresentavam quantidades mais altas de CRMP2 tendiam a viver mais e tinham menor probabilidade de desenvolver metástases distantes. Esse padrão sugeriu que o CRMP2 se comporta mais como um freio do que como um acelerador no câncer de mama, atuando como um defensor interno em vez de um indutor da doença.
Como os pulmões são preparados para a invasão
Células cancerosas raramente chegam a um órgão distante por surpresa. Muito antes de sua chegada, o tumor primário libera moléculas que remodelam esse órgão em algo que os cientistas chamam de “nicho pré‑metastático” — um microambiente que favorece a sobrevivência do câncer. Usando um modelo de camundongo bem estabelecido que imita de perto o câncer de mama humano, a equipe mostrou que, quando as células tumorais mamárias foram modificadas para produzir CRMP2 em excesso, os tumores primários cresceram na mesma velocidade, mas os pulmões tornaram‑se muito menos hospitaleiros. Marcadores de inflamação e remodelamento tecidual nos pulmões diminuíram, e menos células imunes que normalmente suprimem as defesas antitumorais foram recrutadas. Como resultado, após a remoção do tumor primário, formaram‑se muito menos nódulos metastáticos nos pulmões.
Uma cascata de sinalização que provoca problemas
Aprofundando, os cientistas perguntaram quais sinais secretados pelo tumor eram responsáveis por preparar os pulmões. Eles focaram em CXCL10, uma pequena proteína mensageira (quimiocina) conhecida por atrair certas células imunes e por reativar células tumorais dormentes. Em células de câncer de mama humanas e de camundongo cultivadas em laboratório, o aumento de CRMP2 reduziu drasticamente a quantidade de CXCL10 produzida e liberada. Em camundongos, pulmões expostos a material tumoral rico em CRMP2 mostraram níveis muito mais baixos de CXCL10 e menos células imunes entrantes que normalmente abafam a atividade de células T protetoras. Quando os pesquisadores bloquearam CXCL10 com um anticorpo, a colonização pulmonar por células cancerosas diminuiu; quando adicionaram CXCL10 em excesso, o efeito protetor do CRMP2 foi anulado. Isso posicionou CXCL10 claramente a jusante do CRMP2 como um instigador chave de um nicho favorável à metástase.
O intermediário oculto que estabiliza sinais prejudiciais
Como o CRMP2 atua dentro das células enquanto CXCL10 é secretado, a equipe suspeitou da existência de um intermediário molecular. Eles identificaram ILF3, uma proteína ligadora de RNA, como parceira direta do CRMP2. ILF3 se liga ao RNA que codifica CXCL10 e normalmente o protege da degradação, permitindo que mais proteína CXCL10 seja produzida. O CRMP2 liga‑se ao ILF3 em pontos de contato específicos e o marca para destruição pelo maquinário de reciclagem proteica da célula, encurtando a vida útil do ILF3 e rompendo sua proteção sobre o RNA de CXCL10. Quando os níveis de CRMP2 são altos, o ILF3 é degradado mais rapidamente, o RNA de CXCL10 torna‑se instável e menos da quimiocina inflamatória é secretada. Quando o ILF3 foi restaurado artificialmente, ele pôde reverter a supressão de CXCL10 pelo CRMP2, confirmando seu papel como o elo crucial nessa cadeia.
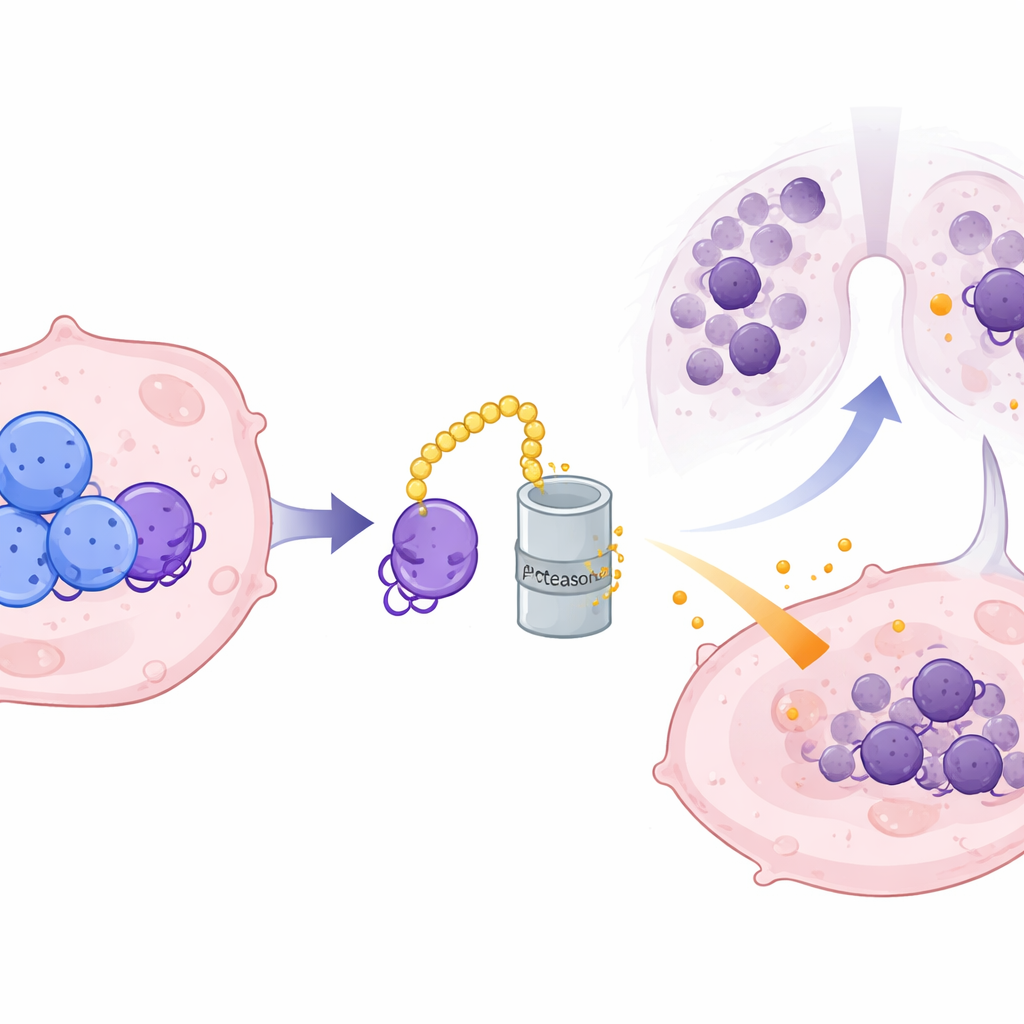
Transformando um composto vegetal em um aliado potencial
Para testar se essa via poderia ser aproveitada terapeuticamente, os pesquisadores triaram uma biblioteca de compostos naturais e descobriram que a psoraleno — uma molécula de origem vegetal usada há muito tempo em tratamentos de pele — liga‑se diretamente ao CRMP2 e o torna mais estável. Em experimentos celulares, a psoraleno elevou os níveis de CRMP2, reduziu ILF3 e CXCL10 e diminuiu o comportamento invasivo das células do câncer de mama sem prejudicar sua viabilidade geral. Em vários modelos de camundongo, a psoraleno não reduziu os tumores primários de mama, mas diminuiu fortemente as metástases pulmonares e atenuou a formação do nicho pré‑metastático, novamente de modo dependente do CRMP2. Embora a psoraleno em si possa causar toxicidade hepática e precise ser refinada, esses resultados mostram que pequenas moléculas podem reforçar o papel protetor do CRMP2.
O que isso significa para os pacientes
Em conjunto, este trabalho revela um eixo protetor dentro das células do câncer de mama no qual o CRMP2 desestabiliza o ILF3, que por sua vez reduz o CXCL10 e impede que os pulmões se tornem terreno fértil para metástases. Em vez de atacar diretamente as células cancerosas, essa estratégia visa desarmar os nichos distantes dos quais elas dependem, inclinando a balança a favor das defesas do próprio organismo. Embora muito ainda precise ser feito antes que essa abordagem chegue à clínica, mirar na via CRMP2–ILF3–CXCL10 — possivelmente com fármacos semelhantes à psoraleno mais seguros — oferece um ângulo promissor para impedir a disseminação do câncer de mama.
Citação: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Palavras-chave: metástase do câncer de mama, nicho pré‑metastático, sinalização por quimiocinas, proteínas ligadoras de RNA, terapêuticos derivados de produtos naturais