Clear Sky Science · pt
CCL11 promove a recorrência do carcinoma hepatocelular após cirurgia ao potencializar macrófagos M2-like imunossupressores CCR5+ CD206+ e ao favorecer a invasividade tumoral
Por que o câncer de fígado pode voltar após a cirurgia
A cirurgia hepática costuma ser a melhor esperança para pessoas com câncer de fígado em estágio inicial, mas muitos pacientes veem o câncer retornar dentro de alguns anos. Este estudo coloca uma pergunta simples, porém crucial: a resposta inflamatória do próprio corpo à cirurgia pode, involuntariamente, ajudar células tumorais remanescentes a crescer e se espalhar? Os pesquisadores se concentram em uma molécula sinalizadora chamada CCL11 e mostram como um surto dessa molécula após a cirurgia pode tanto enfraquecer a imunidade antitumoral quanto tornar as células tumorais sobreviventes mais agressivas.
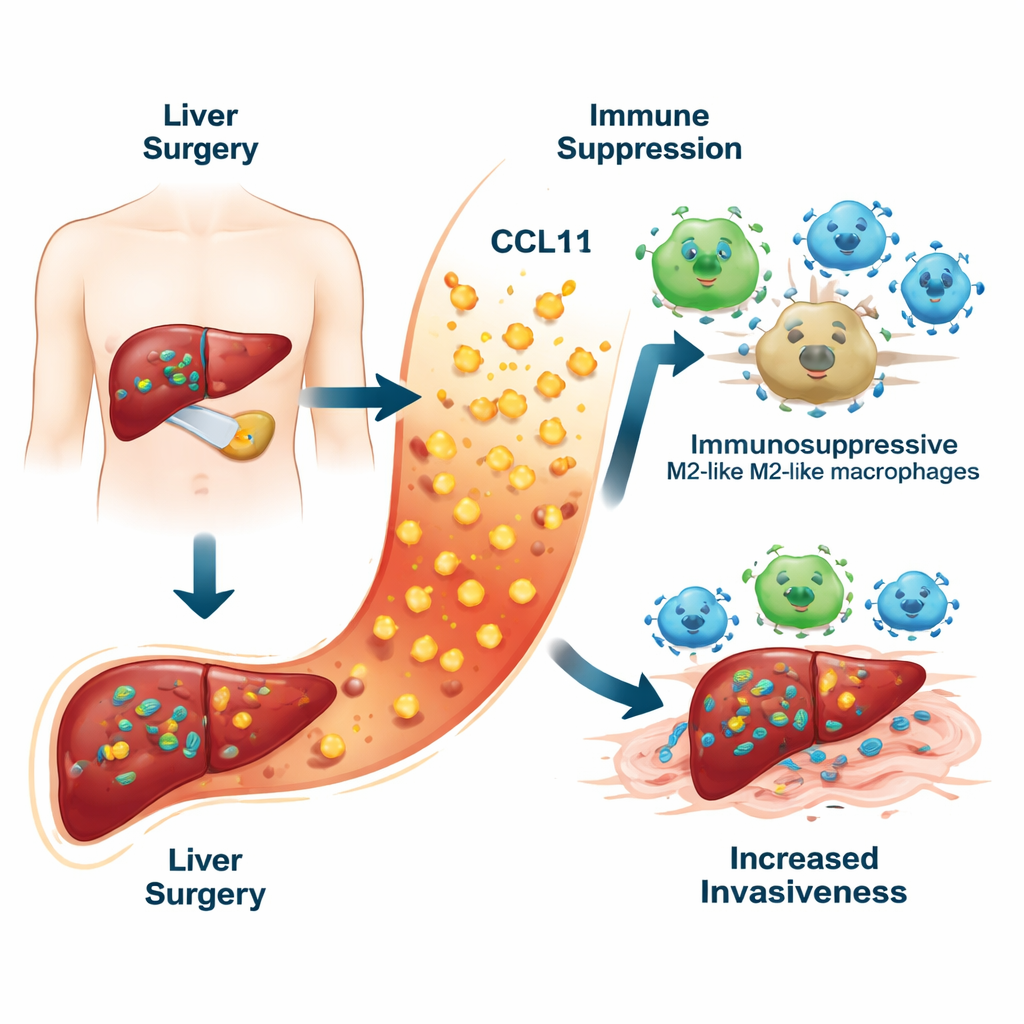
Um perigo oculto na resposta de cicatrização
Quando os cirurgiões removem um tumor hepático, é preciso pinçar vasos sanguíneos e lesionar o tecido ao redor. Esse dano desencadeia uma onda de inflamação que ajuda o fígado a cicatrizar. Ao medir dez moléculas inflamatórias diferentes no sangue de pacientes uma semana após a cirurgia, a equipe descobriu que uma quimiocina, CCL11, se destacou. Pacientes cujo câncer de fígado posteriormente recidivou apresentaram níveis significativamente mais altos de CCL11 do que aqueles que permaneceram livres de câncer. Níveis elevados de CCL11 também se associaram a pior sobrevida. Quando os pesquisadores combinaram CCL11 com dados clínicos rotineiros, como exames de sangue e características do tumor, eles construíram um “placar de risco” que previu a recorrência em cinco anos com mais precisão do que modelos tradicionais.
O tecido hepático que parece normal ainda importa
A maior parte da atenção na pesquisa do câncer se volta ao próprio tumor, mas este estudo mostra que o tecido hepático “normal” ao redor pode ser igualmente importante. Em amostras de mais de 100 pacientes, a CCL11 estava, na verdade, mais alta no tecido hepático não tumoral do que nos nódulos cancerosos ou em fígados de doadores saudáveis. Pacientes cujo tecido hepático próximo produzia mais CCL11 tinham maior probabilidade de doença avançada, disseminação à distância e recidiva após a cirurgia. Em modelos murinos que mimetizam a breve perda e retorno do fluxo sanguíneo durante uma operação, a lesão hepática elevou rapidamente os níveis de CCL11. Em condições de baixo oxigênio no laboratório, células de apoio do fígado, como miofibroblastos e células do endotélio vascular, também produziram mais CCL11, sugerindo que o estresse cirúrgico prepara o remanescente hepático inteiro para se tornar um ambiente pró-câncer.
Como a CCL11 transforma defensores imunes em espectadores
Para entender como a CCL11 molda a imunidade, os autores focalizaram macrófagos, células brancas versáteis que podem tanto atacar tumores quanto protegê-los. Eles descobriram que, no tecido hepático não tumoral, níveis mais altos de CCL11 andavam de mãos dadas com uma subpopulação de macrófagos que expressa o marcador CCR5 e exibe um perfil chamado M2-like, favorável ao tumor. Em pacientes, fígados ricos nesses macrófagos CCR5+ M2-like associaram-se a pior sobrevida. Em cultura celular, adicionar CCL11 levou monócitos a se diferenciarem nesse tipo imunossupressor de macrófago, aumentando moléculas como PD-L1 e IL-10 e liberando outros sinais que atraem e modulam mais células imunes. Esses macrófagos condicionados por CCL11 então incentivaram células T auxiliares naïve a se tornarem células T reguladoras, uma população conhecida por atenuar respostas antitumorais. Experimentos mecanísticos mostraram que a CCL11 ativa uma cascata de sinais dentro dos macrófagos que culmina na via NF-κB e na produção de PD-L1, ajudando a proteger as células cancerosas do ataque imunológico.
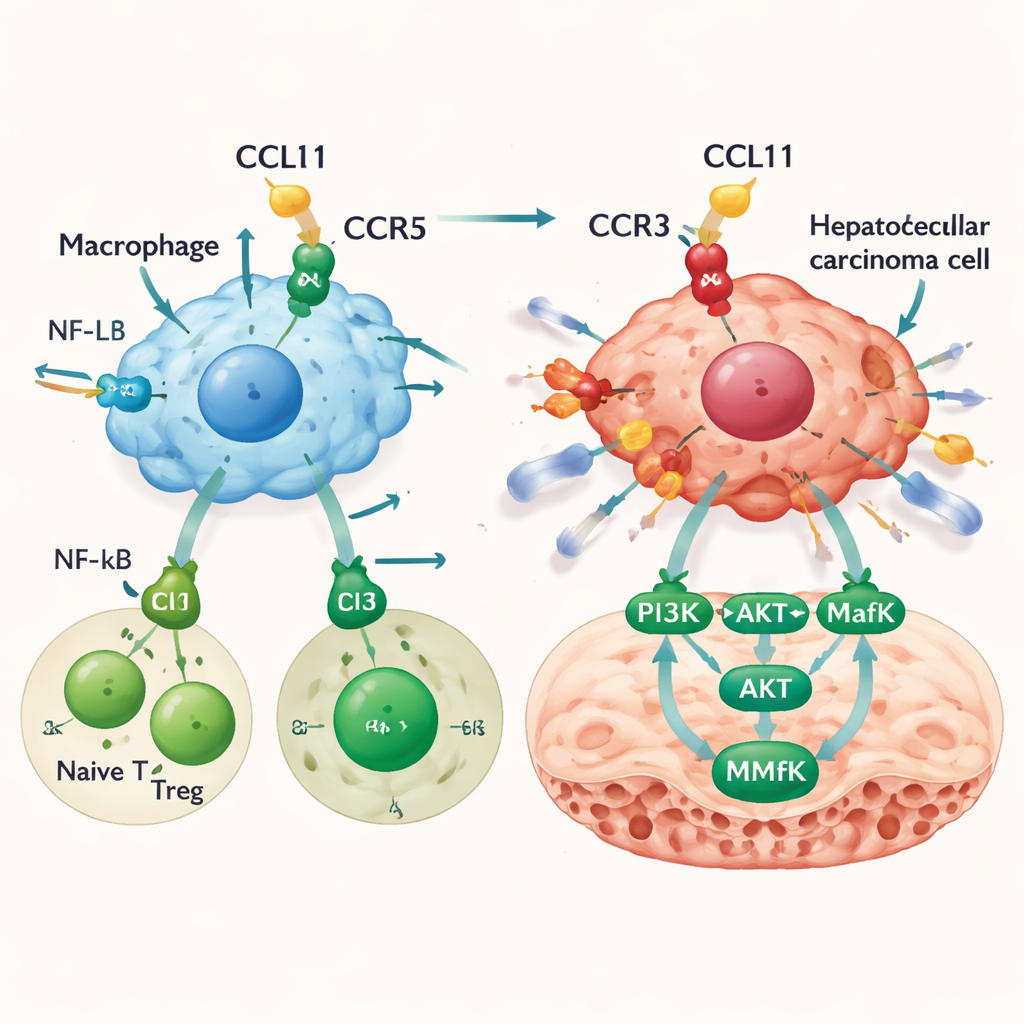
Como a CCL11 torna as células tumorais remanescentes mais invasivas
A CCL11 não apenas remodela a paisagem imune; ela também age diretamente sobre as células do câncer hepático. Embora as próprias células tumorais produzam pouca CCL11, elas carregam um de seus receptores, o CCR3. Em ensaios laboratoriais, a CCL11 não acelerou a multiplicação das células de câncer de fígado, mas aumentou sua migração e capacidade de invadir barreiras, uma característica do potencial metastático. Bloquear o receptor CCR3 anulou amplamente esse efeito. Análises de genes apontaram para uma via em que o sinal CCL11–CCR3 ativa PI3K e AKT, que então ativam um fator de transcrição chamado MafK. MafK, por sua vez, aumenta a produção de MMP13, uma enzima que degrada o tecido circundante e abre caminhos para a disseminação do câncer. Em modelos murinos, infundir CCL11 no fígado aumentou a carga tumoral e levou a mais metástases, juntamente com níveis mais altos da via PI3K–AKT–MafK–MMP13 dentro dos tumores.
Transformando um sinal arriscado em oportunidade terapêutica
Como a CCL11 parece tanto silenciar defesas imunes quanto fortalecer as células tumorais residuais, os pesquisadores testaram se bloqueá-la após a cirurgia poderia alterar os desfechos. Em camundongos com tumores hepáticos que foram cirurgicamente removidos, o tratamento com um anticorpo que neutraliza a CCL11 reduziu dramaticamente a taxa de retorno do câncer no fígado e melhorou a sobrevida, sem efeitos colaterais óbvios como perda de peso. Em conjunto, os achados apresentam a CCL11 como um interruptor mestre que conecta a lesão cirúrgica a um ambiente hepático imunossupressor e favorável à invasão. Para pacientes, este trabalho sugere que medir a CCL11 após a cirurgia poderia ajudar a identificar aqueles com maior risco de recidiva, e que fármacos que miram o eixo CCL11–CCR5/CCR3 podem, um dia, fazer parte de estratégias para impedir o retorno do câncer de fígado.
Citação: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Palavras-chave: recorrência do câncer de fígado, quimiocina CCL11, microambiente tumoral, supressão imunológica, metástase do câncer