Clear Sky Science · pt
Fibroblastos associados ao câncer promovem resistência ao osimertinibe em células de câncer de pulmão não pequenas via modificação NET1 m7G mediada por METTL1
Por que alguns cânceres de pulmão deixam de responder a um remédio “inteligente”
Medicamentos direcionados como o osimertinibe transformaram o tratamento para muitas pessoas com um tipo comum de câncer de pulmão, oferecendo mais tempo de sobrevida com menos efeitos colaterais do que a quimioterapia tradicional. Ainda assim, para a maioria dos pacientes, esses benefícios são temporários: os tumores acabam encontrando maneiras de ludibriar a droga. Este estudo faz uma pergunta aparentemente simples, mas de grande alcance: o tecido de suporte do tumor — especificamente células chamadas fibroblastos associados ao câncer — estaria silenciosamente ajudando as células cancerosas a escapar dos efeitos do osimertinibe?
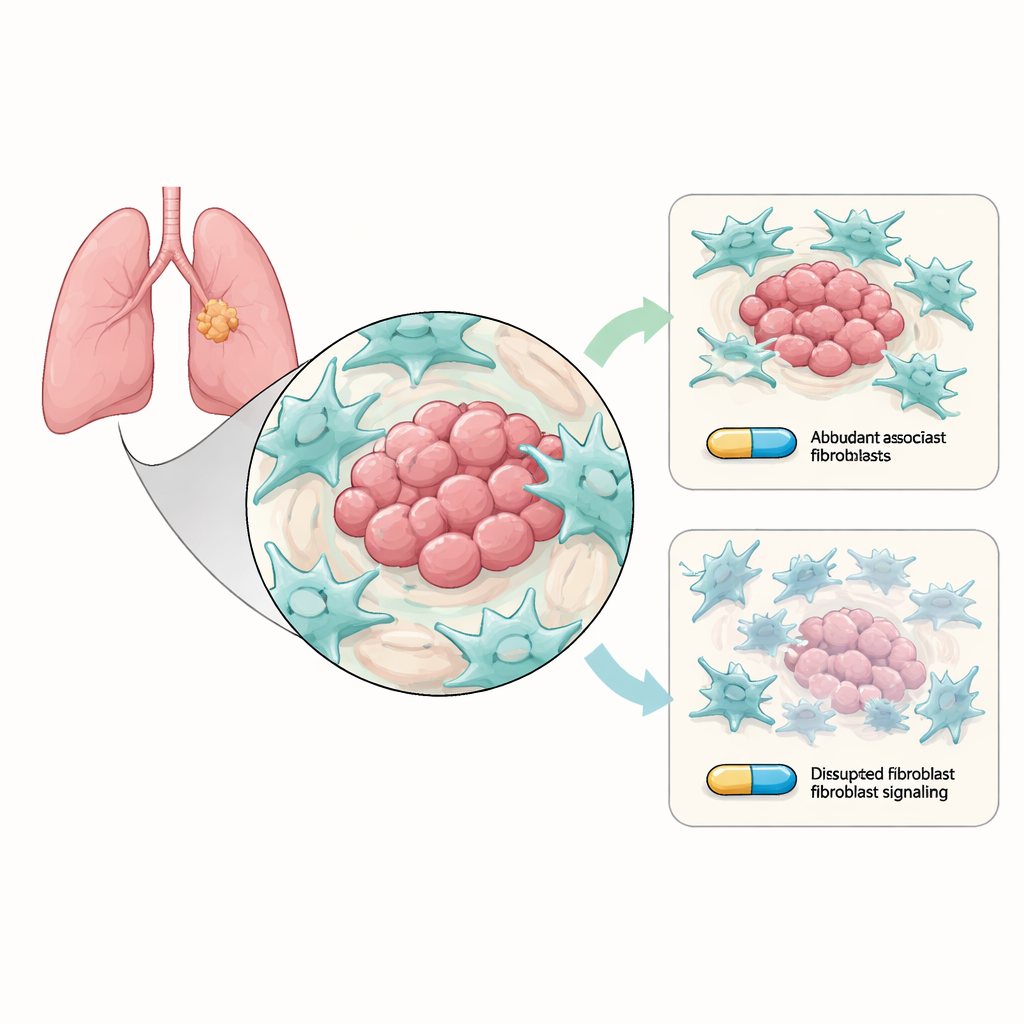
Células auxiliares que secretamente protegem o tumor
O câncer de pulmão não pequenas células cresce dentro de um bairro movimentado de células não cancerosas conhecido como microambiente tumoral. Entre os moradores mais abundantes estão os fibroblastos associados ao câncer (CAFs), células do tecido conjuntivo que remodelam a área ao redor do tumor. Os pesquisadores cultivaram células de câncer de pulmão com as habituais mutações do EGFR sensíveis ao osimertinibe junto com CAFs em laboratório. Eles descobriram que, quando os CAFs estavam presentes, as células cancerosas eram mais difíceis de eliminar com osimertinibe: formavam mais colônias, apresentavam menos autodestruição e mostravam traços “tipo estaminais” mais fortes, associados à sobrevivência de longo prazo e à recidiva. Em outras palavras, embora a droga ainda atingisse as células cancerosas, os fibroblastos ao redor as ajudavam silenciosamente a resistir.
Uma etiqueta química no RNA que muda as regras
A equipe então olhou além dos próprios genes para as etiquetas químicas que decoram o RNA — as cópias funcionais da informação genética dentro das células. Uma dessas etiquetas, chamada m7G, pode influenciar a estabilidade de uma molécula de RNA e a eficiência com que ela é traduzida em proteína. Usando testes bioquímicos e mapeamento em todo o genoma, os pesquisadores mostraram que os CAFs aumentam a marcação m7G geral nos RNAs dentro das células de câncer de pulmão. Esse aumento era impulsionado principalmente por uma enzima metiltransferase chamada METTL1, que coloca marcas m7G em RNAs mensageiros. Os níveis de METTL1 eram mais altos em tumores pulmonares do que no tecido normal adjacente e estavam ligados a doenças mais avançadas e pior sobrevida dos pacientes, sugerindo que essa enzima faz mais do que apenas ajustar funções celulares rotineiras.
Um sinal secretado e uma cadeia molecular vulnerável
Como os CAFs elevam o METTL1 nas células cancerosas? O estudo aponta para uma proteína chamada HMGB1, que os CAFs liberam no ambiente ao redor. Comparados com as células cancerosas, os CAFs secretaram quantidades muito maiores de HMGB1. Quando os pesquisadores adicionaram HMGB1 a células de câncer de pulmão, os níveis de METTL1 e as marcas m7G aumentaram; quando bloquearam o HMGB1 no meio condicionado por CAFs, esse efeito diminuiu. Aprofundando, eles identificaram um alvo de RNA chave do METTL1: NET1, um gene que ajuda a impulsionar o crescimento e a mobilidade celular. Os CAFs aumentaram tanto a marcação m7G quanto a abundância do RNA e da proteína NET1, e o METTL1 ligou-se fisicamente ao RNA NET1 para estabilizá-lo. Menos METTL1 significou menos NET1 modificado, sinais de sobrevivência das células cancerosas mais fracos e maior sensibilidade ao osimertinibe.
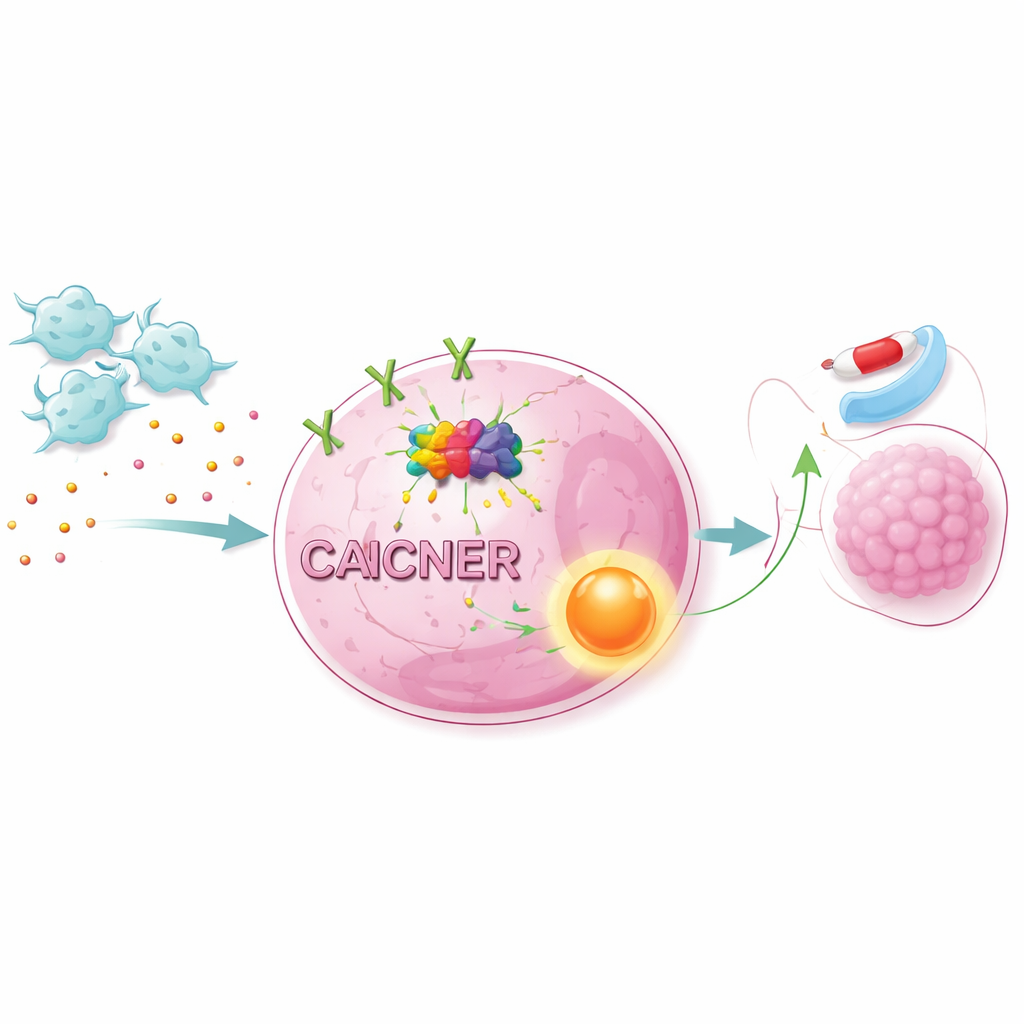
Ligando vias de sobrevivência dentro das células cancerosas
O sinal fortalecido de NET1 não atuou sozinho. Ao combinar grandes conjuntos de dados de RNA com análise de vias, os cientistas mostraram que os CAFs ativam uma via importante de crescimento e sobrevivência dentro das células conhecida como via AKT/NF-κB. Bloquear AKT ou NF-κB com inibidores específicos tornou as células de câncer de pulmão mais vulneráveis ao osimertinibe, mesmo na presença de CAFs. Alterar os níveis de NET1 teve efeitos semelhantes: reduzir NET1 enfraqueceu a proteção dos CAFs, enquanto aumentar NET1 ampliou a resistência. Em camundongos implantados com células humanas de câncer de pulmão, a adição de CAFs fez os tumores crescerem mais rápido e responderem menos ao osimertinibe. Silenciar METTL1 nas células cancerosas reduziu as marcas m7G, diminuiu NET1 e a ativação das vias, e cortou drasticamente o crescimento tumoral impulsionado pelos CAFs.
O que isso significa para o tratamento futuro do câncer de pulmão
Para pessoas com câncer de pulmão mutante em EGFR, este trabalho oferece uma nova forma de entender por que drogas potentes como o osimertinibe eventualmente fracassam. Em vez de atribuir a falha apenas a novas mutações nas células cancerosas, ele destaca uma cadeia molecular que começa fora da célula tumoral — com CAFs liberando HMGB1 — e segue por METTL1, marcas m7G no NET1 e ativação de vias de sobrevivência que atenuam o efeito da droga. Interromper essa cadeia em qualquer ponto poderia, em princípio, restaurar ou prolongar a sensibilidade ao tratamento. Embora fármacos que atinjam diretamente METTL1, HMGB1 ou RNAs específicos marcados por m7G ainda estejam em estágios iniciais, o estudo sugere que combinar osimertinibe com terapias direcionadas às células de suporte do tumor ou aos seus sinais de modificação de RNA pode ajudar a manter esse tipo de câncer de pulmão sob controle por mais tempo.
Citação: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Palavras-chave: resistência ao osimertinibe, câncer de pulmão não pequenas células, fibroblastos associados ao câncer, metilação de RNA, via METTL1 NET1