Clear Sky Science · pt
miR-424(322)~503 prejudica a progressão do câncer colorretal impulsionada pela deficiência de PTEN
Por que este estudo é importante para o câncer de cólon
O câncer de cólon continua sendo um dos tipos de câncer mais comuns e mortais no mundo, e muitos pacientes ainda progridem para doença avançada apesar de cirurgia, quimioterapia e terapias direcionadas. Este estudo investiga um pequeno conjunto de "interruptores" genéticos chamados microRNAs que podem desacelerar ou acelerar o crescimento tumoral. Ao revelar como um cluster específico de microRNAs interage com um conhecido gene supressor de tumor, PTEN, o trabalho ajuda a explicar por que alguns cânceres de cólon se tornam mais agressivos e aponta novas formas de prever risco e conceber terapias.
Pequenos interruptores de RNA com grande impacto
MicroRNAs são moléculas curtas de RNA que não codificam proteínas, mas ajustam finamente como centenas de genes são usados em uma célula. O cluster miR-424(322)~503, composto por dois microRNAs relacionados, intrigou pesquisadores porque pode atuar como freio ou acelerador em diferentes cânceres. No câncer de cólon, seu papel era incerto. Os autores focaram em tumores impulsionados pela perda de PTEN, um gene que normalmente mantém os sinais de crescimento sob controle e que é frequentemente alterado em tumores colorretais. Eles fizeram uma pergunta simples, porém potente: o que acontece com o desenvolvimento do câncer de cólon quando tanto o PTEN quanto esse cluster de microRNAs estão ausentes?
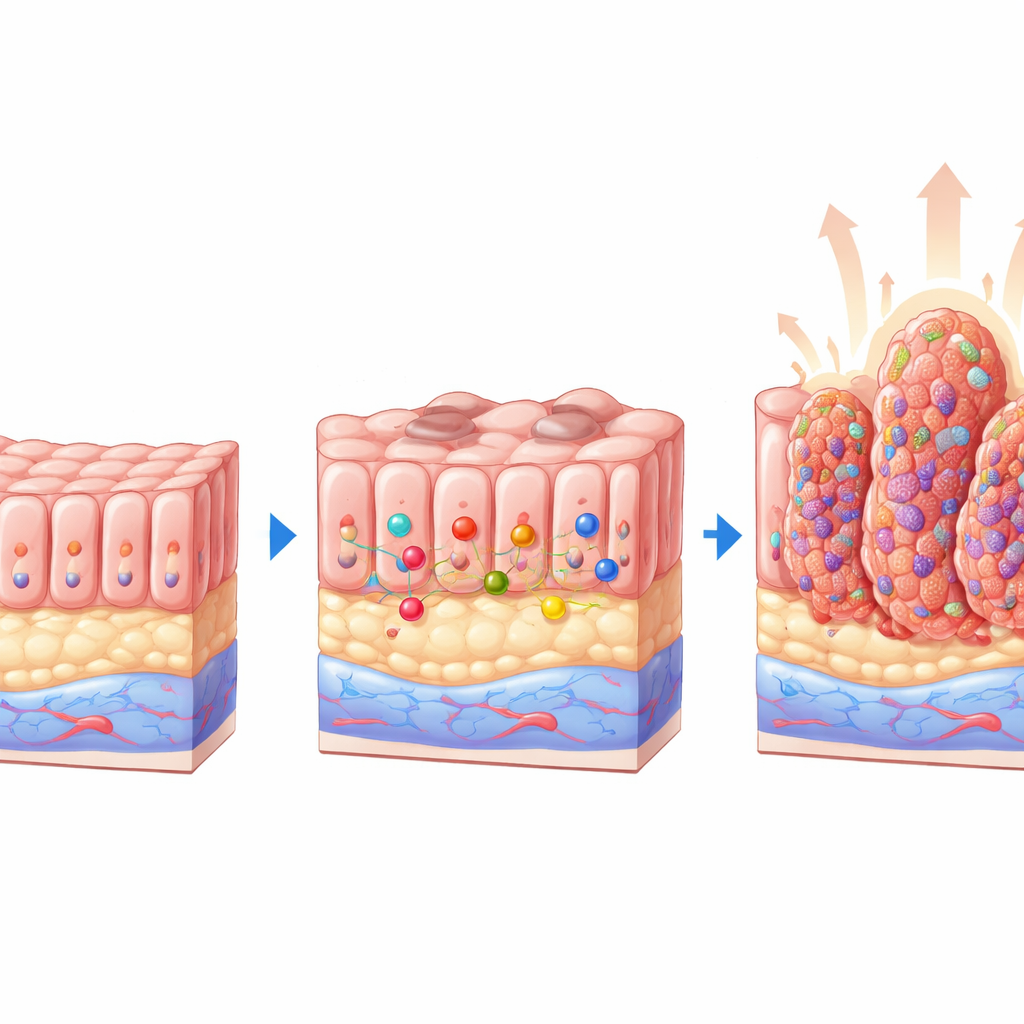
Modelos murinos revelam um papel protetor
Para responder, a equipe usou camundongos geneticamente modificados em que o PTEN pode ser desligado no revestimento intestinal, e os cruzou com animais que não possuem o cluster miR-424(322)~503. Isso gerou quatro grupos: animais normais, camundongos com falta apenas dos microRNAs, camundongos com falta apenas de PTEN e camundongos knockout duplo com ausência de ambos. Após induzir a perda de PTEN, examinaram cuidadosamente os cólons. Animais com falta apenas de PTEN desenvolveram múltiplos pequenos pólipos, muitos com tecido anômalo em estágio inicial. Em contraste marcante, camundongos sem PTEN e sem o cluster de microRNAs apresentaram muito mais lesões, pólipos maiores e uma proporção maior de alterações avançadas, incluindo displasia de alto grau e adenocarcinoma manifesto. O cluster de microRNAs por si só não causou doença, mostrando que sua perda é particularmente prejudicial quando o PTEN já está ausente.
Via clássica inalterada, mudança para novos culpados
O câncer de cólon é frequentemente impulsionado pela hiperativação da via Wnt/β-catenina, uma rota chave que controla as células-tronco no intestino. Como esse cluster de microRNAs pode influenciar essa via no tecido mamário, os autores testaram se o mesmo ocorria aqui. Surpreendentemente, os níveis e a localização da β-catenina e de seu correceptor LRP6 no cólon não mudaram quando o cluster de microRNAs foi removido, mesmo nos animais knockout duplos. Em vez disso, um perfil de expressão gênica em larga escala apontou para outro lado: tumores sem PTEN e sem os microRNAs exibiram fortes assinaturas de remodelamento tecidual, resposta a ferimentos e transição epitélio-mesenquimal, um programa ligado à invasão e metástase. Rotas de sinalização conduzidas por quinases MAP (ERK1/2 e p38) e pelo fator de crescimento TGFβ foram particularmente enriquecidas.
Como os sinais de crescimento saem do controle
Aprofundando-se, os pesquisadores examinaram proteínas no tecido do cólon. Eles descobriram que, enquanto a perda de PTEN isolada aumentou a via PI3K/AKT, a adição da perda do cluster de microRNAs produziu uma nova elevação na atividade MAPK: mais JNK, p38, MKK4 ativados e, especialmente, ERK1/2. Esses sinais altamente ativos coincidiram com níveis maiores de ciclina D1, um motor chave da divisão celular. Ao mesmo tempo, componentes da via TGFβ que promovem sua atividade (SMAD3 e SMAD4) aumentaram, enquanto um freio interno (SMAD7) diminuiu, e células cancerosas mostraram marcação nuclear mais intensa de SMAD2/3, consistente com ativação da via. Ao comparar genes de tumores murinos com alvos previstos de microRNAs, a equipe identificou IGF1, um potente fator de crescimento que alimenta as cascatas MAPK, como alvo direto do cluster miR-424(322)~503. Quando os microRNAs estavam ausentes, IGF1 escapou da repressão, impulsionando ainda mais a sinalização MAPK. Análises de conjuntos de dados de câncer de cólon humanos refletiram essas descobertas: IGF1 estava mais alto em tumores com baixos níveis de miR-424 ou miR-503, e o RNA longo não codificante que hospeda esses microRNAs, MIR503HG, assim como os próprios microRNAs, foram alterados coordenadamente em tumores de pacientes.
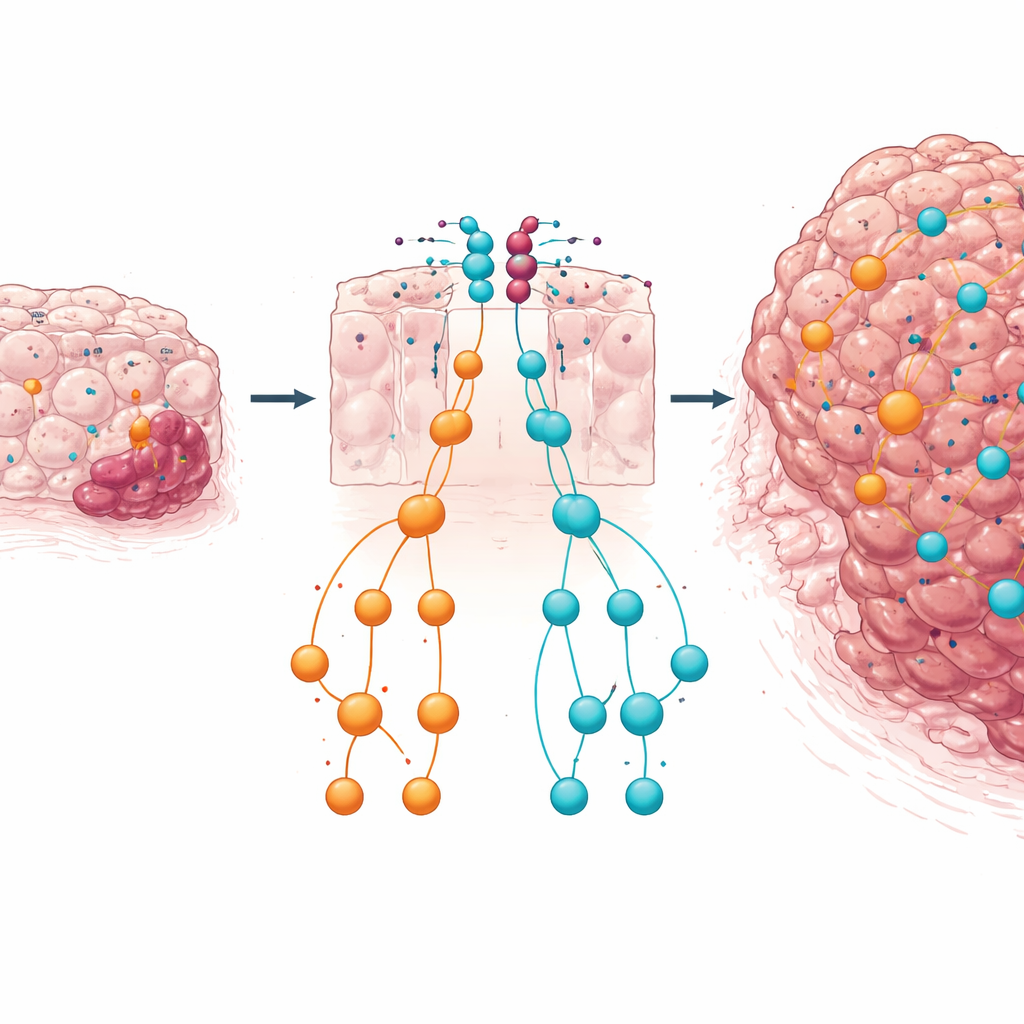
Uma dupla rede de segurança e o que isso significa para pacientes
Em conjunto, os resultados sugerem que, em tecido colorretal deficiente em PTEN, o cluster miR-424(322)~503 atua como uma segunda rede de segurança. Quando o PTEN é perdido, esses microRNAs são aumentados, em parte por sinais como TGFβ, e trabalham para conter vias de crescimento poderosas como IGF1–MAPK e TGFβ–SMAD. Se esse freio microRNA for removido, os sinais de crescimento e remodelamento correm sem controle, acelerando a transição de pólipos benignos para câncer invasivo. Para um leitor leigo, a mensagem chave é que nem todas as mudanças genéticas em um tumor empurram na mesma direção: algumas são defesas embutidas. Entender como PTEN e esse cluster de microRNAs cooperam para manter o crescimento celular em equilíbrio pode ajudar a identificar pacientes de alto risco e inspirar tratamentos combinados que atinjam tanto os eixos PI3K/AKT quanto MAPK/TGFβ no câncer colorretal.
Citação: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Palavras-chave: câncer colorretal, PTEN, microRNA, sinalização MAPK, TGF-beta