Clear Sky Science · pt
a supressão da autofagia impulsionada por mTOR define uma vulnerabilidade metabólica em câncer de mama HR+/HER2− resistente a inibidores de CDK4/6
Por que isso importa para pacientes com câncer de mama
Muitas mulheres com câncer de mama avançado vivem mais hoje graças a drogas chamadas inibidores de CDK4/6, que desaceleram a divisão das células tumorais. Infelizmente, a maioria dos tumores acaba encontrando maneiras de escapar desses medicamentos. Este estudo faz uma pergunta promissora: quando o câncer de mama se torna resistente aos fármacos CDK4/6, ele ganha uma nova fraqueza que os médicos poderiam explorar com medicamentos metabólicos já existentes e relativamente simples, como metformina ou dicloroacetato (DCA)?
Quando os fármacos que atuam no ciclo celular param de funcionar
Os médicos costumam tratar o tipo mais comum de câncer de mama — receptor hormonal positivo, HER2-negativo — com terapia hormonal combinada a inibidores de CDK4/6 como palbociclib ou ribociclib. Essas drogas atacam proteínas que empurram as células pelo ciclo de divisão. Com o tempo, porém, algumas células cancerosas se adaptam e tornam-se fortemente resistentes, continuando a crescer mesmo na presença de doses altas do medicamento. Os pesquisadores recriaram esse problema em laboratório expondo linhagens de câncer de mama (T47D e MCF7) a quantidades crescentes de inibidores de CDK4/6. Eles terminaram com dois tipos de sobreviventes: células parcialmente resistentes e um grupo menor de clones altamente resistentes que já não respondiam bem ao tratamento.
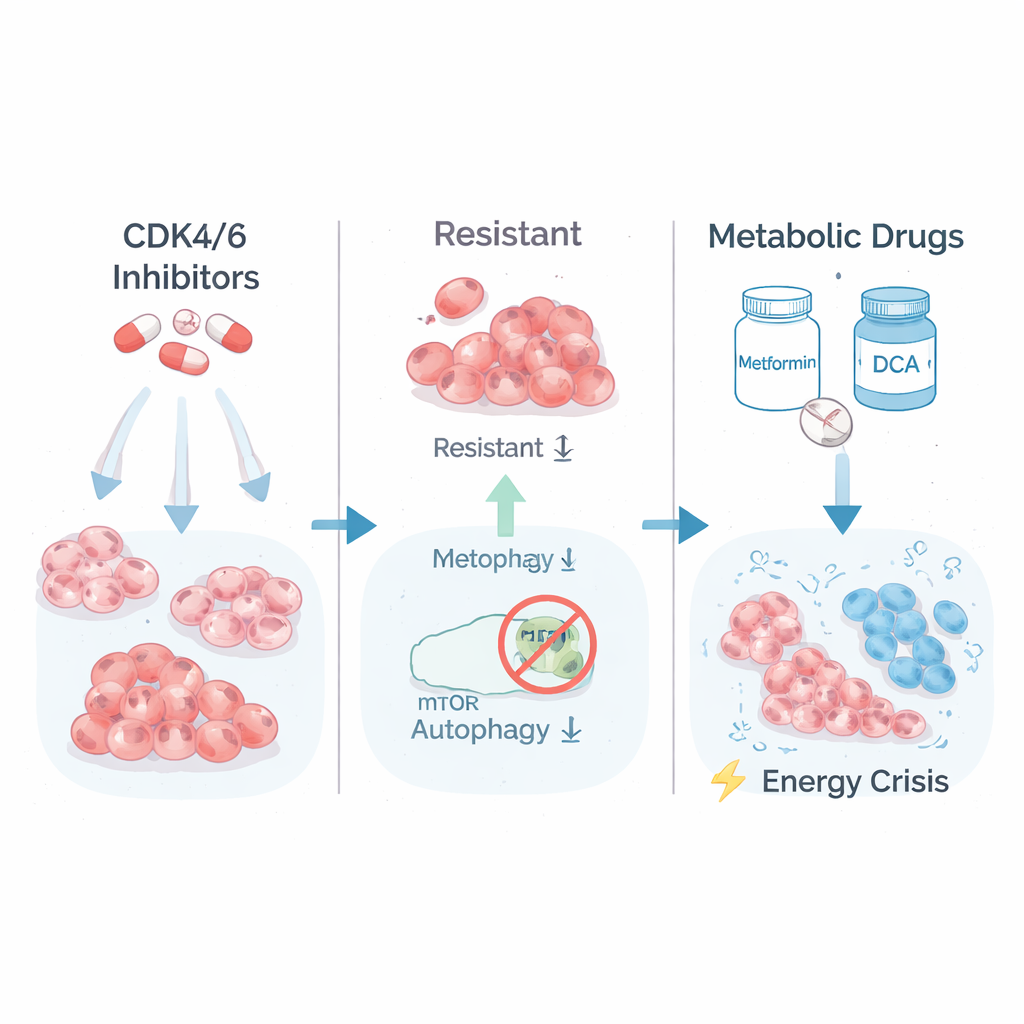
Uma fraqueza oculta no uso de energia do tumor
Para entender o que tornava as células altamente resistentes diferentes, a equipe examinou quais genes estavam ligados ou desligados. Eles descobriram que as células mais resistentes tinham vias relacionadas à queima de açúcar (glicólise) e ao sinal de crescimento controlado por um complexo proteico chamado mTORC1 aumentadas. Em outras palavras, essas células viviam em alta velocidade, consumindo combustível rapidamente para manter o crescimento. Os cientistas então testaram se esse metabolismo “em alta” poderia ser usado contra as células. Trataram células resistentes e parentais com metformina, um remédio comum para diabetes que estressa as usinas de energia da célula, e com DCA, que força as células a processarem o combustível de forma mais eficiente. Surpreendentemente, os clones mais resistentes aos medicamentos tornaram‑se os mais vulneráveis: seu crescimento de longo prazo em cultura colapsou com o tratamento metabólico, enquanto as células parentais e apenas parcialmente resistentes foram muito menos afetadas.
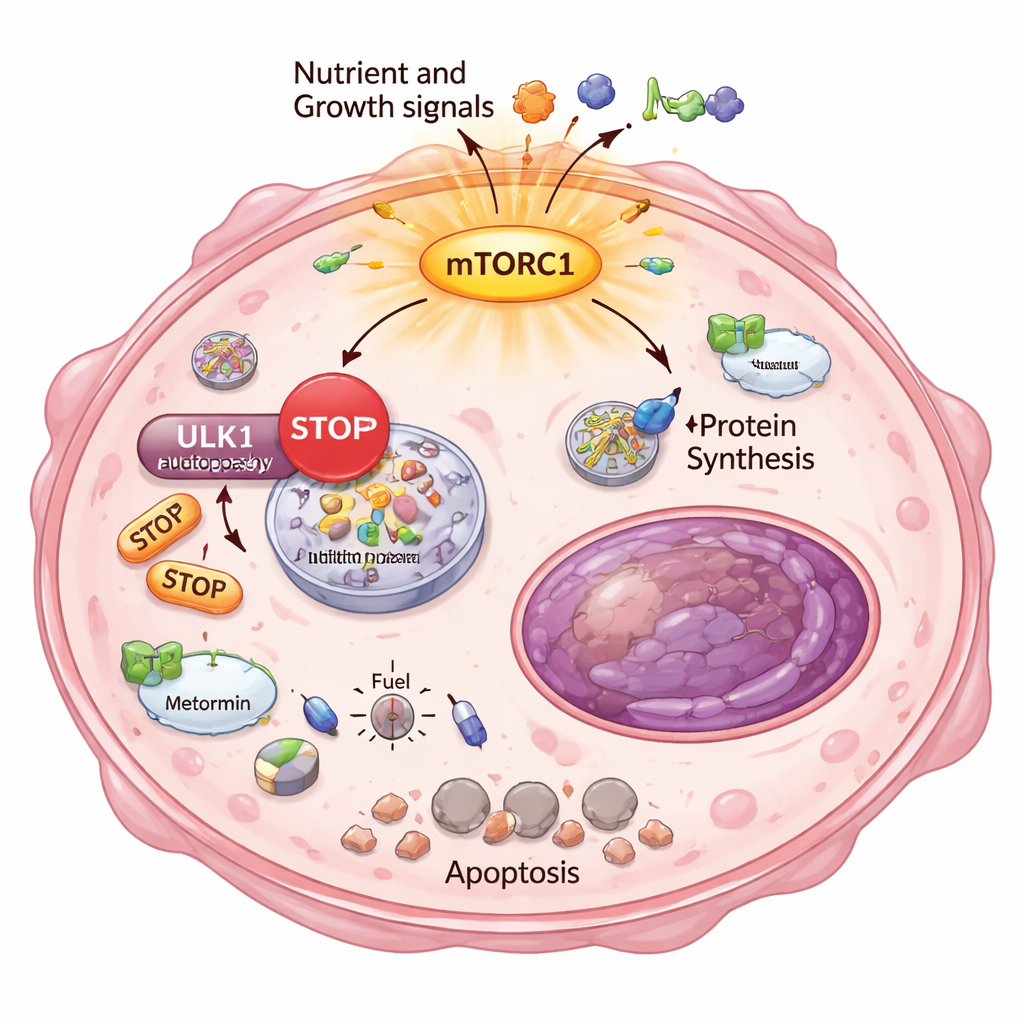
Autolimpeza bloqueada e um colapso energético
Por que essas células cancerosas escapistas seriam tão sensíveis ao estresse energético? A resposta residiu em outro processo básico de sobrevivência: autofagia, o sistema interno de “reciclagem e limpeza” da célula. Normalmente, quando a energia diminui, as células degradam e reutilizam seus próprios componentes para se manter vivas. Os pesquisadores mostraram que, nos clones altamente resistentes, o mTORC1 estava hiperativo e colocou um freio químico sobre ULK1, um iniciador chave da autofagia. Usando um ensaio sensível, demonstraram que essas células não conseguiam ativar ou aumentar a autofagia adequadamente, nem mesmo quando estimuladas por drogas metabólicas. Como resultado, metformina e DCA provocaram uma crise energética severa: sensores de baixa energia foram ativados, a produção de lipídios foi interrompida e apareceram marcadores de morte celular irreversível, especificamente nas células fortemente resistentes.
Evidências a partir de tumores reais de pacientes
Modelos de laboratório nem sempre refletem o que acontece nos pacientes, então a equipe recorreu a amostras humanas de tumor de mama. Eles coraram mais de cem cânceres para um marcador de atividade de mTORC1 (4E‑BP1 fosforilada) e para p62, uma proteína que se acumula quando a autofagia está bloqueada. Tumores com alta atividade de mTORC1 tenderam a ter mais p62, apoiando a ideia de que um padrão de “sinal de crescimento acelerado mais reciclagem comprometida” existe em cânceres de mama reais, não apenas em linhagens celulares. Isso sugere que um subconjunto de pacientes pode ter tumores com a mesma fraqueza metabólica observada no laboratório.
O que isso pode significar para tratamentos futuros
Para o público leigo, a mensagem-chave é que quando os cânceres de mama evoluem para escapar de potentes inibidores de CDK4/6, eles também podem se colocar em um beco metabólico. Ao ligar permanentemente sinais de crescimento e desligar a reciclagem celular, esses tumores tornam‑se fortemente dependentes de um suprimento constante de energia. O estudo mostra que essa configuração pode ser explorada com medicamentos metabólicos como metformina e DCA, já bem conhecidos em outras doenças. Importante, os autores propõem que testes simples em tecido para atividade de mTORC1 e marcadores de autofagia poderiam ajudar a identificar pacientes cujos tumores resistentes estão prontos para esse tipo de ataque metabólico, abrindo a porta para tratamentos de resgate mais personalizados após falha dos inibidores de CDK4/6.
Citação: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Palavras-chave: câncer de mama, resistência a inibidor de CDK4/6, mTOR, autofagia, terapia metabólica