Clear Sky Science · pt
Alternância de splicing do isoforma oncogênica BCS1L suprime a progressão do câncer de ovário ao perturbar a função mitocondrial
Usinas de energia dentro das células cancerosas
Cada célula do nosso corpo depende de pequenas usinas de energia chamadas mitocôndrias. Células cancerosas, que crescem e se espalham rapidamente, são especialmente famintas por energia. Este estudo revela como o câncer de ovário reconfigura um dos seus auxiliares mitocondriais chave e mostra que inverter delicadamente um “interruptor” molecular nesse auxiliar pode privar os tumores de energia enquanto poupa em grande parte os tecidos saudáveis.
Por que os tumores dependem de seus motores
As células do câncer de ovário, como muitos cânceres, conseguem explorar fontes de energia diferentes de forma flexível. Ao vasculhar grandes bancos de dados de pacientes e perfis de célula única, os pesquisadores descobriram que muitos tumores ovarianos operam suas mitocôndrias em um modo de alta potência conhecido como fosforilação oxidativa, ou OXPHOS. Tumores com essa atividade mitocondrial aumentada eram mais agressivos e mais comuns em doença avançada. Entre as muitas proteínas que constroem a maquinaria de energia mitocondrial, uma se destacou: BCS1L, uma chaperona que ajuda a montar o Complexo III, um hub central na linha de produção de energia da célula. Tumores com OXPHOS elevada e certos subtipos celulares tumorais mostraram atividade especialmente forte de BCS1L, sugerindo que as células cancerosas dependiam fortemente desse auxiliar para manter seus motores funcionando.
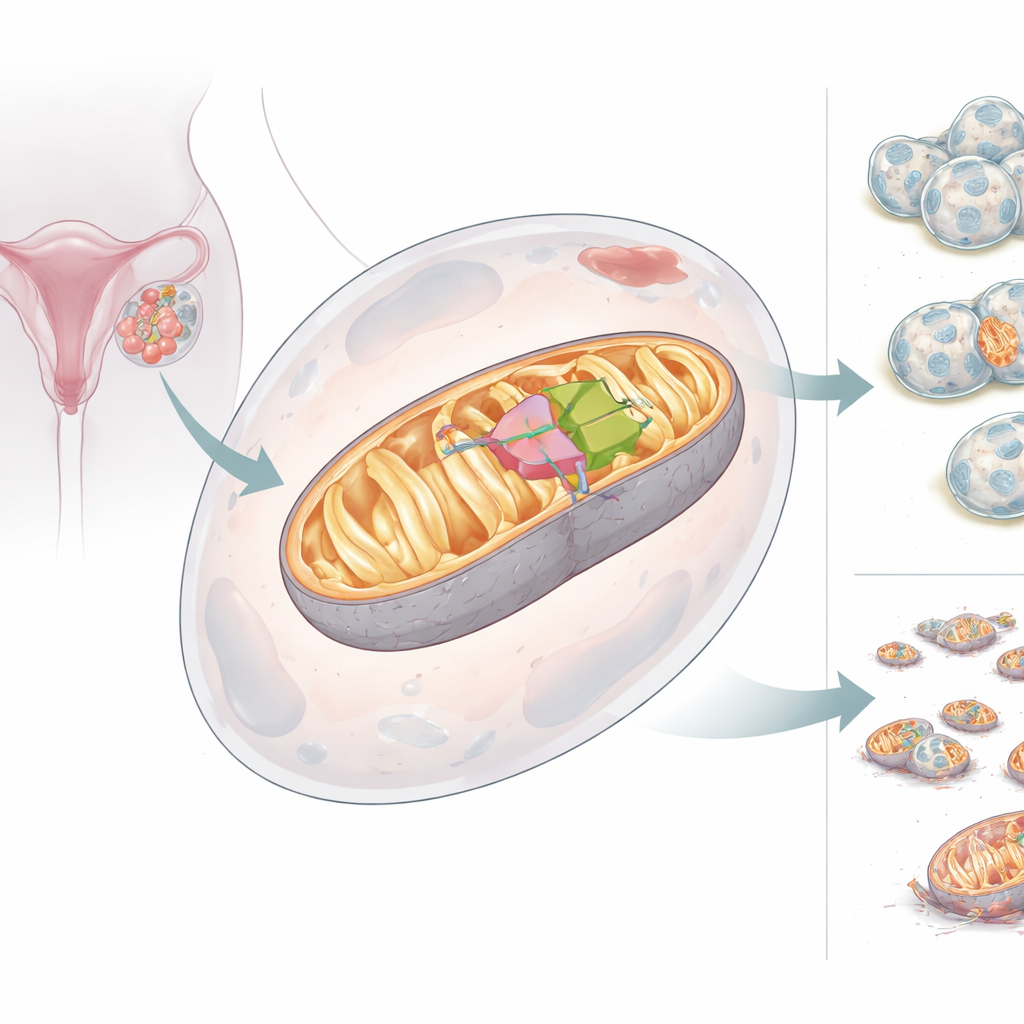
As duas faces de um auxiliar mitocondrial
A equipe descobriu que o gene BCS1L pode produzir duas versões, ou isoformas, de sua proteína. A forma de comprimento total, BCS1L-L, carrega uma etiqueta de endereço que a envia para as mitocôndrias, onde apoia a montagem adequada do Complexo III e alta produção de energia. A forma mais curta, BCS1L-S, carece de um segmento chave e não consegue alcançar as mitocôndrias; em vez disso, localiza-se no citosol e no núcleo e não sustenta a produção de energia. Em tecidos saudáveis, a versão curta é comum, mas nos cânceres de ovário o equilíbrio se inverte: a forma longa, ligada às mitocôndrias, domina. Quando as células foram forçadas a produzir mais BCS1L-L, suas mitocôndrias geraram mais energia, mantiveram maior potencial de membrana, produziram menos subprodutos oxigenados danosos e resistiram à morte celular. Quando BCS1L foi reduzida, as mitocôndrias fragmentaram, a produção de energia caiu, moléculas de oxigênio prejudiciais aumentaram e as células cancerosas ficaram mais suscetíveis à morte.
Como o câncer reprograma a mensagem
Produzir a versão longa ou curta de BCS1L depende de como a célula edita sua mensagem de RNA, um processo chamado splicing. Os pesquisadores buscaram proteínas que interagissem com o RNA de BCS1L e influenciassem essa escolha. Eles focaram em USP39, um fator de splicing já ligado a vários cânceres. Em células de câncer de ovário, USP39 se liga perto do segmento de RNA que se torna o exão 2 de BCS1L e incentiva sua inclusão, favorecendo assim a versão longa direcionada às mitocôndrias. Quando USP39 foi silenciado, as células saltaram esse segmento com mais frequência, deslocando-se para a forma curta BCS1L-S. Essa mudança enfraqueceu o Complexo III, reduziu a respiração mitocondrial e a produção de ATP, aumentou o estresse oxidativo e desencadeou a morte das células cancerosas. Restaurar BCS1L-L nessas células recuperou grande parte da função mitocondrial e da sobrevivência, mostrando que USP39 conduz um interruptor mitocondrial crítico em grande parte através de BCS1L.
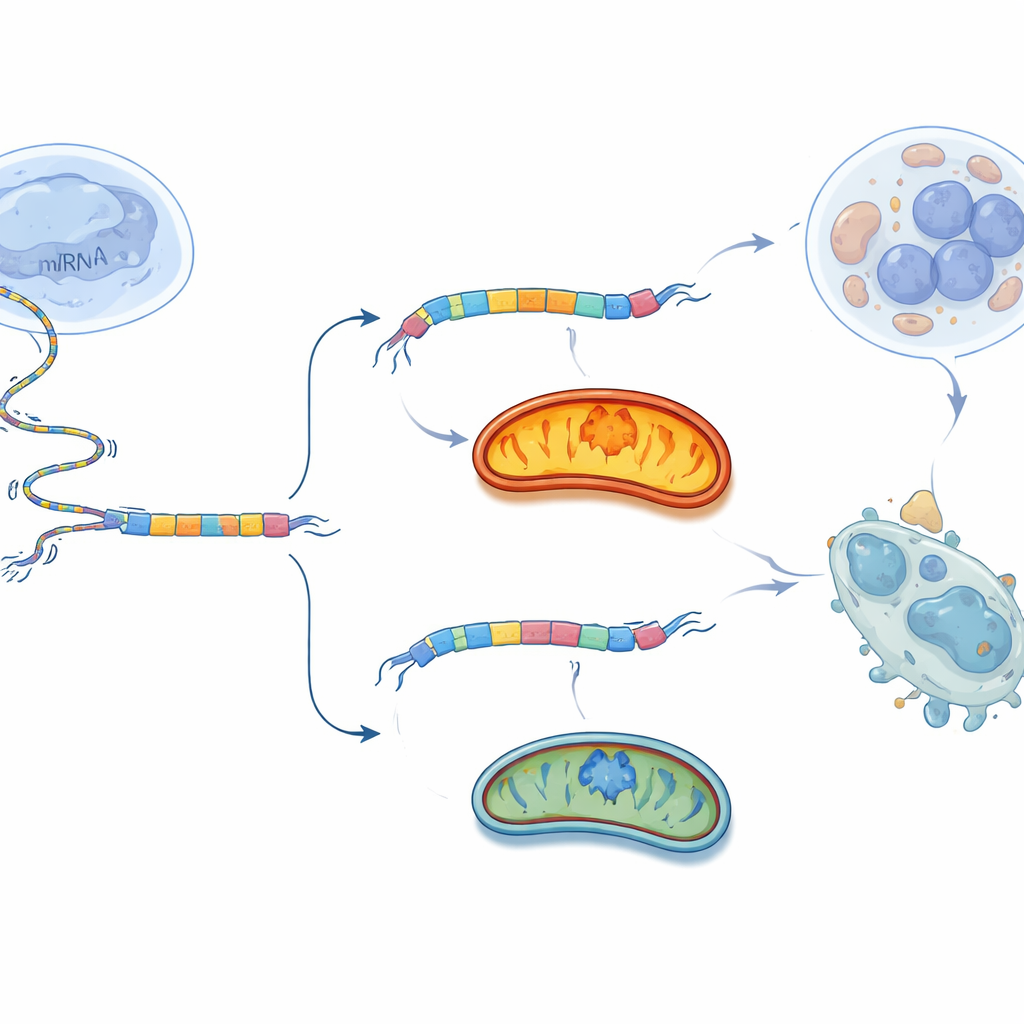
Virando o interruptor contra o tumor
Em vez de bloquear as mitocôndrias de forma ampla, o que poderia prejudicar muitos tecidos, a equipe testou uma tática mais cirúrgica: influenciar a escolha de splicing do próprio BCS1L. Eles projetaram pequenos trechos de material genético chamados oligonucleotídeos antissenso (ASOs) que se ligam exatamente ao redor do exão 2 do RNA de BCS1L. Esses ASOs atuam como pequenos pregadores, alterando como a maquinaria de splicing lê a mensagem e encorajando a célula a pular o exão 2. Em células de câncer de ovário cultivadas em placa, o melhor ASO reduziu fortemente a forma longa BCS1L-L e aumentou a forma curta BCS1L-S. Como resultado, a respiração mitocondrial e a produção de ATP caíram, os níveis de oxigênio prejudicial aumentaram e muitas mais células sofreram morte programada. Quando o mesmo ASO foi injetado em tumores de câncer de ovário em camundongos, o crescimento tumoral diminuiu e os tumores pesaram menos, com um efeito muito mais forte nas células cancerosas do que em fibroblastos normais.
O que isso pode significar para pacientes
De forma simples, este trabalho mostra que muitos cânceres de ovário dependem de uma versão “turbo” de uma proteína auxiliar mitocondrial para abastecer seu crescimento. Um fator de splicing, USP39, inclina a maquinaria de edição de RNA da célula para que mais dessa versão turbo seja produzida, mantendo as usinas de energia do tumor em ótimo estado. Usando ASOs projetados com precisão para reverter a escolha de splicing em direção à versão mais fraca, os pesquisadores podem incapacitar seletivamente as mitocôndrias das células cancerosas, desencadeando sua morte enquanto deixam a maioria das células normais menos afetadas. Embora a entrega desses fármacos ASO aos tumores permaneça um desafio importante, este estudo aponta o interruptor de splicing de BCS1L como uma alavanca promissora e altamente específica para tratar o câncer de ovário.
Citação: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Palavras-chave: câncer de ovário, mitocôndrias, splicing de RNA, BCS1L, oligonucleotídeos antissenso