Clear Sky Science · pt
PGC-1α protege contra MASH via inibição dependente de Tim23 da ferroptose mediada por DRP1
Por que isso importa para a saúde cotidiana
Muitas pessoas com obesidade ou diabetes tipo 2 desenvolvem silenciosamente um problema hepático sério chamado esteato-hepatite associada à disfunção metabólica (MASH). Nessa condição, os hepatócitos carregados de gordura ficam inflamados e começam a morrer, abrindo caminho para fibrose, cirrose e câncer de fígado. Este estudo revela um sistema silencioso de autoproteção dentro dos hepatócitos — centrado nas pequenas usinas chamadas mitocôndrias — que pode tanto proteger o fígado quanto, quando falha, acelerar a doença. Entender esse interruptor interno de segurança pode abrir portas para novos tratamentos contra uma das ameaças hepáticas mais comuns no mundo.
Um olhar mais atento sobre uma doença hepática silenciosa
A MASH se desenvolve quando um fígado gorduroso simples evolui para um estado mais perigoso, caracterizado por hepatócitos inchados e lesionados, inflamação e, eventualmente, tecido cicatricial. Os autores examinaram amostras de fígado de pacientes com MASH e de modelos murinos alimentados com dietas ricas em gordura, açúcares ou deficientes em nutrientes que imitam a condição humana. Eles se concentraram em um tipo específico de morte celular chamado ferroptose, no qual ferro e lipídios danificados se combinam para gerar moléculas tóxicas que perfuram as membranas celulares. Em pessoas e camundongos com MASH, as células hepáticas exibiram sinais dessa morte impulsionada por ferro e gordura: depósitos excessivos de ferro, mitocôndrias distorcidas e altos níveis de proteínas que promovem dano lipídico, junto com baixos níveis de proteínas que normalmente detoxificam subprodutos nocivos.
Evidências de que bloquear a morte celular dirigida por ferro ajuda
Para testar se a ferroptose é apenas um espectador ou um motor da doença, os pesquisadores trataram camundongos em dieta rica em gordura com ferrostatina-1, um composto que bloqueia especificamente a ferroptose. Camundongos que receberam o inibidor apresentaram menos acúmulo de gordura, menos sobrecarga de ferro e menos sinais de inflamação e fibrose no fígado. Exames de sangue mostraram função hepática melhor e saúde metabólica aprimorada, incluindo colesterol mais baixo e melhor sensibilidade à insulina. Em hepatócitos isolados de camundongo expostos ao ácido palmítico — uma gordura que imita a sobrecarga vista na MASH — o mesmo fármaco reduziu acúmulo lipídico, carga de ferro, dano oxidativo e sinais inflamatórios. Juntos, esses resultados indicam que a ferroptose é um motor importante de dano na MASH e que interromper esse processo pode atenuar substancialmente a doença.
O guardião interno do fígado nas mitocôndrias
A equipe então focou na PGC-1α, um regulador mestre que ajuda as mitocôndrias a produzir energia e lidar com estresse. Em fígados humanos com MASH, assim como em camundongos doentes e hepatócitos estressados, os níveis de PGC-1α estavam marcadamente mais baixos, enquanto uma proteína de fissão mitocondrial chamada DRP1 e uma enzima ativadora de lipídios chamada ACSL4 estavam aumentadas. Usando camundongos geneticamente modificados sem PGC-1α apenas nos hepatócitos, os autores constataram que a perda desse guardião tornou as dietas ricas em gordura muito mais prejudiciais: os fígados ficaram mais gordurosos, mais inflamados, com maior acúmulo de ferro e exibiram sinais mais fortes de ferroptose. No nível celular, a deficiência de PGC-1α aumentou a atividade de DRP1, elevou ACSL4 e proteínas importadoras de ferro, e enfraqueceu as defesas antioxidantes que normalmente mantêm a ferroptose sob controle.
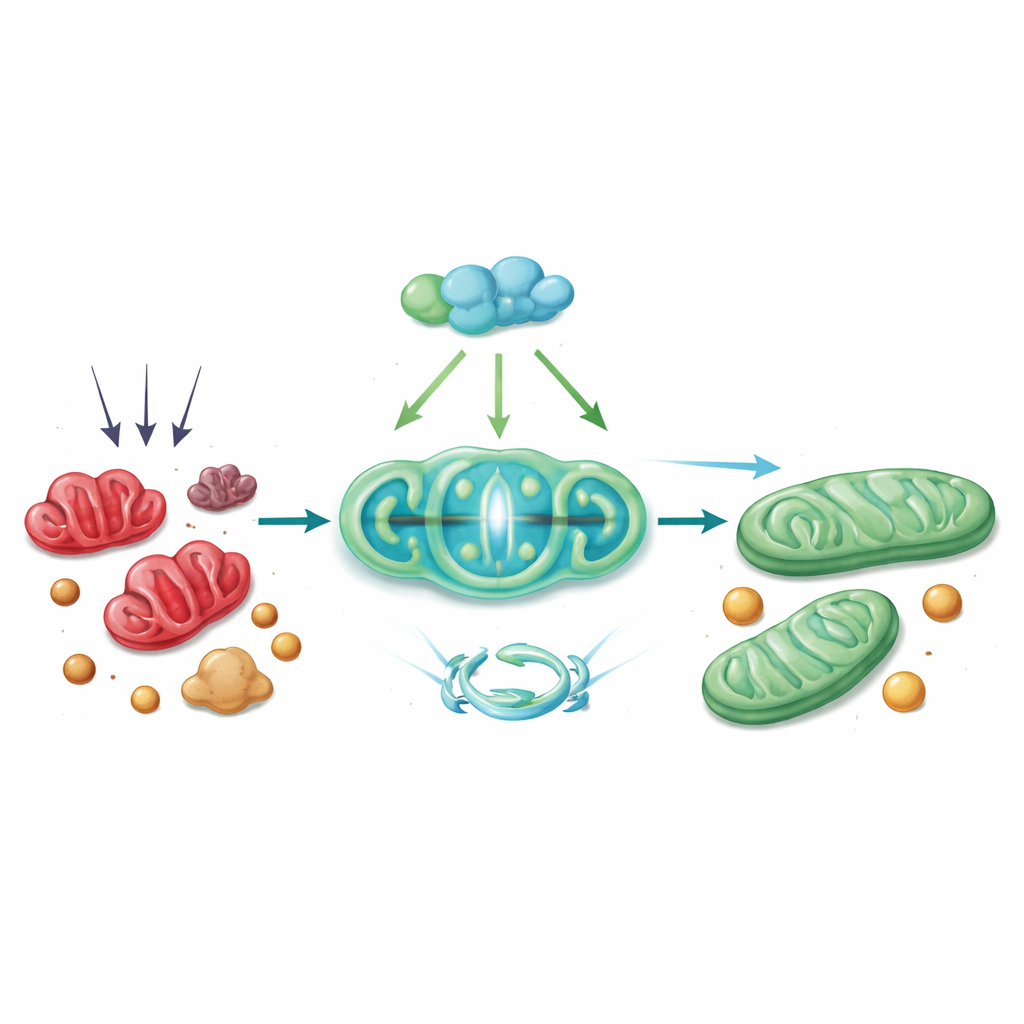
Uma reação em cadeia protetora dentro da célula
Mecanicamente, a PGC-1α atua por meio de uma cadeia de parceiros. Ela trabalha com um fator de transcrição chamado Nrf1 para aumentar a produção de Tim23, um canal na membrana mitocondrial interna essencial para a importação de proteínas e manutenção da estrutura saudável. Quando os níveis de Tim23 caem, o potencial de membrana mitocondrial se deteriora, o que desencadeia a fragmentação do órgão por DRP1. O estudo mostra que com Tim23 reduzido, o DRP1 fica mais ativo e mais propenso a se associar à ACSL4 na superfície mitocondrial, atraindo essa enzima modificadora de lipídios para dentro das mitocôndrias. Lá, a ACSL4 contribui para as alterações lipídicas que tornam as células vulneráveis à ferroptose. Restaurar a PGC-1α — seja em camundongos usando um vetor viral de transferência gênica ou em hepatócitos cultivados com um ativador baseado em CRISPR — reverteu muitas dessas etapas: Tim23 aumentou, a atividade de DRP1 e ACSL4 diminuiu, as mitocôndrias pareceram mais saudáveis e os marcadores de ferroptose e lesão hepática diminuíram.
Como essa descoberta pode orientar terapias futuras
Para um não especialista, a conclusão principal é que o fígado possui um freio interno contra a morte celular dirigida por ferro e lipídios, e que esse freio está incorporado nas mitocôndrias. A cadeia PGC-1α–Tim23–DRP1–ACSL4 funciona como um circuito de segurança: quando a PGC-1α é robusta, Tim23 mantém as mitocôndrias estáveis, DRP1 e ACSL4 ficam contidos e os hepatócitos têm menos propensão à autodestruição. Quando esse circuito falha, a ferroptose acelera e a MASH piora. Ao identificar essa via em tecido humano e em modelos animais, o estudo aponta duas estratégias complementares para tratamentos futuros — bloquear diretamente a ferroptose e aumentar a atividade de PGC-1α ou Tim23 para estabilizar as mitocôndrias — oferecendo esperança para intervenções mais precoces e eficazes antes que a fibrose hepática irreversível se instale.
Citação: Zhao, Y., Zhang, L., Li, B. et al. PGC-1α protects against MASH via Tim23-dependent inhibition of DRP1-mediated ferroptosis. Cell Death Dis 17, 246 (2026). https://doi.org/10.1038/s41419-026-08493-8
Palavras-chave: doença hepática gordurosa, mitocôndrias, morte celular, metabolismo do ferro, inflamação hepática