Clear Sky Science · pt
NSD2 inibe a expressão de PD-L1 via fosforilação oxidativa para controlar a vigilância imune no carcinoma hepatocelular
Por que esta história sobre câncer de fígado importa
O carcinoma hepatocelular, a forma mais comum de câncer de fígado, costuma ser diagnosticado tardiamente e resiste a muitos tratamentos. Drogas de imunoterapia que bloqueiam a “capa de invisibilidade” PD-L1 nas células tumorais ajudam alguns pacientes, mas não a maioria. Este estudo revela um ator inesperado, uma proteína chamada NSD2, que conecta a forma como as células de câncer de fígado produzem energia à sua visibilidade para o sistema imune. Entender essa ligação pode apontar para novas maneiras de potencializar terapias atuais e identificar quais pacientes têm maior probabilidade de se beneficiar.
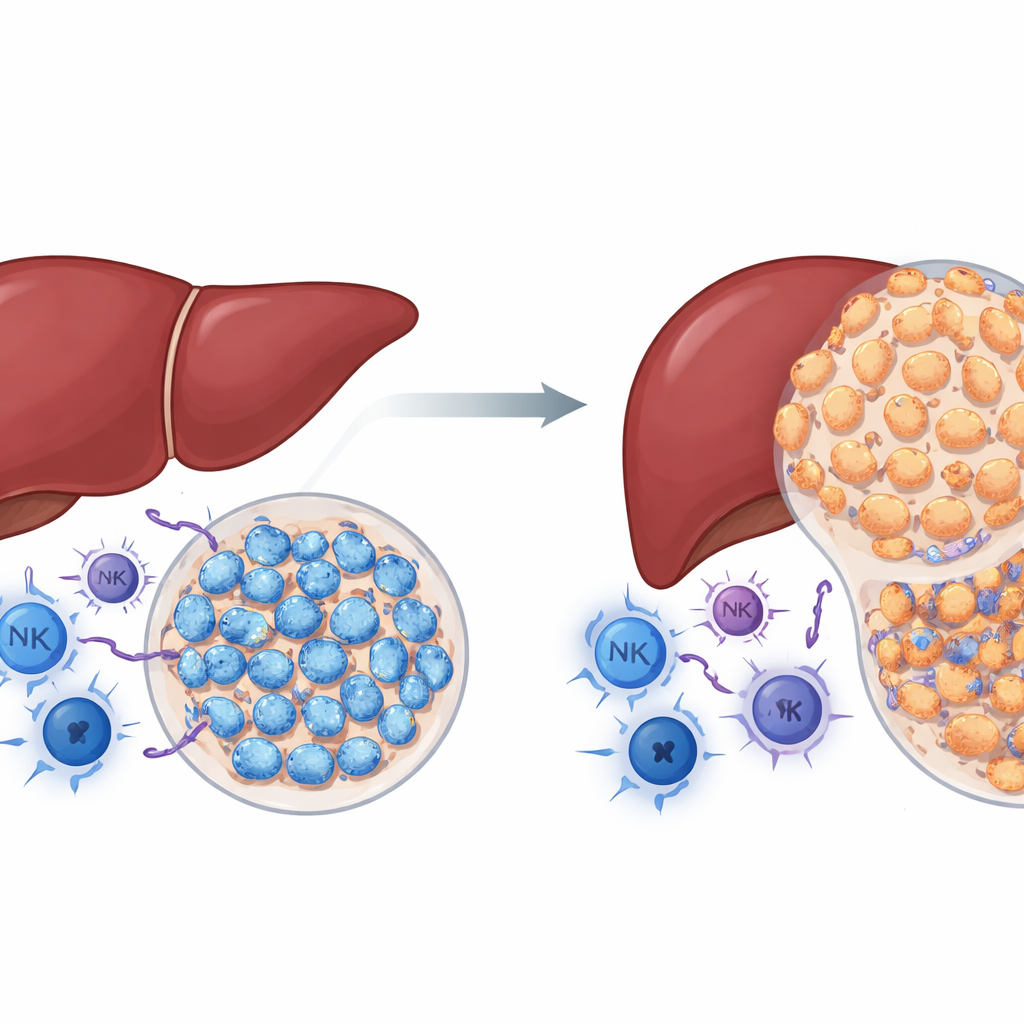
Um papel surpreendente para uma proteína cancerígena conhecida
NSD2 é uma enzima que modifica histonas, as proteínas em torno das quais o DNA se enrola. Em muitos cânceres, NSD2 tem sido vista como um motor do crescimento tumoral. Os autores perguntaram se o mesmo vale para o câncer de fígado. Usando camundongos geneticamente modificados nos quais NSD2 é ativada especificamente nas células do fígado, eles trataram os animais com um químico que induz de forma confiável tumores hepáticos. Contrariando as expectativas, camundongos com excesso de NSD2 desenvolveram muito menos tumores e menores do que os camundongos normais, e seus fígados mostraram menos dano, fibrose e proliferação celular. Ao mesmo tempo, os tumores de fígados com superexpressão de NSD2 continham mais células imunes antitumorais, incluindo células T auxiliares e citotóxicas e células natural killer. Esses achados sugerem que, na presença de um sistema imune intacto, NSD2 se comporta menos como um acelerador e mais como um freio ao câncer de fígado.
Fábricas de energia e uso de combustível nas células tumorais
Para entender como NSD2 restringe os tumores, a equipe perfilou a atividade gênica no tecido hepático. Eles descobriram que a superexpressão de NSD2 suprimia fortemente genes envolvidos na fosforilação oxidativa, o processo pelo qual as mitocôndrias — as “usinas” da célula — geram energia usando oxigênio. Experimentos complementares em linhagens de câncer de fígado de camundongo e humano mostraram que aumentar NSD2 reduziu a expressão de muitos genes de fosforilação oxidativa, diminuiu o consumo de oxigênio e a produção de ATP, e reduziu o potencial de membrana mitocondrial, um sinal de atividade mitocondrial enfraquecida. Ao mesmo tempo, essas células consumiram menos glicose, mas não migraram sua dependência para a glicólise, indicando uma redução líquida na produção de energia. A perda de NSD2 teve efeitos opostos, fortalecendo a potência mitocondrial e o uso de combustível.
Como NSD2 reorganiza energia e visibilidade imune
Investigando mais a fundo, os pesquisadores combinaram mapeamento genômico da cromatina com dados de expressão gênica e identificaram um conjunto de genes diretamente ativados quando NSD2 está presente. Dois desses, Camk2d e Prkce, são conhecidos por restringir a atividade mitocondrial. NSD2 aumentou uma marca histona específica (H3K36me2) em seus promotores, elevando sua expressão. Reintroduzir esses genes em células de câncer de fígado deficientes em NSD2 reduziu o uso de oxigênio mitocondrial e a produção de ATP, confirmando que atuam como freios downstream da NSD2 sobre a fosforilação oxidativa. Importante, trabalhos anteriores sugeriram que mitocôndrias altamente ativas favorecem altos níveis de PD-L1 nas células tumorais. Coerente com isso, os autores observaram que a superexpressão de NSD2 reduziu os níveis de PD-L1, enquanto a perda de NSD2 aumentou o PD-L1 em células de câncer de fígado e em tecido tumoral.
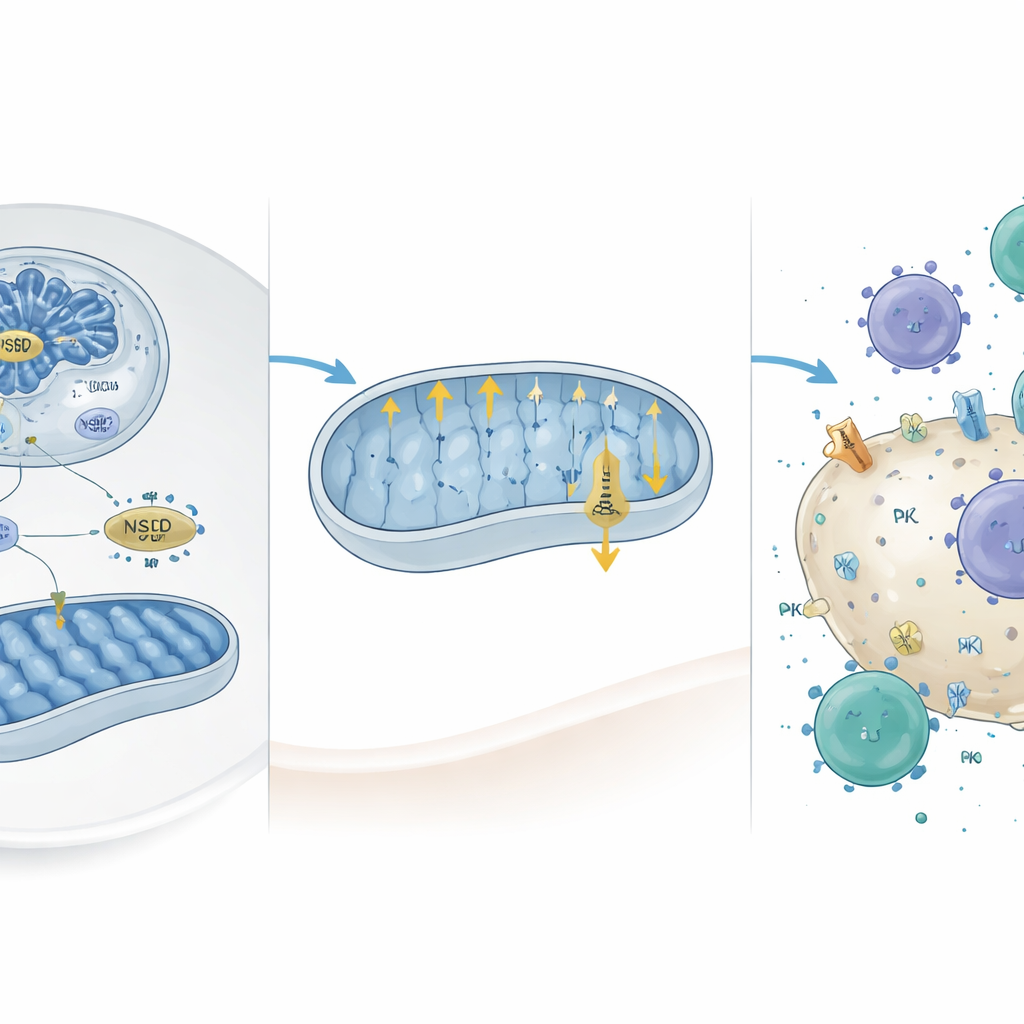
Baixando o escudo e despertando o ataque imune
O impacto funcional dessas mudanças moleculares foi testado em camundongos que receberam injeções hepáticas de células cancerígenas geneticamente programadas para ganhar ou perder NSD2. Células sem NSD2 formaram rapidamente tumores maiores, expressaram mais PD-L1 e foram infiltradas por menos células T e células natural killer, especialmente células T citotóxicas ativadas. Quando os pesquisadores bloquearam quimicamente o complexo V mitocondrial, um componente-chave da fosforilação oxidativa, os níveis de PD-L1 em células deficientes em NSD2 caíram novamente em direção ao normal e as células imunes foram mais capazes de induzir a morte das células tumorais. De maneira semelhante, superexpressar Camk2d ou Prkce em células sem NSD2, ou tratar tumores com um anticorpo bloqueador de PD-L1, reduziu o tamanho tumoral e restaurou a infiltração de células imunes. Em conjuntos de dados de pacientes, baixa expressão de NSD2 esteve associada a pior sobrevida, mas, intrigantemente, a uma melhor resposta à terapia dirigida a PD-L1, sugerindo que o status de NSD2 pode ajudar a prever quem se beneficia desses medicamentos.
O que isso significa para o futuro do tratamento do câncer de fígado
Para um leitor geral, a mensagem-chave é que este estudo redefine NSD2 como um fator supressor tumoral no câncer de fígado, ao menos na presença de um sistema imunológico funcional. Ao reduzir a produção de energia baseada em oxigênio da célula, NSD2 diminui indiretamente o PD-L1 nas células tumorais, removendo parte de sua capa de invisibilidade e permitindo que as células imunes as reconheçam e ataquem. Essa cadeia recém-descrita NSD2–energia–PD-L1 sugere duas ideias práticas: primeiro, pacientes cujos tumores não expressam NSD2 podem ser candidatos especialmente adequados para drogas bloqueadoras de PD-L1; e segundo, combinar drogas que inibem a produção mitocondrial de energia com imunoterapia pode oferecer um golpe duplo poderoso contra o câncer de fígado.
Citação: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Palavras-chave: carcinoma hepatocelular, NSD2, fosforilação oxidativa, PD-L1, imunoterapia tumoral