Clear Sky Science · pt
Regulação do empalme de DDX39B mediada por SNRPD2 promove a progressão do câncer endometrial ao suprimir a ativação de éxons crípticos de CTSC
Por que mensagens ocultas em genes do câncer importam
O câncer endometrial, um tumor comum do útero, está aumentando no mundo todo, e ainda existem poucas opções eficazes para muitos pacientes com doença avançada. Este estudo revela como um processo sutil dentro das células — a forma como elas recortam e colam mensagens genéticas — pode impulsionar o crescimento e a disseminação de tumores endometriais. Ao expor um “diagrama de fiação” frágil do qual as células cancerosas dependem, o trabalho aponta para novas maneiras de desligar tumores usando medicamentos genéticos de precisão.
Um câncer em crescimento que precisa de novas respostas
O câncer endometrial é agora o câncer ginecológico mais frequente em muitos países ocidentais, com casos e mortes aumentando de forma constante tanto no Ocidente quanto na China. Cirurgia, radiação, quimioterapia, tratamento hormonal e imunoterapia são usados, mas estão longe de ser perfeitos. A remoção do útero acaba com a fertilidade, tratamentos hormonais frequentemente falham, e tumores agressivos costumam reaparecer. Esses desafios têm levado os pesquisadores a investigar mais a fundo dentro das células cancerosas por pontos fracos moleculares que possam ser alvo de terapias mais precisas.
As máquinas de empalme da célula como um elo fraco
Para funcionar, nossos genes são primeiro copiados em longas moléculas de RNA que precisam ser aparadas e costuradas em um processo chamado empalme. Máquinas proteicas especializadas chamadas spliceossomos decidem quais trechos são mantidos e quais são descartados, editando na prática o roteiro que a célula usa para produzir proteínas. A equipe focou em um componente do spliceossomo chamado SNRPD2, parte de uma família de proteínas “Sm” que ajudam a montar o maquinário de empalme. Ao explorar grandes bancos de dados de genes e proteínas do câncer e examinar amostras de pacientes, eles descobriram que os níveis de SNRPD2 são notavelmente mais altos em tumores endometriais do que no revestimento uterino normal, e que pacientes cujos tumores têm mais SNRPD2 tendem a ter desfechos piores.
Desligar um editor mestre desacelera os tumores
Para testar se o SNRPD2 é apenas um observador ou um motor ativo, os pesquisadores reduziram sua expressão em linhagens de células de câncer endometrial cultivadas em laboratório. Quando o SNRPD2 foi silenciado, as células se dividiram mais lentamente, formaram menos colônias e tiveram menor capacidade de migrar e invadir através de membranas — comportamentos ligados à metástase. Quando essas células alteradas foram implantadas em camundongos, os tumores resultantes foram muito menores e apresentaram menos células em divisão ativa. Importante, a equipe projetou oligonucleotídeos antissenso — pequenos trechos sintéticos de DNA com caráter farmacológico — que miram especificamente o RNA de SNRPD2. Em um modelo de xenotransplante derivado de paciente, no qual fragmentos tumorais humanos crescem em camundongos com imunidade comprometida, esses fármacos antissenso reduziram fortemente os níveis de SNRPD2 e o tamanho dos tumores, sugerindo que SNRPD2 pode ser alvo de drogas de maneira clinicamente relevante.
Uma cadeia em três passos do erro de empalme ao crescimento do câncer
Aprofundando-se nos dados genéticos, os investigadores perguntaram como a perda de SNRPD2 reconfigura as mensagens de RNA pelo genoma. Eles descobriram que, quando o SNRPD2 é reduzido, uma enzima chave no processamento de RNA chamada DDX39B começa a falhar. Normalmente, DDX39B ajuda a remover um intron específico — um segmento de RNA que deve ser cortado — da sua própria mensagem. Sem SNRPD2 suficiente, esse intron permanece, criando uma versão defeituosa do RNA de DDX39B que a célula rapidamente elimina. A queda de DDX39B então tem um efeito cascata sobre outro gene, CTSC, que codifica uma enzima proteolítica conhecida por apoiar o crescimento e a disseminação tumoral. Em condições saudáveis, um éxon “críptico” oculto dentro do RNA de CTSC é ignorado, permitindo que as células produzam a proteína CTSC em tamanho completo e ativa. Com DDX39B reduzido, esse éxon críptico é incluído por engano, inserindo sinais de parada prematuros no RNA. A mensagem malformada de CTSC é degradada antes de produzir muita proteína, e as células cancerosas perdem parte de sua agressividade.
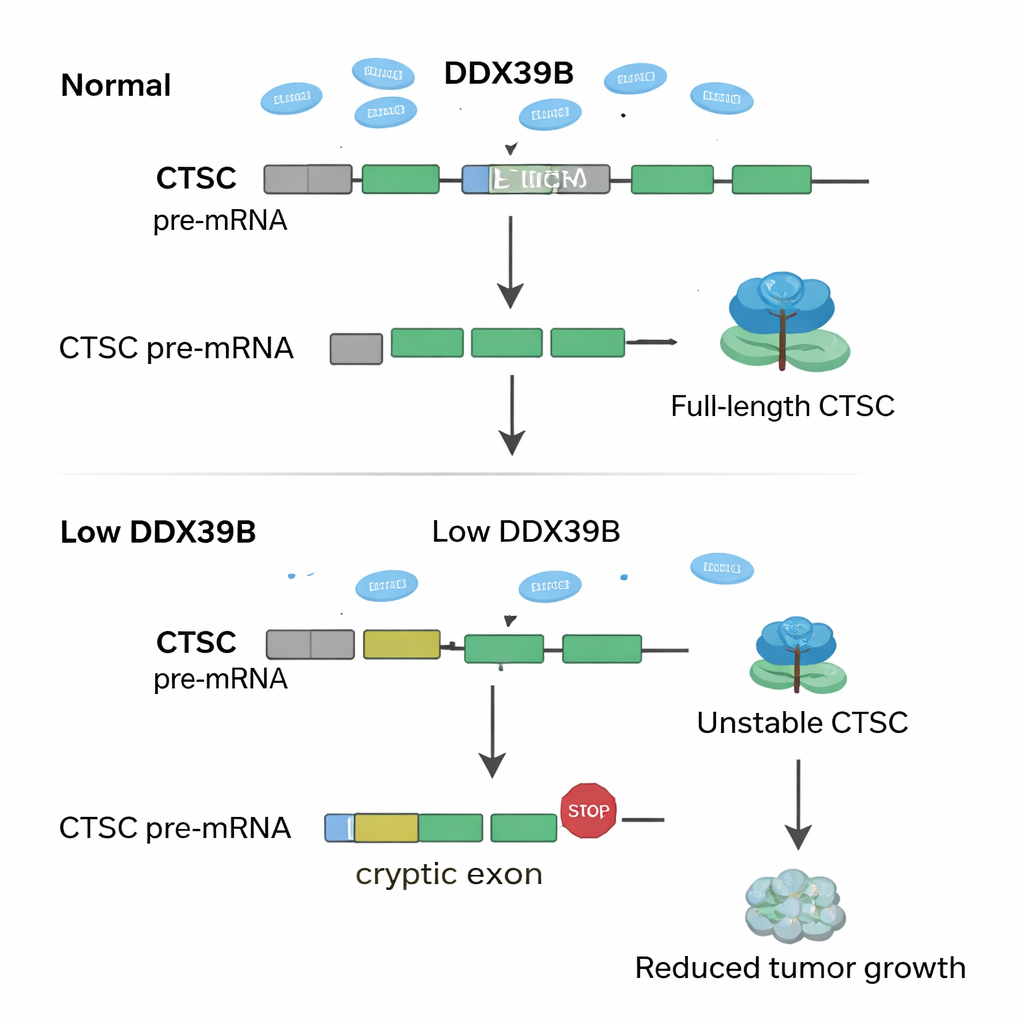
O que isso significa para tratamentos futuros
Em termos simples, os autores revelam um sistema em cascata — SNRPD2 → DDX39B → CTSC — que células do câncer endometrial exploram para prosperar. Níveis altos de SNRPD2 mantêm DDX39B abundante; DDX39B, por sua vez, impede que CTSC use éxons crípticos deletérios, preservando a proteína CTSC em sua força total, que ajuda os tumores a crescer e a se espalhar. Quando SNRPD2 é bloqueado, essa cadeia desaba, os níveis de CTSC caem e os tumores enfraquecem. Para não especialistas, a ideia-chave é que células cancerosas dependem de uma edição de RNA muito precisa, e até mesmo pequenos “erros” forçados podem envenenar seletivamente seu crescimento. Mirar SNRPD2 com drogas antissenso, ou forçar diretamente o uso de éxons crípticos em CTSC, pode oferecer novas terapias mais direcionadas para pacientes com câncer endometrial.
Citação: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Palavras-chave: câncer endometrial, emparelhamento de RNA, SNRPD2, DDX39B, CTSC