Clear Sky Science · pt
DNMT2 inibe a progressão do câncer de tireoide anaplásico ao reduzir a produção de 5’tiRNAGly-GCC
Por que essa química oculta do RNA importa
O câncer de tireoide anaplásico está entre os cânceres humanos mais letais, frequentemente levando os pacientes à morte em poucos meses apesar de cirurgia, radiação e quimioterapia. Este estudo revela um culpado inesperado no interior das células cancerosas: pequenas marcas químicas em RNA de transferência, as moléculas que ajudam a construir proteínas. Os autores mostram que quando uma enzima específica, DNMT2, é perdida ou reduzida, os tumores da tireoide crescem mais rápido, se espalham com maior facilidade e resistem ao medicamento quimioterápico comum doxorrubicina. Ainda mais intrigante, eles identificam um pequeno fragmento de RNA que aparece quando o DNMT2 está baixo e demonstram que bloquear esse fragmento pode virar uma nova estratégia terapêutica.
Uma enzima protetora que desaparece
Os RNAs de transferência (tRNAs) normalmente transportam aminoácidos até a máquina celular de síntese de proteínas, e sua estabilidade depende de delicadas decorações químicas. DNMT2 é uma enzima que adiciona uma dessas marcas, chamada grupo metil, em posições específicas do tRNA. Em muitos cânceres, o DNMT2 está elevado e se acredita que favoreça os tumores, mas aqui a história é invertida. Ao analisar grandes conjuntos de dados de pacientes e amostras tumorais, os pesquisadores descobriram que os níveis de DNMT2 são significativamente mais baixos no tecido de câncer de tireoide anaplásico do que na tireoide normal. Pacientes cujos tumores apresentavam mais DNMT2 tenderam a viver mais tempo sem piora da doença, sugerindo que o DNMT2 age mais como um freio do que como um acelerador nessa condição.
Como o baixo DNMT2 alimenta comportamento agressivo
Para saber o que o DNMT2 faz nas células cancerosas, a equipe manipulou seus níveis em linhagens celulares de câncer de tireoide anaplásico cultivadas em placas e em modelos de camundongos. Quando o DNMT2 foi reduzido, as células multiplicaram-se mais rápido, invadiram membranas com maior facilidade e formaram mais colônias — todos sinais de um tumor agressivo. Essas células também ficaram menos sensíveis à doxorrubicina, um fármaco padrão para esse câncer. Em camundongos, tumores geneticamente projetados para ter menos DNMT2 cresceram mais e se espalharam para os pulmões com maior frequência, enquanto aumentar a expressão de DNMT2 teve o efeito oposto. Os pesquisadores atribuíram parte dessas mudanças à ativação de um programa celular conhecido como transição epitélio–mesênquima, que torna as células cancerosas mais móveis e invasivas.
Do tRNA danificado a fragmentos pequenos e nocivos
Avançando na investigação, o estudo mostra que o DNMT2 coloca uma marca metil em uma posição específica (chamada C38) em apenas três tipos de tRNA. Sem essa proteção, os tRNAs ficam mais vulneráveis ao corte por outra enzima, a angiogenina. Esse corte produz um pequeno fragmento de RNA derivado do tRNA-Gly-GCC, denominado 5’tiRNAGly-GCC. Por sequenciamento e testes bioquímicos, os autores descobriram que quando o DNMT2 está baixo, esse fragmento se acumula, especialmente a partir do tRNA transportador de glicina. Em experimentos in vitro, adicionar a marca metil protegeu fortemente o tRNA contra a clivagem, confirmando que o DNMT2 normalmente resguarda essas moléculas de serem fragmentadas em pedaços menores e potencialmente danosos.
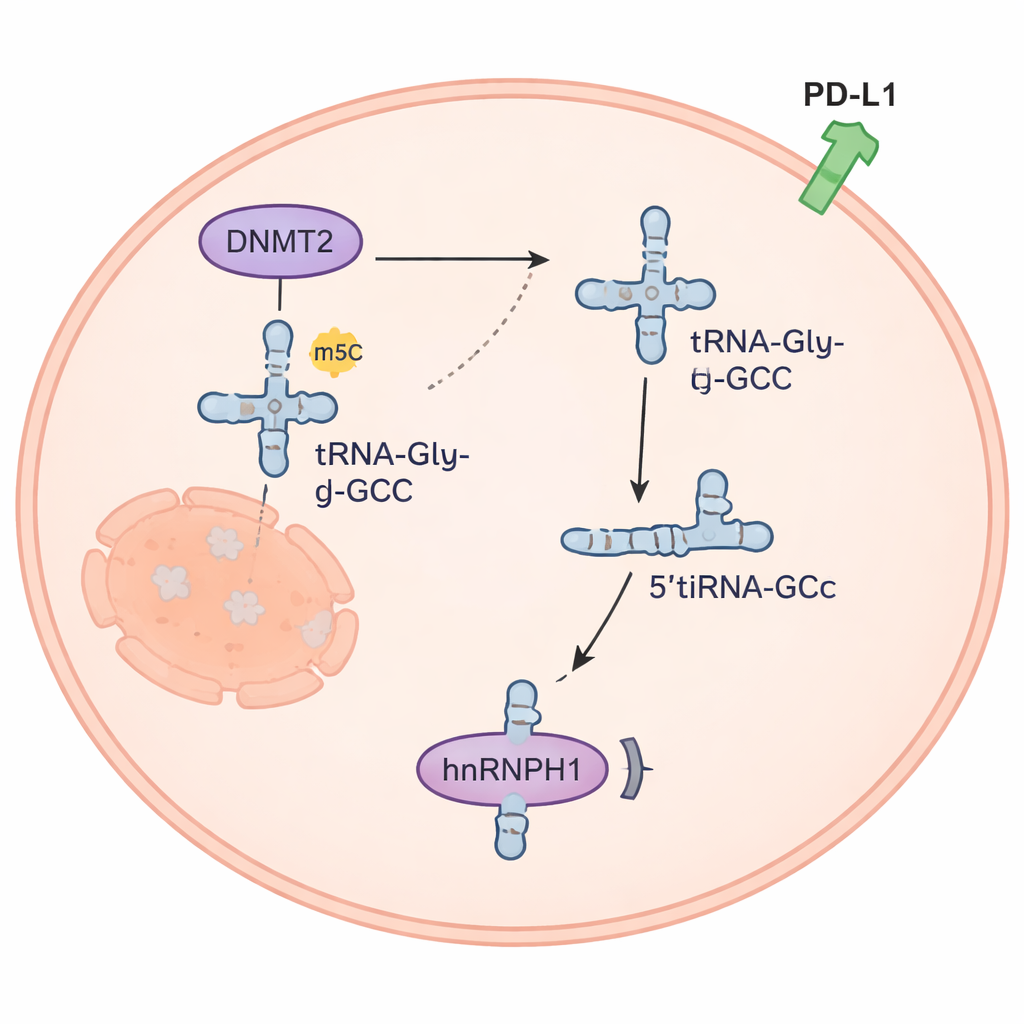
Um pequeno fragmento de RNA redesenha sinais do câncer
O fragmento 5’tiRNAGly-GCC mostrou-se mais do que detrito molecular. Ele era abundante em células de câncer de tireoide anaplásico, mas raro em células de tireoide normais. Quando os pesquisadores elevaram artificialmente seus níveis, as células cancerosas proliferaram mais rápido, invadiram mais e ficaram mais resistentes à doxorrubicina; reduzir o fragmento teve o efeito contrário. Em camundongos, um inibidor quimicamente concebido para 5’tiRNAGly-GCC desacelerou o crescimento tumoral, e combinar esse inibidor com doxorrubicina funcionou ainda melhor do que cada tratamento isoladamente. A equipe descobriu que 5’tiRNAGly-GCC se liga a uma proteína chamada hnRNPH1, reduzindo sua quantidade dentro das células. Como hnRNPH1 normalmente ajuda a manter os níveis da proteína relacionada ao sistema imune PD-L1 sob controle, a perda de hnRNPH1 permite que PD-L1 aumente — uma alteração que pode ajudar os tumores a escapar do ataque imune e está associada ao acúmulo de células T regulatórias ao redor dos tumores.
O que isso significa para tratamentos futuros
De forma simples, o estudo revela uma reação em cadeia: quando o DNMT2 está baixo, certos tRNAs perdem uma marca protetora, são cortados em pequenos fragmentos, e um desses fragmentos (5’tiRNAGly-GCC) desativa uma proteína que restringe o PD-L1. O resultado é um câncer mais agressivo, resistente a drogas e capaz de evadir o sistema imune. Em vez de tentar aumentar o DNMT2 diretamente — o que poderia ser arriscado em outros tecidos — os autores sugerem mirar no próprio fragmento de RNA nocivo. Os experimentos em camundongos com um inibidor de 5’tiRNAGly-GCC, especialmente quando combinado com doxorrubicina, fornecem uma prova inicial de que interromper essa pequena circuitaria de RNA pode ajudar a conter uma das formas mais letais de câncer de tireoide.
Citação: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Palavras-chave: câncer de tireoide anaplásico, DNMT2, fragmentos de tRNA, quimiorresistência, PD-L1