Clear Sky Science · pt
Revelando ZNF124 como um novo determinante na neurodegeneração: orquestração da homeostase dos fotorreceptores via regulação transcripcional de MSX2
Por que essa descoberta importa para a visão
A retinose pigmentar é uma das principais causas de cegueira hereditária, mas em quase 40% dos pacientes os médicos ainda não conseguem identificar o gene defeituoso. Este estudo revela um novo componente genético, chamado ZNF124, que ajuda a manter as células sensíveis à luz do olho vivas. Ao mostrar como uma mutação nesse gene interrompe uma cadeia de “interruptores” moleculares na retina, os pesquisadores abrem novos caminhos para diagnóstico e, potencialmente, tratamentos direcionados para pessoas com perda visual.
Uma causa oculta de perda de visão hereditária
Os pesquisadores estudaram uma família extensa na qual várias crianças desenvolveram sinais clássicos de retinose pigmentar: cegueira noturna precoce, redução do campo visual periférico e perda gradual da visão central. Exames oftalmológicos detalhados revelaram afinamento da retina e respostas elétricas fracas à luz, ambos indicativos de dano aos fotorreceptores bastonetes e cones. Ainda assim, nenhum dos mais de 80 genes conhecidos associados à retinose pigmentar apresentava defeitos óbvios nesses pacientes, sugerindo que um gene ainda não identificado poderia ser responsável pela doença.
Encontrando um interruptor genético defeituoso
Usando sequenciamento do exoma completo, que lê as partes codificadoras de proteínas do DNA, a equipe identificou uma mutação rara e previamente não relatada no gene ZNF124. Essa mutação altera a forma como o RNA do gene é emparelhado, deletando algumas bases em uma junção crítica. Como resultado, a proteína ZNF124 fica encurtada e perde sua região do tipo dedo de zinco, uma estrutura normalmente usada para reconhecer e se ligar a sequências específicas de DNA. Como proteínas com dedo de zinco frequentemente atuam como interruptores mestres que ligam ou desligam muitos outros genes, um ZNF124 danificado pode ter efeitos amplos nas células da retina.
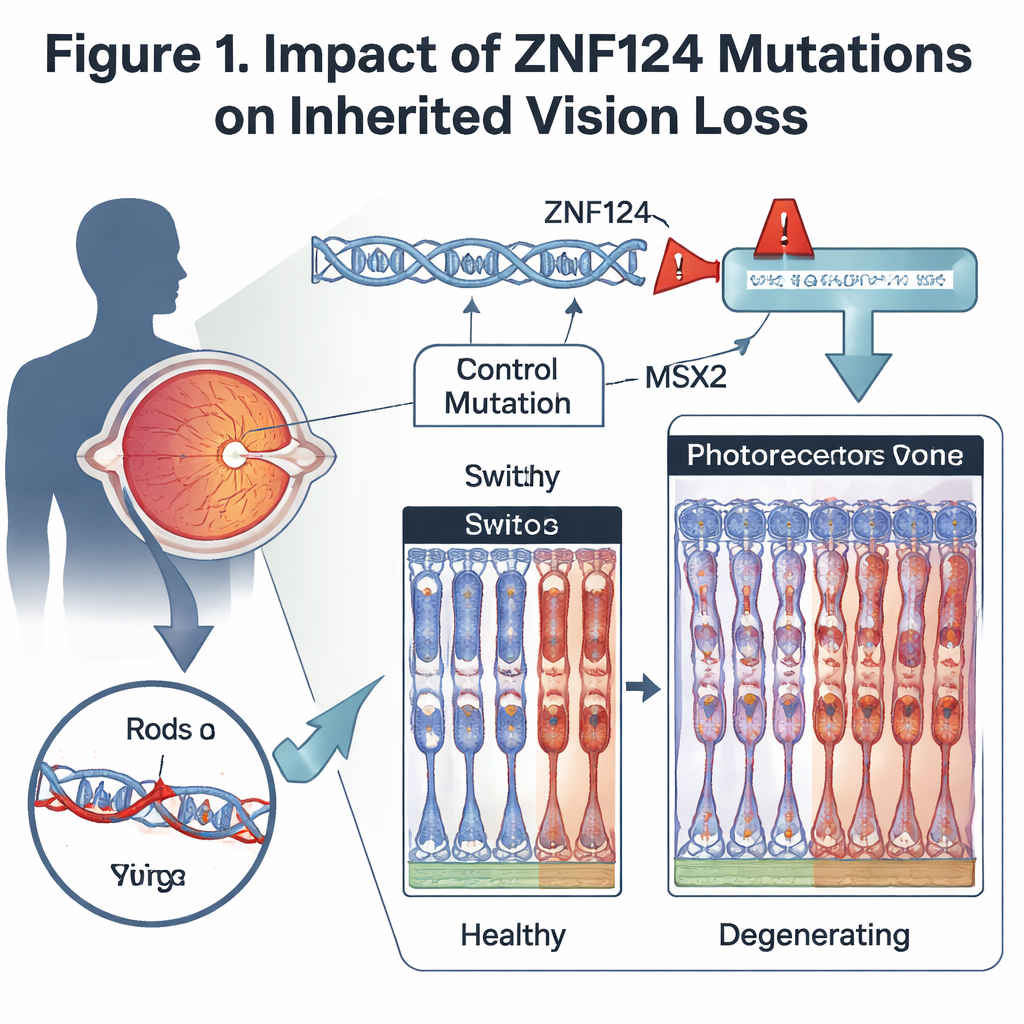
Testando o gene em modelos animais
Para entender como a perda desse interruptor afeta o olho, os cientistas criaram camundongos sem Gm20541, o equivalente mais próximo de ZNF124 em camundongos, especificamente na retina. Esses animais desenvolveram problemas visuais dependentes da idade: suas respostas elétricas à luz fraca e intensa enfraqueceram, e a análise microscópica mostrou afinamento progressivo da camada retiniana que contém os fotorreceptores. Tanto os bastonetes, que sustentam a visão noturna, quanto os cones, que sustentam a visão diurna e a percepção de cores, apresentaram segmentos externos encurtados e perda de proteínas visuais essenciais. Outras células retinianas, como certos tipos de células bipolares, também foram reduzidas, e células de suporte foram ativadas, uma resposta comum a lesões retinianas crônicas.
Descobrindo a via de controle ZNF124–MSX2
A próxima questão foi quais genes o ZNF124 normalmente controla. Usando métodos bioquímicos que mapeiam onde proteínas se ligam ao DNA, combinados com leituras globais de RNA das retinas de camundongos, a equipe descobriu que ZNF124 se liga e ativa outro gene chamado MSX2. Em células saudáveis, ZNF124 adere a uma sequência curta específica na região “liga” do MSX2 e aumenta sua atividade. Em camundongos sem Gm20541, os níveis de MSX2 caíram mais da metade. Quando os pesquisadores deletaram MSX2 especificamente em células bastonetes, esses animais também desenvolveram afinamento da camada de fotorreceptores e segmentos externos encurtados, espelhando os defeitos observados nos camundongos com nocaute semelhante ao de ZNF124. Isso posiciona MSX2 diretamente a jusante de ZNF124 em uma via essencial para a sobrevivência dos fotorreceptores.
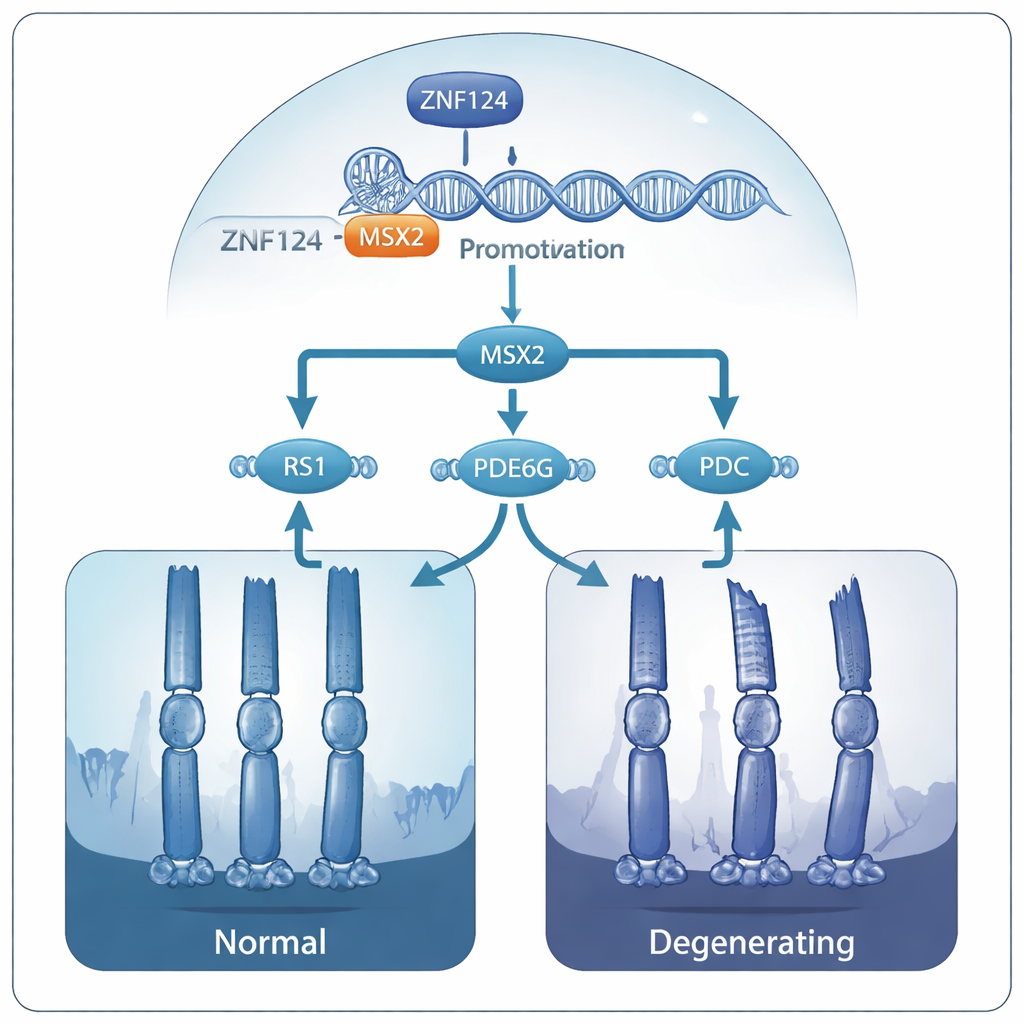
De interruptores gênicos a fotorreceptores frágeis
Análises adicionais mostraram que MSX2, por sua vez, ajuda a manter vários outros genes já conhecidos por estarem ligados a doenças retinianas hereditárias: RS1, PDE6G e PDC. Esses genes sustentam a estrutura da retina e a química do sinal visual. Quando MSX2 foi reduzido, os três genes ficaram menos ativos e seus produtos proteicos diminuíram. Os autores propõem que, em pessoas com mutações deletérias em ZNF124, toda essa cascata fica enfraquecida: ZNF124 não consegue mais ativar plenamente MSX2, MSX2 falha em sustentar RS1, PDE6G e PDC, e com o tempo os fotorreceptores perdem sua integridade estrutural e morrem, levando à perda progressiva da visão.
O que isso significa para pacientes e terapias
Para um público não especializado, a mensagem central é que a retina depende de uma hierarquia finamente ajustada de interruptores genéticos. Este trabalho identifica ZNF124 como um novo interruptor de nível superior cuja falha pode causar cegueira hereditária por meio de um parceiro a jusante específico, MSX2, e seus genes-alvo. Clinicamente, ZNF124 pode agora ser adicionado aos painéis de testes genéticos, ajudando mais famílias a obter diagnósticos precisos. A longo prazo, terapias que restaurem a atividade de ZNF124, MSX2 ou dos genes afetados a jusante podem ajudar a estabilizar ou resgatar as células sensíveis à luz, oferecendo nova esperança para pessoas com formas atualmente inexplicadas de retinose pigmentar.
Citação: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
Palavras-chave: retinose pigmentar, fotorreceptores, ZNF124, MSX2, doença retinal hereditária