Clear Sky Science · pt
HIF2α-induzido lisil oxidase protege a gravidez bem-sucedida remodelando colágenos na interface feto-materna
Por que o útero precisa se preparar para uma nova chegada
Antes que uma gravidez possa se estabelecer, um embrião precoce precisa fazer algo notável: penetrar na parede do útero e construir um sistema de suporte à vida, a placenta. Este artigo explora como o tecido materno se remodela silenciosamente para receber o embrião, com foco em como níveis baixos de oxigênio e uma enzima pouco conhecida ajudam a preparar o revestimento uterino. Compreender essa coreografia delicada pode esclarecer por que algumas gestações falham muito cedo e sugerir novas formas de prevenir infertilidade e complicações na gravidez.
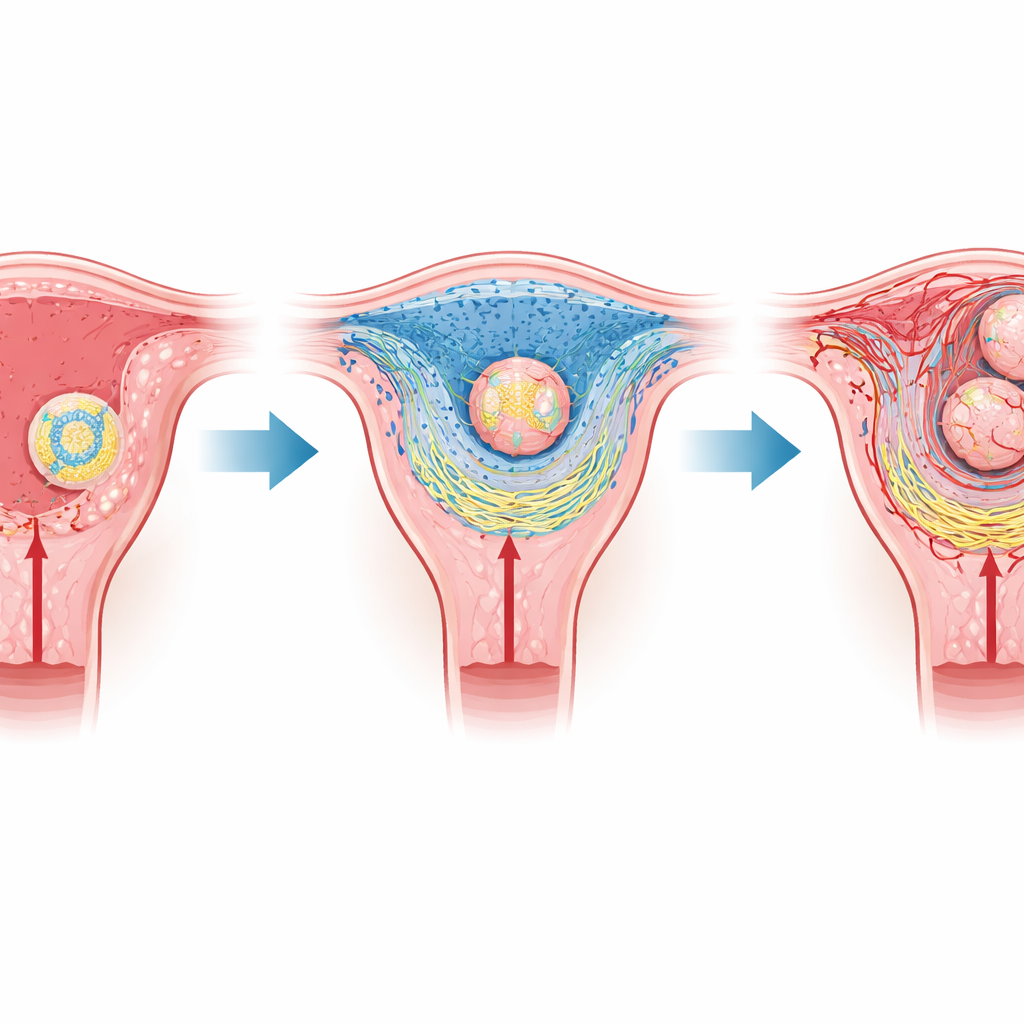
Um encontro delicado entre mãe e embrião
Em mamíferos como camundongos e humanos, o estágio mais precoce da gravidez depende da implantação, quando o embrião se prende e então invade o revestimento uterino. O embrião está envolto por uma camada de células especializadas que depois formarão a placenta, enquanto o tecido materno se transforma numa camada acolchoada chamada decídua. Mais próxima do embrião encontra-se uma região fina conhecida como zona decídua primária, que não tem vasos sanguíneos e, portanto, contém pouco oxigênio. Trabalhos anteriores mostraram que esse nicho naturalmente de baixa oxigenação ajuda a desencadear a implantação, mas não se entendia bem como uma condição física tão simples poderia reorganizar tecidos inteiros.
Baixo oxigênio como um interruptor oculto
Os autores usaram uma técnica poderosa chamada transcriptômica espacial, que mapeia a atividade gênica diretamente em cortes de tecido, para estudar úteros de camundongos nos dias em que os embriões se prendem e invadem. Eles focaram numa proteína chamada HIF2α, que é ativada em condições de baixa oxigenação e atua como um interruptor genético. Em camundongos normais, células da zona decídua primária mostraram forte atividade de genes associados à hipoxia e à construção do material de suporte ao redor, incluindo colágenos que formam a matriz extracelular. Quando HIF2α foi removida apenas do útero, a disposição geral dos tipos celulares parecia surpreendentemente normal. Mas em alta resolução, a rede de colágeno estava desorganizada, a superfície epitelial não se abria adequadamente, e as células embrionárias tinham dificuldade para penetrar o tecido materno.
Uma enzima que entrecruza o arcabouço
Aprofundando, a equipe identificou um ator-chave a montante de HIF2α: a lisil oxidase, ou Lox, uma enzima que entrecruza quimicamente fibras de colágeno e ajuda a tornar o tecido mais rígido e estável. Em gestações normais, os níveis de Lox aumentaram fortemente ao redor dos embriões precisamente quando eles começaram a invadir. Em úteros sem HIF2α, a expressão de Lox caiu, e as fibras de colágeno pareceram fragmentadas em vez de formar uma malha densa. Para testar diretamente a importância de Lox, os pesquisadores criaram camundongos em que Lox foi deletada apenas no útero. Essas fêmeas engravidaram com menos frequência, carregaram menos embriões e frequentemente mostraram sinais de perda embrionária e sangramento mais tarde na gestação, apesar de os primeiros passos de fixação e espessamento do tecido parecerem inicialmente normais.
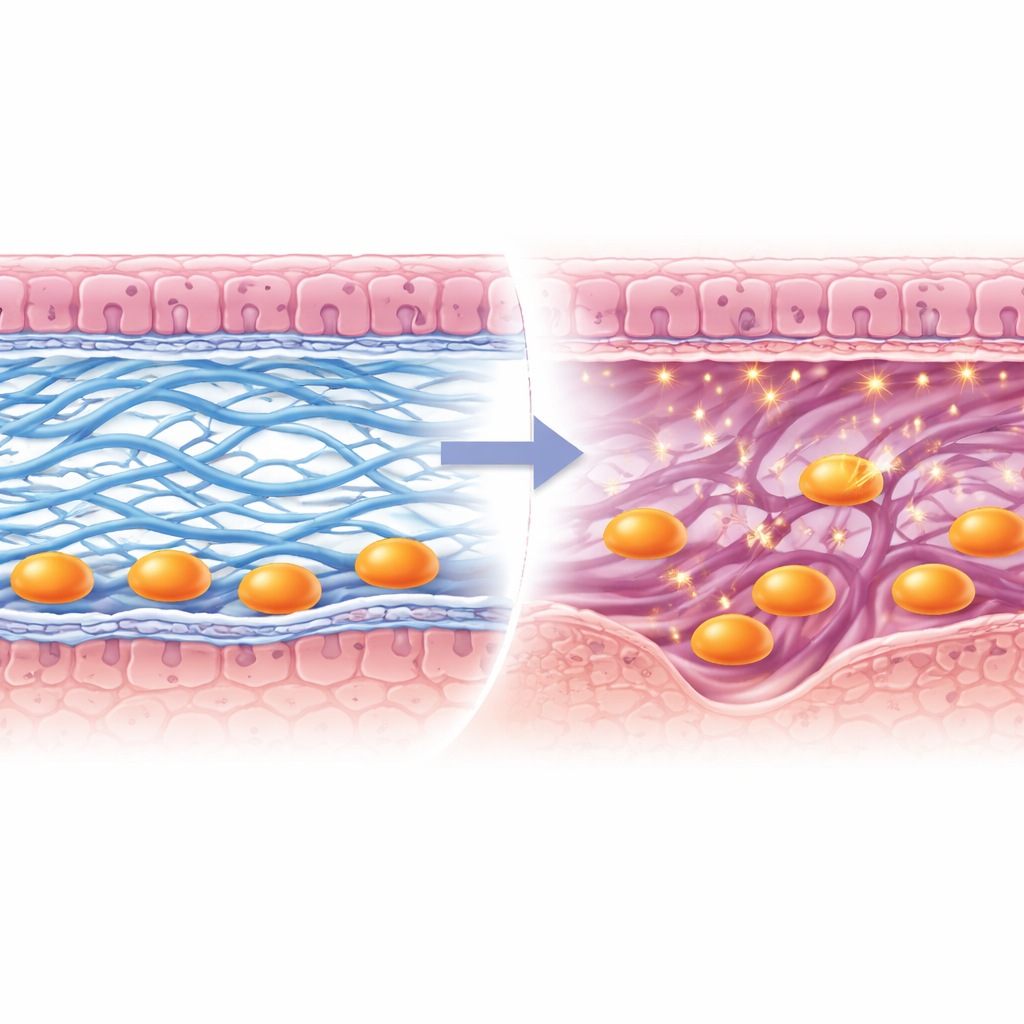
Abrindo um caminho para a placenta
Imagens cuidadosas revelaram o que deu errado quando Lox estava ausente. Uma fina lâmina rica em proteína chamada membrana basal, que normalmente se degrada para permitir a passagem das células embrionárias, permaneceu em grande parte intacta. Fibras de colágeno tipo I no estroma subjacente não conseguiram formar feixes robustos e contínuos, enquanto o colágeno tipo IV na membrana basal não foi adequadamente removido próximo às células invasoras. Como resultado, as células trofoblásticas — os pioneiros derivados do embrião que constroem a placenta — ficaram retidas na superfície em vez de perfurarem a camada materna. A equipe também constatou que uma enzima que corta colágeno, Mmp9, não foi ativada nesses trofoblastos, dificultando ainda mais seu avanço. Com o tempo, as estruturas placentares se formaram de maneira deficiente, os embriões cresceram de forma anômala e o sucesso da gravidez diminuiu.
O que isso significa para a saúde da gravidez
Em conjunto, os achados delineiam uma cadeia de eventos em que o baixo oxigênio na zona de implantação precoce ativa HIF2α, que por sua vez aumenta Lox. Lox então remodela e entrecruza as fibras de colágeno e ajuda a desmontar a membrana basal, além de permitir que enzimas como Mmp9 limpem um caminho. Esse remodelamento fornece tanto um arcabouço estrutural quanto uma porta aberta para que as células trofoblásticas invadam e construam a placenta. Para um leitor leigo, a mensagem é que o sucesso da gravidez depende não apenas de embriões saudáveis e hormônios, mas também do discreto replanejamento da arquitetura tecidual materna. Interrupções nessa via hipóxia–HIF2α–Lox podem estar na base de alguns casos de infertilidade inexplicada, aborto espontâneo e distúrbios ligados à invasão placentária inadequada, sugerindo novos marcadores diagnósticos e alvos terapêuticos para apoiar a gravidez precoce.
Citação: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Palavras-chave: implantação embrionária, matriz extracelular uterina, lisil oxidase, invasão trofoblástica, desenvolvimento placentário