Clear Sky Science · pt
Alvo na fosfatase mitocondrial PGAM5 alivia ferroptose e pancreatite aguda ao aumentar a expressão de FSP1 mediada por NRF2
Por que células estressadas e pâncreas doloridos importam
Quando as células são pressionadas demais, podem morrer de maneiras que danificam todo o organismo. Uma dessas formas de morte celular, chamada ferroptose, é impulsionada pelo ferro e por reações químicas descontroladas que “enferrujam” os lipídios das membranas celulares. Esse processo tem sido associado a lesões em órgãos, incluindo uma condição dolorosa e às vezes fatal conhecida como pancreatite aguda. O estudo por trás deste artigo desvenda um interruptor de controle nas mitocôndrias — as usinas da célula — que pode aumentar ou diminuir a ferroptose, e mostra como bloquear esse interruptor pode proteger o pâncreas em um modelo murino.
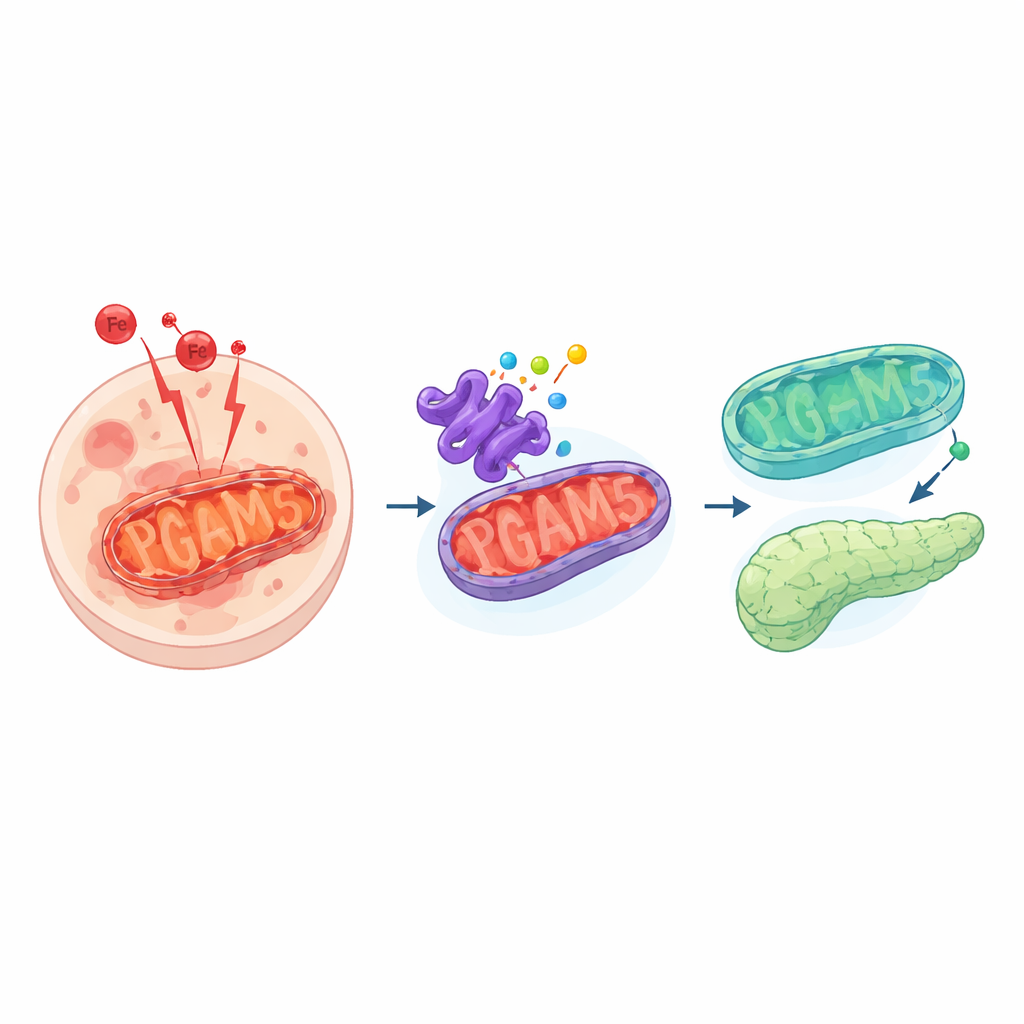
Uma forma perigosa de morte celular
A ferroptose é diferente de formas de morte celular mais familiares, como a apoptose. Em vez de uma autodestruição ordenada, células em ferroptose atravessam uma tempestade de reações mediadas por ferro que tornam rançosos os lipídios delicados de suas membranas. Isso cria subprodutos tóxicos e buracos nas membranas que, em última análise, matam a célula. Normalmente, as células controlam isso com sistemas protetores que desintoxicam essas moléculas reativas. Quando esses sistemas falham ou são sobrecarregados, a ferroptose pode espalhar danos pelos tecidos, contribuindo para doenças que vão do câncer à falência de órgãos.
Um interruptor mitocondrial na mira
Os pesquisadores focaram em uma proteína chamada PGAM5, que se localiza na face interna das mitocôndrias e atua como um centro de sinalização. A PGAM5 ajuda a controlar a forma mitocondrial, responde ao estresse e influencia como as células lidam com a oxidação. Surpreendentemente, quando a equipe reduziu PGAM5 ou forçou as células a produzir mais da proteína, as células ficaram mais difíceis de matar por ferroptose. Inibição química de PGAM5, silenciamento genético e superexpressão reduziram o acúmulo de subprodutos lipídicos danosos e diminuíram a morte celular induzida por um fármaco que provoca ferroptose. Isso revelou que o sistema é finamente ajustado: tanto muito pouca quanto muita PGAM5 empurram as células para um estado mais protegido.
Ligando um escudo interno
Aprofundando-se, os autores descobriram que a influência da PGAM5 passa por um eixo protetor envolvendo outros dois elementos: NRF2 e FSP1. NRF2 é um regulador mestre que, quando ativo no núcleo, liga um amplo conjunto de defesas antioxidantes. FSP1 é um dos seus defensores downstream que ajuda a regenerar um antioxidante solúvel em gordura, bloqueando danos lipídicos na membrana celular. Quando os níveis de PGAM5 foram alterados, as células aumentaram tanto a mensagem quanto os níveis proteicos de NRF2, e NRF2 translocou mais prontamente do citoplasma para o núcleo. Lá, elevou a produção de FSP1. Bloquear FSP1 ou NRF2 eliminou a proteção, restaurando a sensibilidade à ferroptose, o que mostra que essa cadeia PGAM5–NRF2–FSP1 é essencial para a resiliência observada.
Estresse energético como mensageiro oculto
O estudo também revelou como o estresse mitocondrial é traduzido nessa resposta protetora. Perturbar a PGAM5 desequilibrou as mitocôndrias e alterou a moeda energética da célula: a razão de moléculas de menor energia (AMP e ADP) para a de alta energia ATP aumentou, sinalizando estresse energético. Isso, por sua vez, ativou a enzima sensora de energia AMPK. A AMPK ativada modificou diretamente NRF2 de uma forma que favoreceu sua entrada no núcleo, aumentando ainda mais a produção de FSP1. Quando a AMPK foi removida do sistema, NRF2 deixou de se acumular no núcleo, os níveis de FSP1 caíram e as células novamente sucumbiram à ferroptose. Assim, a PGAM5 conecta a condição mitocondrial a uma resposta mais ampla de energia e antioxidantes que protege as células da morte induzida por ferro.
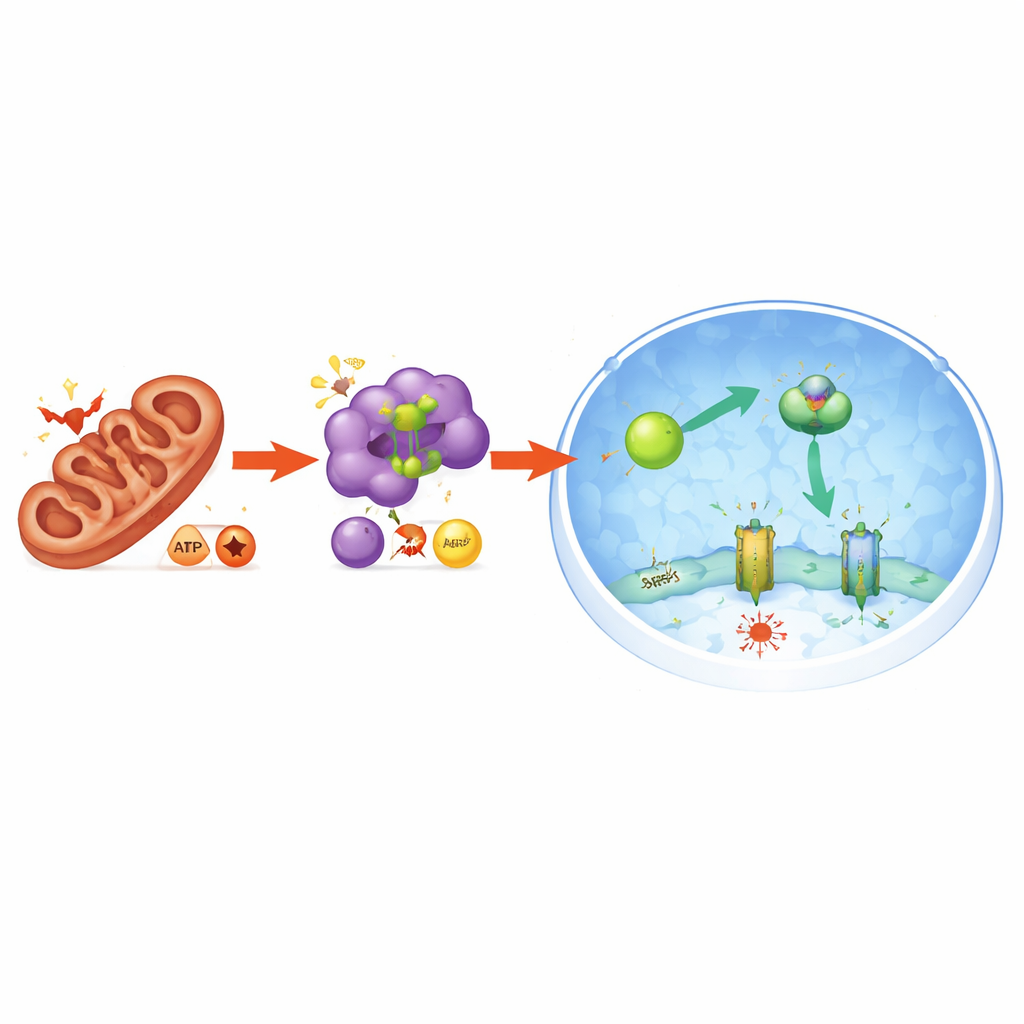
Protegendo o pâncreas em animais vivos
Para testar se esse mecanismo importa em um órgão inteiro, os cientistas recorreram a um modelo murino de pancreatite aguda desencadeada por altas doses do aminoácido arginina. Nesse modelo, o pâncreas apresenta dano extenso, níveis elevados de enzimas sanguíneas que sinalizam lesão tecidual e uma onda de moléculas inflamatórias. Marcadores de peroxidação lipídica — uma assinatura de ferroptose — também aumentaram acentuadamente no pâncreas. Tratar os camundongos com um composto inibidor de PGAM5 aliviou esses sintomas: os marcadores sanguíneos de dano caíram, o tecido pancreático apresentou melhor aspecto ao microscópio e os sinais inflamatórios diminuíram. Ao mesmo tempo, os marcadores de ferroptose caíram, enquanto a atividade da AMPK, NRF2 e os níveis de FSP1 aumentaram no pâncreas, correspondendo à via protetora vista em cultura celular.
O que isso significa para tratamentos futuros
Em conjunto, o trabalho identifica a PGAM5 como um ponto de controle central que liga o estresse mitocondrial, o estado energético celular e um poderoso programa antioxidante que bloqueia a ferroptose. Ao reduzir a atividade da PGAM5, as células ativam AMPK e NRF2, elevam FSP1 e suportam melhor os danos lipídicos induzidos por ferro. Em camundongos, essa estratégia reduz a lesão pancreática na pancreatite aguda. Para o leitor leigo, a mensagem é que os pesquisadores encontraram um novo “disjuntor” interno que pode prevenir uma forma destrutiva de morte celular. Embora ainda haja muito a ser feito antes do uso clínico, mirar na PGAM5 ou em parceiros downstream pode abrir novas vias para tratar condições em que a ferroptose e a falha mitocondrial desempenham um papel prejudicial.
Citação: Ma, S., Qin, J., Luan, J. et al. Targeting mitochondrial phosphatase PGAM5 alleviates ferroptosis and acute pancreatitis by upregulating NRF2-mediated FSP1 expression. Cell Death Dis 17, 252 (2026). https://doi.org/10.1038/s41419-026-08484-9
Palavras-chave: ferroptose, mitocôndrias, pancreatite aguda, estresse oxidativo, morte celular