Clear Sky Science · pt
Ubiquitinação de mH2A1 mediada por UBE3A ativa a transcrição de TERT para promover resistência à senescência no câncer de pâncreas
Por que esta pesquisa importa para pacientes
O câncer de pâncreas está entre os mais letais, em parte porque as células tumorais são extraordinariamente habilidosas em escapar dos freios naturais do envelhecimento do corpo. Este estudo revela um “circuito de sabotagem” molecular oculto que ajuda as células do câncer pancreático a permanecerem jovens, continuarem a se dividir e resistirem ao tratamento. Ao compreender esse circuito, os pesquisadores apontam uma nova forma de induzir senescência nessas células e, em seguida, eliminá‑las seletivamente, abrindo espaço para terapias combinadas mais inteligentes.
Envelhecimento como o freio natural ao tumor
Todas as células carregam um relógio interno que eventualmente as faz parar de se dividir, um processo conhecido como senescência. Em lesões pancreáticas iniciais, esse relógio pode retardar o desenvolvimento tumoral ao levar células pré‑cancerosas à aposentadoria permanente. Muitos tratamentos anticâncer também atuam, em parte, forçando as células tumorais a entrar nesse estado de envelhecimento. Contudo, se essas células senescentes não forem eliminadas, elas podem alimentar inflamação e ajudar o câncer a retornar. Isso deu origem a uma nova ideia terapêutica: primeiro induzir senescência nas células cancerosas e depois eliminar essas células envelhecidas com fármacos “senolíticos” que são especialmente tóxicos para elas.
Uma enzima promotora de câncer em destaque
Para identificar genes que ajudam as células do câncer pancreático a desafiar a senescência, a equipe explorou grandes conjuntos de dados de pacientes e então validou suas descobertas em amostras tumorais e linhagens celulares. Eles se concentraram em uma proteína chamada UBE3A, uma enzima que marca outras proteínas para destruição. Os níveis de UBE3A eram muito maiores em tumores pancreáticos do que no tecido normal adjacente, e pacientes com mais UBE3A tendiam a ter cânceres maiores, mais avançados e pior sobrevida. Em células cultivadas em laboratório, o aumento de UBE3A acelerou o crescimento, reduziu marcadores clássicos de envelhecimento celular e diminuiu as secreções inflamatórias típicas de células senescentes. Silenciar UBE3A teve o efeito oposto e, em modelos de camundongo, reduziu drasticamente o crescimento tumoral e as metástases hepáticas. 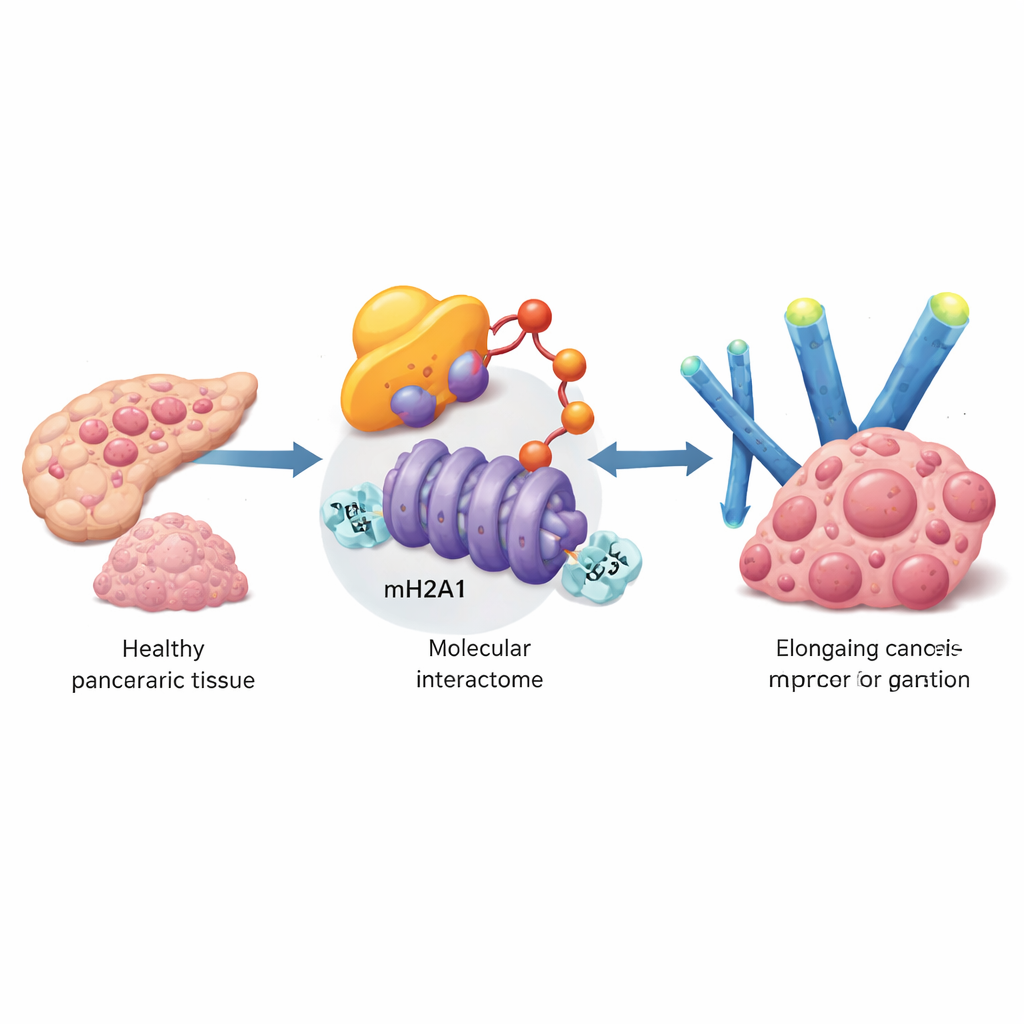
Como as células cancerosas apagam um freio na cromatina
Aprofundando, os pesquisadores investigaram quais moléculas são alvos da UBE3A. Usando triagens avançadas por espectrometria de massa, eles descobriram que a UBE3A se liga e marca quimicamente uma variante especial da histona chamada macroH2A1 (mH2A1), que ajuda a compactar o DNA e normalmente atua como um freio na atividade gênica. A UBE3A anexa uma cadeia de etiquetas de “destrua‑me” à mH2A1 em uma posição específica, fazendo com que ela seja degradada pela maquinaria celular de eliminação de proteínas. Em tumores pancreáticos, os níveis de mH2A1 eram menores onde UBE3A estava alto, e restaurar mH2A1 contrariou a capacidade da UBE3A de bloquear a senescência e impulsionar o crescimento tumoral. Isso revela um passo chave: as células do câncer de pâncreas removem uma marca protetora na cromatina usando a UBE3A para eliminar a mH2A1.
Desbloqueando a telomerase para manter as células jovens
A próxima pergunta foi quais genes ficam liberados quando a mH2A1 é removida. Ao combinar sequenciamento de RNA com mapas de ligação ao DNA, a equipe identificou o gene da telomerase, TERT, como um alvo central. A telomerase mantém as tampas protetoras nas extremidades dos cromossomos, permitindo que as células continuem a se dividir em vez de entrar em senescência. O estudo mostra que a mH2A1 normalmente fica em uma região potenciadora dentro do gene TERT, onde recruta outra enzima, EZH2, para depositar uma marca química repressiva nas histonas vizinhas. Essa combinação mantém o TERT silenciado e permite que os telômeros encurtem. Quando a UBE3A destrói a mH2A1, o complexo repressivo se dissolve, o potenciador se torna ativo, o TERT é ligado, os telômeros são mantidos e as células do câncer pancreático ganham resistência ao envelhecimento. Formas mutantes de UBE3A que não conseguem marcar proteínas, ou mH2A1 mutante que não pode ser marcada, quebram esse circuito e restauram o freio da senescência.
Combinando indução de senescência com limpeza senolítica
Por fim, os pesquisadores testaram se essa via poderia ser explorada terapeuticamente. Inibir a UBE3A empurrou as células do câncer pancreático em direção à senescência e aumentou sua dependência de proteínas anti‑morte da família BCL‑2 — uma vulnerabilidade conhecida das células senescentes. A equipe então combinou a inibição de UBE3A com ABT‑263, um fármaco senolítico que tem como alvo essas proteínas de sobrevivência. Em células cultivadas, a combinação levou muito mais células cancerosas a entrar em morte programada do que cada tratamento isoladamente. Em modelos de camundongo, tumores com UBE3A reduzida encolheram ainda mais quando os animais receberam ABT‑263, e os marcadores de proliferação celular dentro dos tumores caíram acentuadamente. 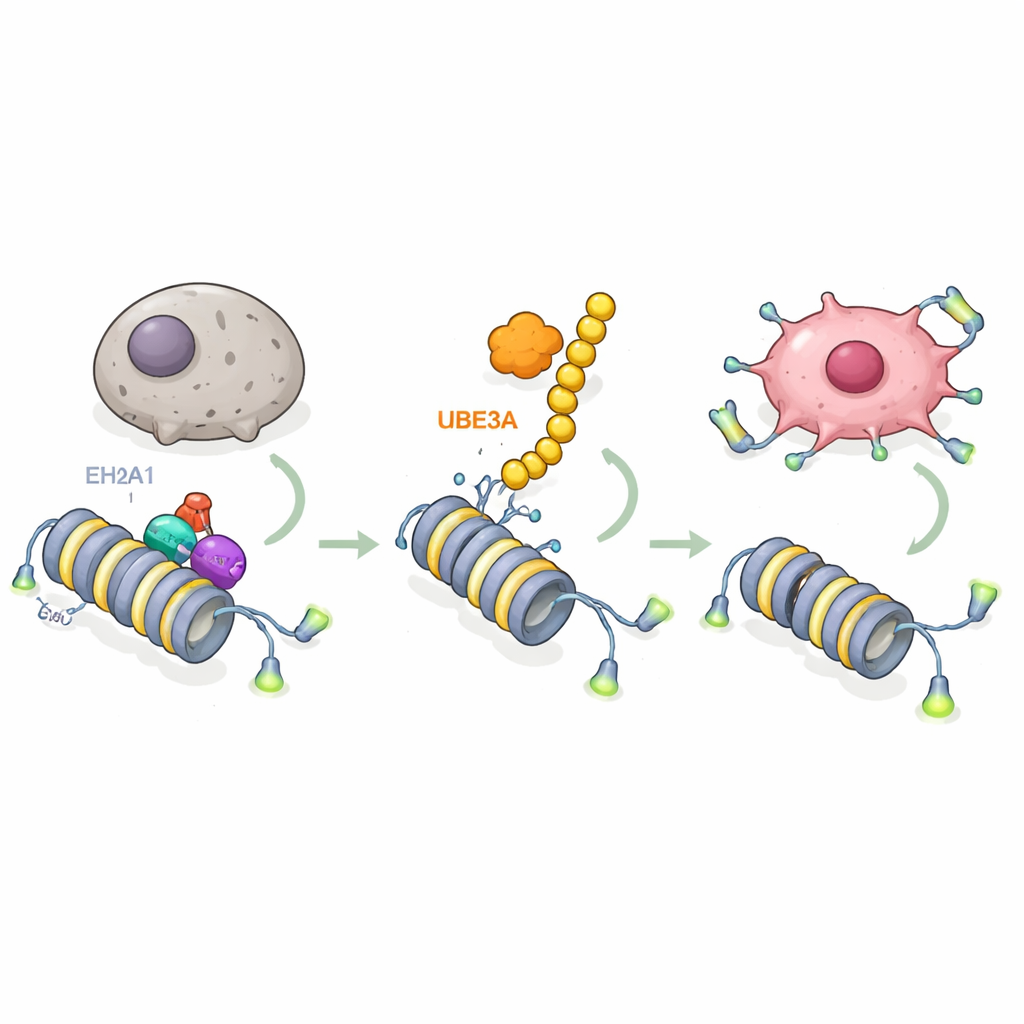
O que isso significa para tratamentos futuros
Este trabalho revela uma cadeia de eventos detalhada pela qual as células do câncer pancreático evitam envelhecer: a UBE3A destrói o freio da cromatina mH2A1, que por sua vez alivia a repressão do gene da telomerase TERT e ajuda a manter os telômeros, permitindo que as células continuem a se dividir. Ao direcionar a UBE3A, os médicos podem ser capazes de religar o programa natural de envelhecimento celular e então usar fármacos senolíticos como o ABT‑263 para eliminar seletivamente essas células cancerosas vulneráveis e envelhecidas. Embora sejam necessários mais estudos para traduzir esse mecanismo em terapias para pacientes, o eixo UBE3A–mH2A1–TERT oferece uma nova e promissora abordagem contra um dos cânceres mais resistentes ao tratamento.
Citação: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Palavras-chave: câncer de pâncreas, senescência celular, telomerase, ligase de ubiquitina, terapia senolítica