Clear Sky Science · pt
Semaforina 6D induz respostas antitumorais de interferon tipo I para reprogramar o microambiente tumoral no câncer colorretal
Por que esta pesquisa importa para pessoas com câncer de cólon
O câncer colorretal é uma das principais causas de morte por câncer no mundo, em parte porque muitos tumores resistem aos tratamentos atuais, incluindo medicamentos imunoterápicos de ponta. Este estudo revela um “sistema de freio” natural dentro dos tumores de cólon que frequentemente está desativado e mostra como reativá-lo pode convidar o sistema imunológico a voltar à luta. Compreender esse interruptor oculto pode ajudar médicos a prever melhor os desfechos e a desenhar terapias combinadas que tornem a imunoterapia eficaz para muito mais pacientes.
Um guardião silencioso dentro das células tumorais
No centro do trabalho está uma molécula chamada Semaforina 6D (SEMA6D), inicialmente conhecida por guiar o crescimento de nervos e moldar o coração em desenvolvimento. Os pesquisadores descobriram que a SEMA6D na verdade se comporta como um supressor tumoral no câncer colorretal: no tecido de cólon saudável ela está presente, mas no tecido canceroso seus níveis são marcadamente reduzidos. Em múltiplos conjuntos de dados de pacientes e amostras tumorais, baixos níveis de SEMA6D estiveram associados a tumores maiores, invasão mais profunda, mais metástases e sobrevida significativamente pior. Esse padrão se manteve mesmo quando outros fatores clínicos foram considerados, indicando que a SEMA6D é um marcador independente da agressividade do tumor colorretal.
Como os tumores desligam essa proteção
A equipe então investigou por que a SEMA6D costuma estar ausente nos tumores. Eles descobriram que o gene é frequentemente silenciado por uma modificação química chamada hipermetilação do promotor—etiquetas químicas extras adicionadas à região de controle do gene que funcionam como fita adesiva molecular sobre um interruptor de luz. Usando mapeamento detalhado do DNA, demonstraram que trechos-chave da região reguladora da SEMA6D são fortemente metilados em células cancerosas, mas não em células normais do cólon. Quando trataram células cancerosas com um fármaco desmetilante usado em cânceres hematológicos, as marcas de metilação foram removidas e a produção de SEMA6D foi restaurada. Os níveis mais baixos de SEMA6D foram encontrados em subtipos de câncer de cólon já conhecidos por alta metilação do DNA, grande instabilidade genética e forte tendência a disseminação, reforçando a ligação entre esse mecanismo de silenciamento e doença agressiva.
De bloqueador de crescimento a impulsionador imune
Restaurar a SEMA6D alterou o comportamento tumoral em dois níveis. Primeiro, no nível da célula cancerosa, forçar a expressão de SEMA6D retardou seu crescimento, reduziu a capacidade de migração e invasão e reverteu características da transição epitélio–mesênquima, um programa que ajuda os tumores a se espalharem. Em culturas e organoides tridimensionais derivados de tumores de pacientes, células com mais SEMA6D formaram menos colônias, menores e mostraram mais sinais de morte celular programada. Em camundongos, tumores projetados para superexpressar SEMA6D cresceram mais lentamente e produziram menos metástases pulmonares e hepáticas, enquanto a redução de SEMA6D teve o efeito oposto. Segundo, no nível imunológico, tumores ricos em SEMA6D em camundongos imunocompetentes continham muito mais células T CD4 e CD8—as principais forças de ataque da imunidade adaptativa—enquanto tumores pobres em SEMA6D estavam relativamente vazios desses defensores. Quando os pesquisadores depletaram células T, o efeito de desaceleração do crescimento promovido pela SEMA6D desapareceu em grande parte, mostrando que boa parte de seu poder vem de mobilizar o sistema imune.
Decodificando a via de alarme interna
Aprofundando-se, o estudo mapeou os passos moleculares que conectam a SEMA6D à ativação imune. Na superfície das células tumorais, a SEMA6D sinaliza por meio de um receptor parceiro chamado Plexin A4. No interior da célula, essa dupla interage fisicamente com uma proteína chamada IRF9, um componente-chave da maquinaria que responde aos interferons tipo I—os mesmos sinais de alarme antivirais que as células usam para combater infecções. Quando SEMA6D está presente e o Plexin A4 está intacto, IRF9 e seus parceiros são ativados, ligam conjuntos de genes estimulados por interferon e ajudam a célula tumoral a emitir sinais que atraem e ativam células T. Remover SEMA6D ou Plexin A4 quebra essa cadeia e silencia o alarme; restaurar IRF9 pode resgatar parcialmente o efeito. Em camundongos, tumores com sinalização ativa SEMA6D–Plexin A4–IRF9 apresentaram maior infiltração de células T e níveis mais baixos do marcador de proliferação Ki-67, consistente com maior pressão imune sobre o câncer.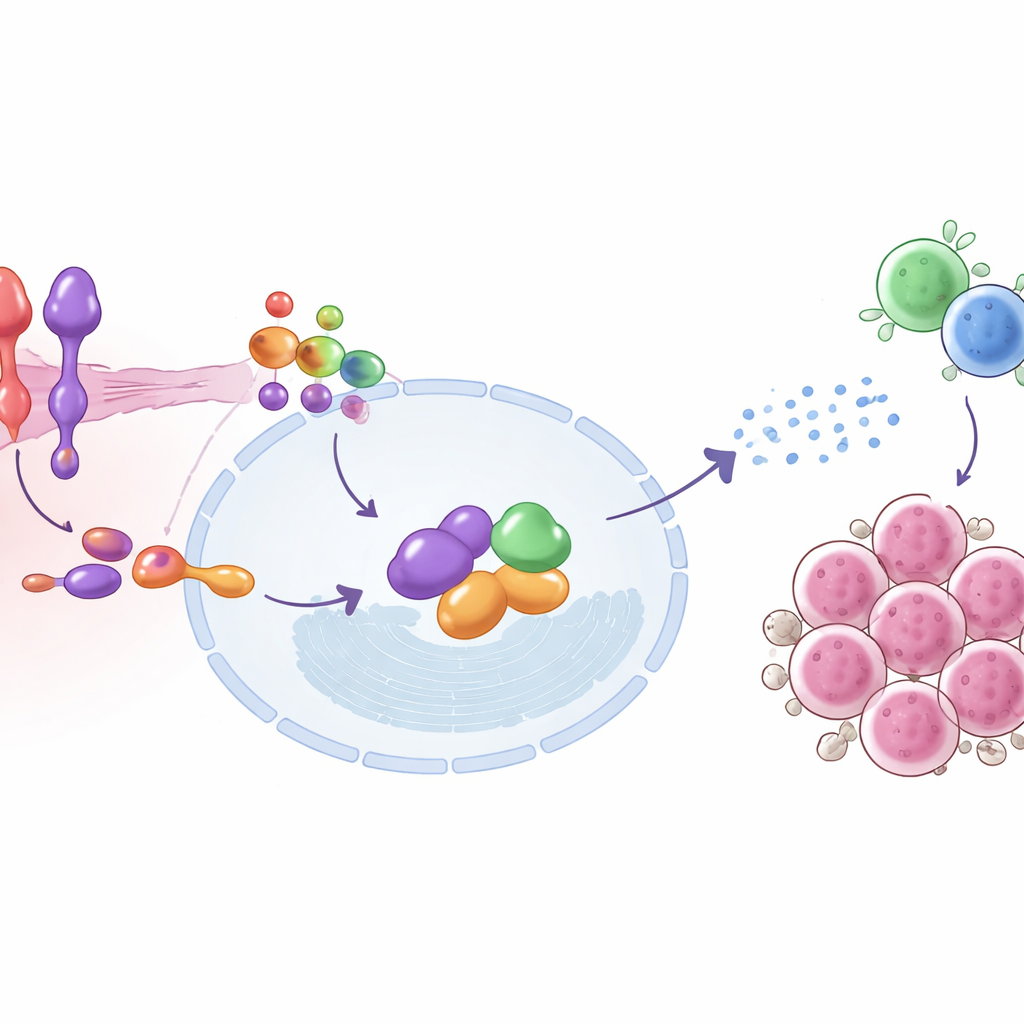
Reacendendo a imunidade com terapia combinada
Como a SEMA6D é silenciada por metilação, os autores testaram se um fármaco hipometilante poderia reativá-la em tumores vivos e, assim, melhorar as respostas ao bloqueio de pontos de controle imune. Em tumores de cólon de camundongos tratados com decitabina seguida por um anticorpo anti–PD-1, os tumores cresceram muito mais lentamente do que com qualquer dos tratamentos isolados. A combinação aumentou os níveis de SEMA6D, potenciou a atividade da via de interferon, reduziu a proliferação celular e reforçou a infiltração de células T. Esses resultados sugerem que, ao remover “trancas” de metilação de genes relevantes para o sistema imune como a SEMA6D, drogas epigenéticas podem transformar tumores imunologicamente “frios” em tumores mais “quentes” e mais vulneráveis a inibidores de checkpoint.
O que isso significa para o cuidado futuro
Para o público em geral, a conclusão é que alguns cânceres de cólon se escondem do sistema imunológico ao desligar quimicamente um sinal interno de perigo. Este trabalho identifica a SEMA6D tanto como esse sinal quanto como uma alça promissora para terapia. Medir a SEMA6D e seu estado de metilação pode ajudar a classificar tumores, prever desfechos e orientar escolhas terapêuticas. Igualmente importante, o estudo fornece uma justificativa biológica clara para combinar agentes desmetilantes do DNA com imunoterapia para reativar a vigilância imune em pacientes cujos tumores atualmente não respondem. Embora sejam necessários ensaios clínicos, essa estratégia pode um dia ampliar os benefícios da imunoterapia para um grupo muito maior de pessoas com câncer colorretal.
Citação: Shi, W., Zhang, F., Sun, WQ. et al. Semaphorin 6D drives anti-tumor type I interferon responses to reprogram the tumor microenvironment in colorectal cancer. Cell Death Dis 17, 256 (2026). https://doi.org/10.1038/s41419-026-08478-7
Palavras-chave: câncer colorretal, microambiente tumoral, terapia epigenética, interferon tipo I, imunologia tumoral