Clear Sky Science · pt
Redirecionando o destino das células de melanoma: moduladores de TRPM8 desencadeiam apoptose e aumentam a citotoxicidade de células NK
Por que usar um “sensor de frio” contra o câncer de pele importa
O melanoma é uma forma perigosa de câncer de pele que frequentemente aprende a escapar tanto dos medicamentos quanto do sistema imunológico. Este estudo explora uma vulnerabilidade inesperada nas células de melanoma: uma proteína chamada TRPM8, mais conhecida como o sensor que permite às células nervosas perceber frio ou mentol. Os pesquisadores mostram que fármacos cuidadosamente projetados para bloquear o TRPM8 podem forçar as células de melanoma a se autodestruírem, além de torná-las mais fáceis de serem atacadas por células imunes natural killer (NK). Essa ação dupla sugere uma nova abordagem para tratar melanomas avançados e resistentes.
Um interruptor oculto nas células de melanoma
Ao explorar grandes bancos de dados sobre câncer e examinar células de melanoma derivadas de pacientes no laboratório, a equipe descobriu que o TRPM8 é muito mais abundante em melanoma metastático do que em pele normal, incluindo melanócitos saudáveis e fibroblastos dérmicos. Por meio de imagens, mostraram que o TRPM8 localiza-se tanto na superfície celular quanto em membranas internas, posicionando-o em pontos estratégicos para influenciar o comportamento celular. Quando aplicaram um painel de novas moléculas direcionadas ao TRPM8, dois compostos (denominados 4 e 9) se destacaram de forma consistente: reduziram drasticamente a sobrevivência das células de melanoma ao longo do tempo, enquanto deixavam as células da pele normal amplamente intactas. Testes genéticos confirmaram que, quando o TRPM8 foi removido, esses fármacos perderam seu poder letal, e quando o TRPM8 foi aumentado, as células de melanoma ficaram ainda mais sensíveis, provando que o efeito depende desse canal específico. 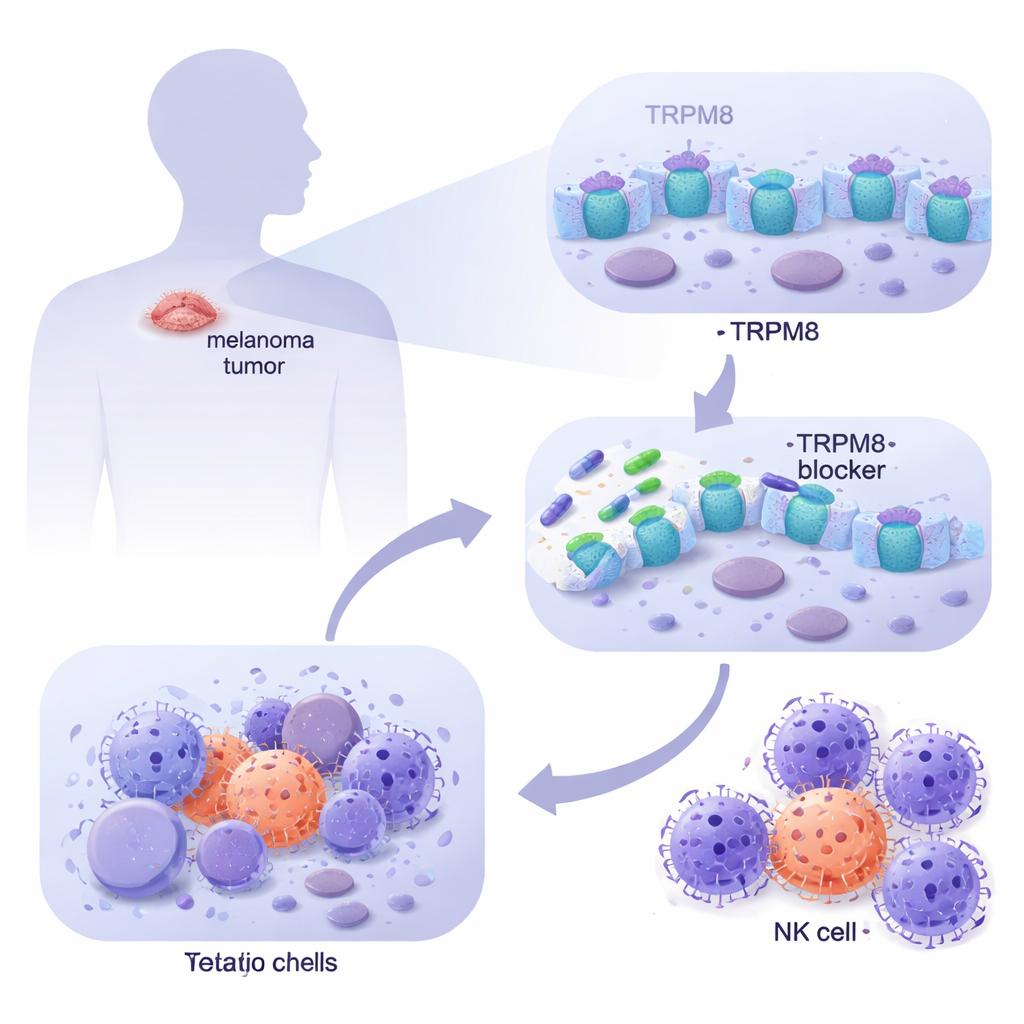
Forçando as células cancerosas a uma crise energética
Diferentemente de ativadores clássicos do TRPM8, como o mentol, que provocam um afluxo de cálcio nas células, esses novos bloqueadores não desencadearam alterações de cálcio. Em vez disso, lançaram uma onda de estresse oxidativo dentro das células de melanoma. Os compostos aumentaram rapidamente as espécies reativas de oxigênio, especialmente dentro das mitocôndrias, as usinas de energia da célula. Esse surto oxidativo fez com que as mitocôndrias perdessem sua carga elétrica, fragmentassem e liberassem citocromo c, um passo chave para ativar o programa interno de “suicídio” da célula. Antioxidantes que neutralizaram essas moléculas reativas resgataram em grande parte as células, mostrando que o desequilíbrio redox não é um efeito colateral, mas o motor da morte celular. A jusante, marcadores clássicos de morte, como ativação da caspase-3 e clivagem da PARP, confirmaram que as células estavam passando por apoptose programada em vez de um dano aleatório.
Desarmando sinais de sobrevivência e despertando um guardião
O impacto oxidativo desencadeou uma resposta de estresse mais ampla. Os fármacos ativaram ATM, um sensor de dano ao DNA, e levaram ao acúmulo e ativação de p53, uma famosa proteína supressora de tumor que decide se uma célula danificada deve se reparar ou morrer. Ao mesmo tempo, os compostos enfraqueceram uma das principais rotas de sobrevivência do melanoma: a via PI3K–AKT. Normalmente, o TRPM8 interage fisicamente com componentes da PI3K para ajudar a manter o AKT em sua forma ativa, promotora de crescimento. Após o tratamento, essa parceria se desfez e a atividade de AKT caiu, inclinando ainda mais o equilíbrio para a morte celular. Importante, essas mudanças foram pronunciadas nas células de melanoma, mas não em células não cancerosas, sugerindo uma janela terapêutica em que o tumor é atingido duramente enquanto o tecido saudável é poupado.
Tornando os tumores mais visíveis para as “esquadrões de ataque” imunológicos
O perigo do melanoma também está em sua habilidade de escapar da vigilância imune. Os pesquisadores, portanto, investigaram o que acontece com as células tumorais que sobrevivem a doses baixas dos bloqueadores de TRPM8 por períodos mais longos. Eles descobriram que essas células remanescentes começaram a exibir mais de um marcador de superfície chamado ULBP1, que atua como um sinal de socorro reconhecido pelos receptores NKG2D das células NK. Outros marcadores relacionados não mudaram, indicando um efeito seletivo. Em esferoides tridimensionais de melanoma, que imitam melhor tumores reais, o pré-tratamento com bloqueadores de TRPM8 não apenas encolheu as estruturas e aumentou a morte celular, mas também as tornou muito mais vulneráveis ao ataque de células NK. Quando ULBP1 ou NKG2D foram bloqueados com anticorpos, essa morte adicional desapareceu em grande parte, mostrando que a melhoria da eliminação imune ocorre por meio desse aperto de mão específico entre tumor e células NK. 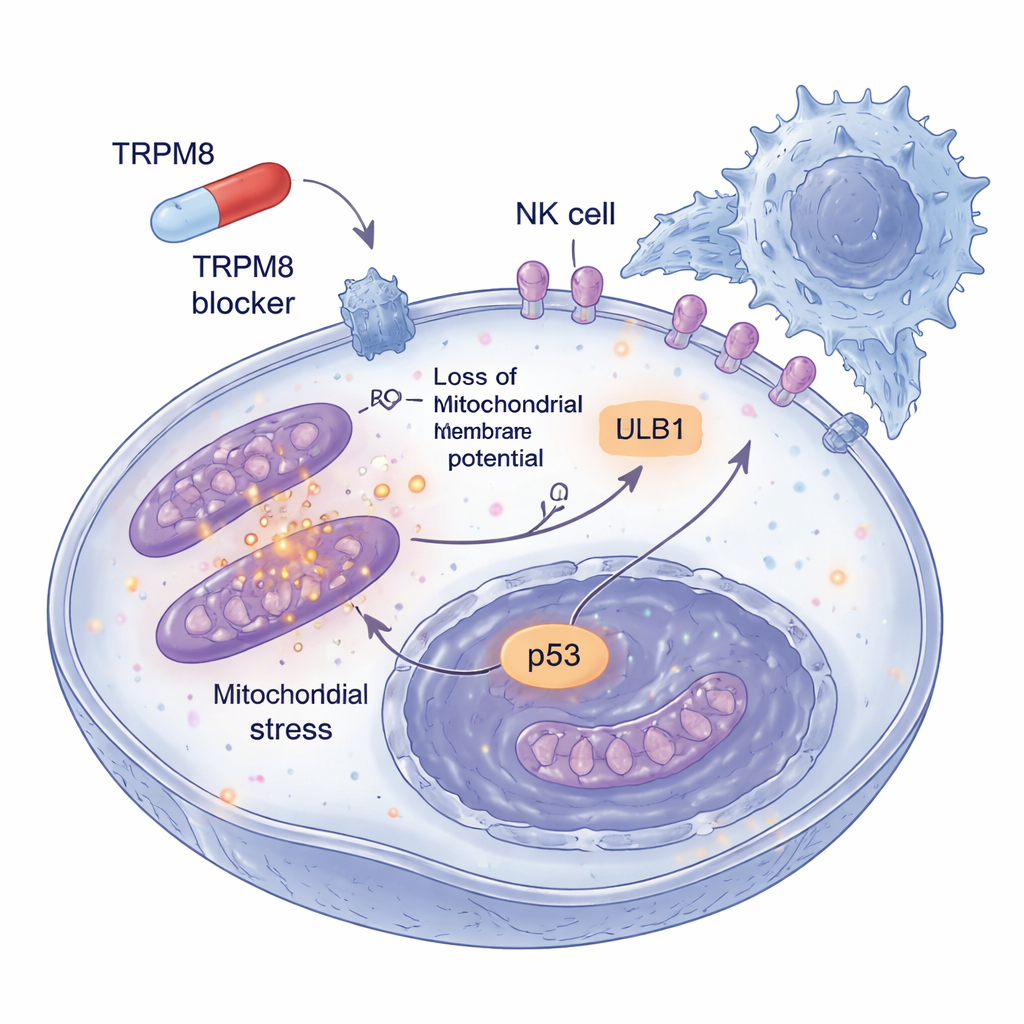
O que isso pode significar para o cuidado futuro do melanoma
Em termos simples, bloquear o “sensor de frio” TRPM8 o transforma em uma alavanca terapêutica: leva as células de melanoma a uma crise mitocondrial e de DNA fatal, ao mesmo tempo em que as identifica para destruição por células NK. Como os fármacos poupam as células da pele normal e não prejudicam as próprias células NK, eles oferecem uma base promissora para novos tratamentos. Os autores sugerem que os bloqueadores de TRPM8 poderiam ser combinados com imunoterapias existentes para atacar o melanoma avançado e resistente a drogas em duas frentes: matar diretamente as células tumorais e tornar os sobreviventes mais fáceis de serem encontrados e destruídos pelo sistema imunológico.
Citação: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Palavras-chave: melanoma, TRPM8, mitocôndrias, estresse oxidativo, células natural killer