Clear Sky Science · pt
KIF20A inibe a ubiquitinação dependente de TRIM21 de DHX9 para aumentar a estabilidade de SOX2, reforçando a stemness e a resistência ao ferroptose em CCEO
Por que esta pesquisa importa para pacientes com câncer oral
O carcinoma espinocelular oral, uma forma comum de câncer de boca, frequentemente recorre e resiste ao tratamento. Muitas falhas de cirurgia, quimioterapia e radioterapia são atribuíveis a um pequeno e obstinado grupo de "células-tronco cancerígenas" que podem regenerar o tumor e resistir à morte celular. Este estudo revela um circuito molecular chave que ajuda essas células a sobreviver e resistir a uma forma mais recente de morte celular chamada ferroptose, e aponta para uma estratégia medicamentosa que pode tornar a quimioterapia padrão mais eficaz.
Um condutor oculto em tumores bucais
Os pesquisadores começaram comparando amostras tumorais de pacientes com câncer oral com tecido saudável próximo. Eles descobriram que uma proteína chamada KIF20A estava consistentemente muito mais alta nas células cancerosas. Ao examinar conjuntos de dados maiores de pacientes, pessoas cujos tumores apresentavam mais KIF20A tendiam a viver por menos tempo, sugerindo que essa proteína está ligada a doença agressiva. 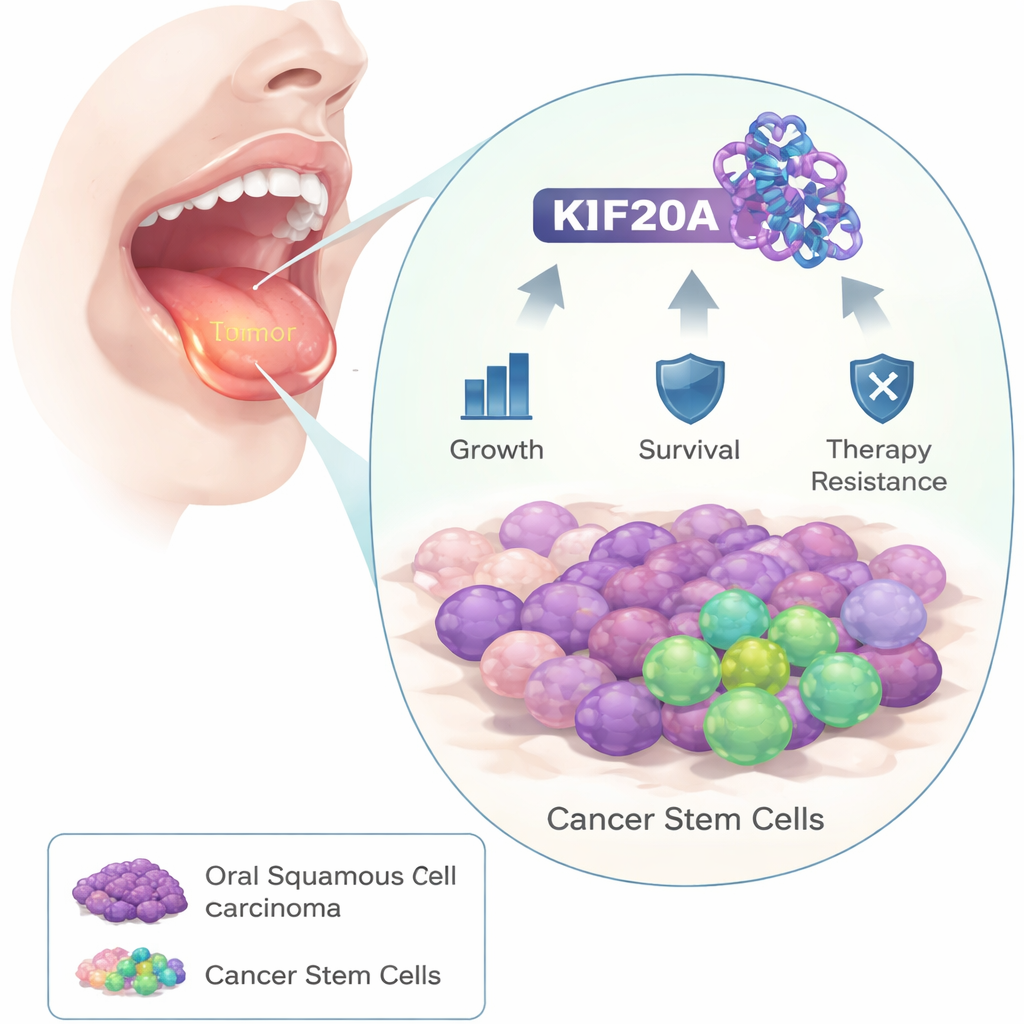
Como KIF20A protege um coadjuvante importante do RNA
Para entender o que KIF20A realmente faz, a equipe usou métodos de mapeamento de proteínas para procurar seus parceiros dentro das células cancerosas. Um parceiro central que emergiu foi DHX9, uma proteína que ajuda a gerir moléculas de RNA e influencia a duração de determinadas mensagens na célula. Os cientistas descobriram que KIF20A se liga a DHX9 e impede que ele seja marcado para destruição por outra proteína, a ligase E3 TRIM21, que normalmente etiqueta o DHX9 com cadeias de ubiquitina que o levam ao triturador proteico da célula. Ao bloquear essa marcação, KIF20A retarda a degradação do DHX9 e aumenta seus níveis, especialmente no citoplasma da célula, onde ele pode atuar sobre alvos específicos de RNA.
Da estabilidade do RNA às células-tronco cancerígenas e à resistência ao ferroptose
Com DHX9 mais estável, outro ator crucial entra em foco: SOX2, um gene mestre que ajuda as células a manterem um estado semelhante ao de células-tronco e a resistir ao tratamento. O estudo mostra que DHX9 protege a mensagem de RNA de SOX2 contra a degradação, permitindo que mais proteína SOX2 seja produzida. Em células de câncer oral, KIF20A em excesso levou a níveis maiores de DHX9 e SOX2, mais formação de esferas tumorais em cultura e uma fração maior de células expressando marcadores de células-tronco — sinais de maior "stemness" cancerígeno. KIF20A também tornou as células menos vulneráveis ao ferroptose, um tipo de morte celular dependente de ferro e lipídios que vem sendo explorado para eliminar células cancerosas resistentes. Quando KIF20A foi desligado, os tumores encolheram mais facilmente em camundongos, e marcadores de ferroptose aumentaram, indicando que os tumores haviam perdido essa proteção.
Um circuito molecular com uma vulnerabilidade tratável
Juntando essas peças, os autores propõem um eixo KIF20A–DHX9–SOX2: KIF20A estabiliza DHX9, DHX9 estabiliza o RNA de SOX2, e SOX2 por sua vez mantém as células-tronco cancerígenas e bloqueia o ferroptose. Esse circuito também alimenta a via PI3K–AKT, uma rota importante de crescimento e sobrevivência em muitos cânceres. 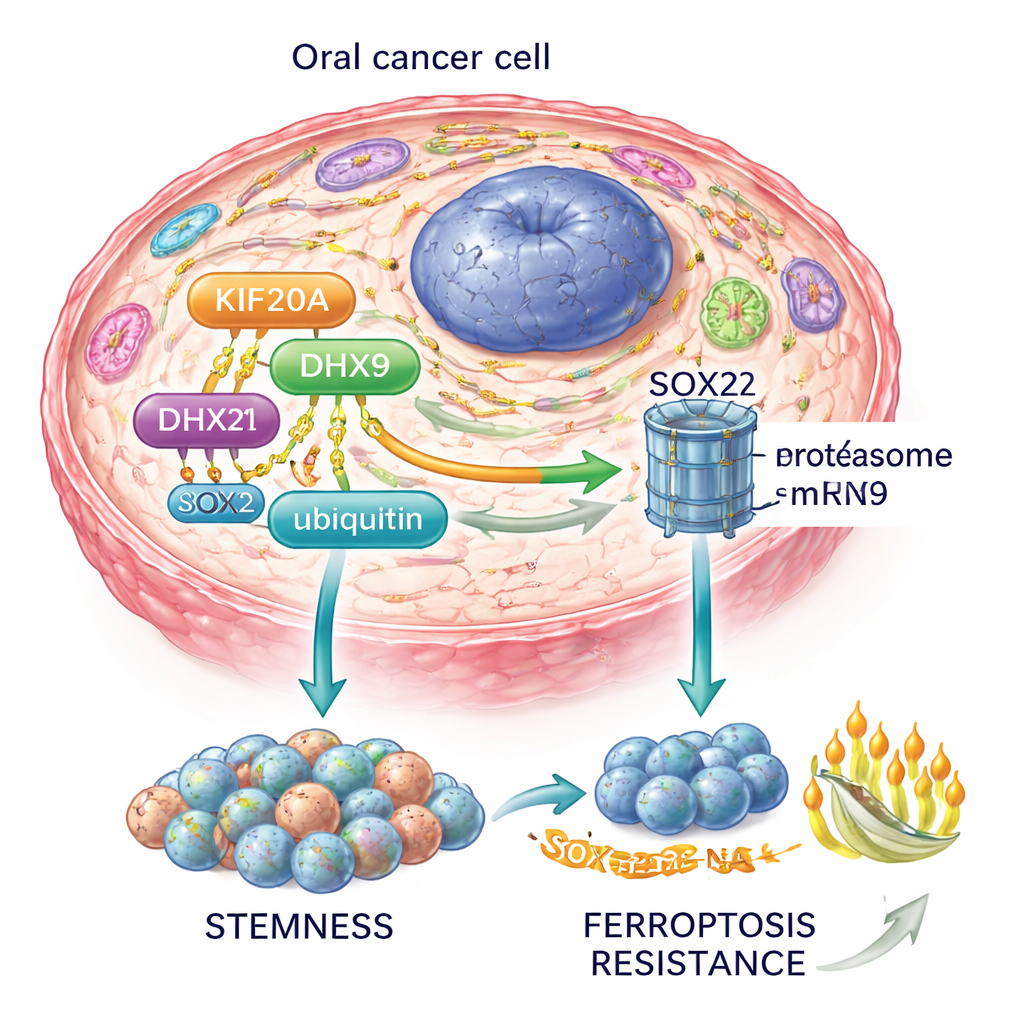
Um fármaco candidato para enfraquecer tumores resistentes
Para avançar rumo ao tratamento, a equipe consultou grandes bancos de dados droga–gene em busca de compostos previstos para contrariar padrões genéticos relacionados a KIF20A. Identificaram ENMD-2076, um inibidor oral multitarget de quinases já testado em outros cânceres. Em células de câncer oral com KIF20A alta, ENMD-2076 reduziu os níveis de KIF20A, DHX9 e SOX2, atenuou a sinalização relacionada à stemness e desacelerou o crescimento. Quando combinado com o quimioterápico padrão cisplatina, ENMD-2076 produziu um efeito anticâncer mais forte do que cada droga isoladamente, tanto em culturas celulares quanto em tumores de camundongos, sem toxicidade aparente adicional.
O que isso significa para terapias futuras
Para um leitor não especialista, a conclusão é que este estudo revela como uma proteína hiperativa, KIF20A, ajuda tumores bucais a manter um pequeno reservatório de células "sementes" vivo e protegido de uma forma promissora de morte celular. Ao mapear essa cadeia — de KIF20A a DHX9 a SOX2 — os pesquisadores destacam novos alvos para fármacos e mostram que um composto experimental existente, ENMD-2076, pode enfraquecer esse eixo e tornar a cisplatina mais eficaz em modelos. Embora mais trabalho seja necessário para testar segurança e confirmar benefícios em pacientes, os achados sustentam um futuro em que bloquear esse circuito poderia ajudar a prevenir recaídas e superar a resistência a medicamentos no câncer oral.
Citação: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Palavras-chave: carcinoma espinocelular oral, células-tronco cancerígenas, ferroptose, KIF20A, SOX2