Clear Sky Science · pt
Selenometionina como um inibidor de ferroptose de duplo mecanismo: biossíntese de GPX4 impulsionada pelo suprimento de selênio além da transsulfuração e caça a ROS mediada pela capacidade redutora independente da atividade de GPX4
Por que proteger nossas células de uma morte “semelhante à ferrugem” importa
As células do nosso corpo podem morrer de várias maneiras, e uma das mais recentes e interessantes é chamada ferroptose — um tipo de dano às membranas celulares impulsionado por ferro, semelhante à “ferrugem”. Esse processo está agora associado a doenças que vão da lesão renal à neurodegeneração. O oligoelemento selênio, conhecido por muitos via suplementos alimentares, desempenha um papel central em impedir essa forma perigosa de morte celular. Este estudo investiga como um aminoácido comum que contém selênio, a selenometionina, pode proteger as células da ferroptose por meio de não apenas uma, mas duas estratégias protetoras distintas.
Um novo defensor encontrado em uma grande triagem de fármacos
Para encontrar pequenas moléculas capazes de bloquear a ferroptose, os pesquisadores rastrearam milhares de compostos de medicamentos aprovados pela FDA e produtos naturais. Eles usaram uma substância chamada RSL3 para desencadear ferroptose em linhagens de células cancerígenas humanas e monitoraram a morte celular e o acúmulo de lipídios oxidados danificados nas membranas. Entre todos os candidatos, a selenometionina destacou-se como um protetor potente: reduziu tanto o dano lipídico quanto a morte celular em diferentes tipos celulares e em dois modelos principais de ferroptose — um induzido pela inibição direta de GPX4 (com RSL3) e outro pela privação de cistina, um bloco de construção do antioxidante glutationa. Esses resultados posicionaram a selenometionina como um inibidor de ferroptose amplo e robusto. 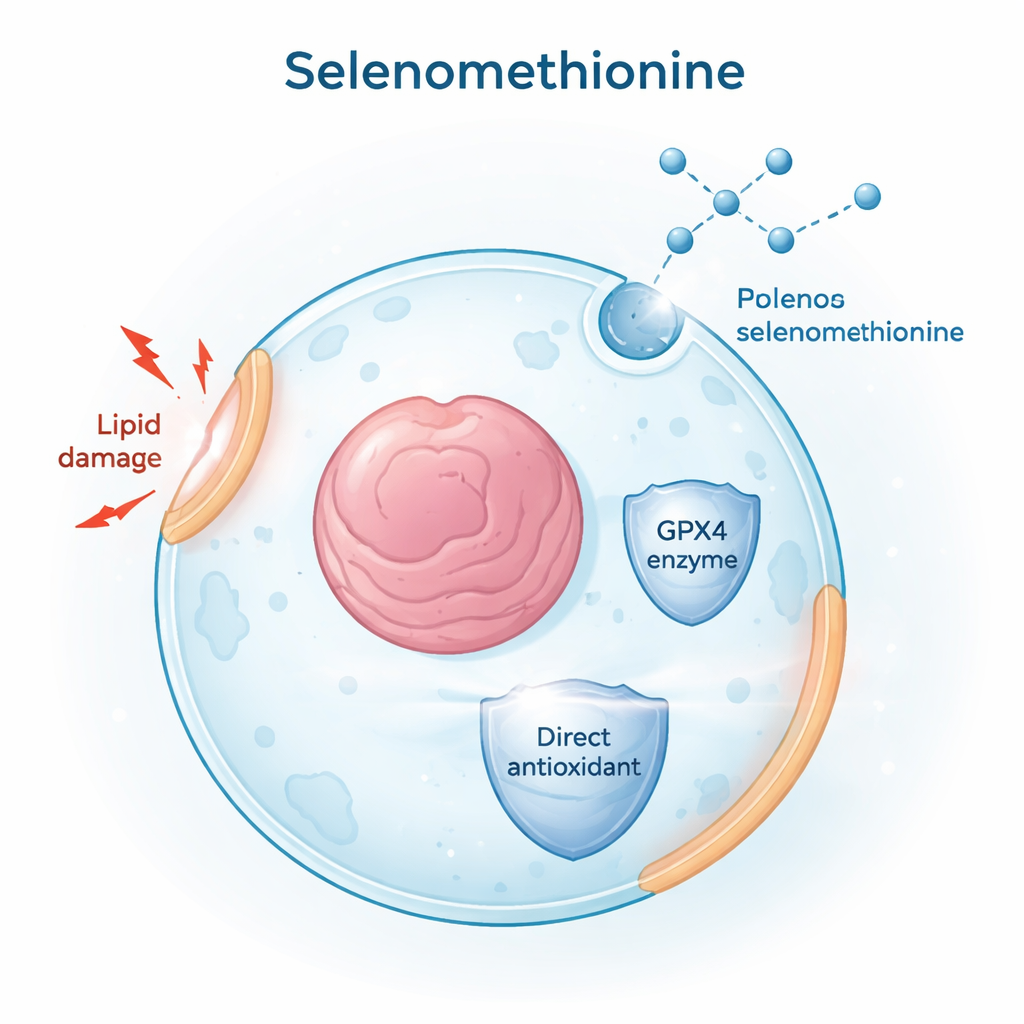
Suprimento de selênio para uma enzima protetora chave
Um escudo anti-ferroptose central nas células é uma enzima chamada GPX4, que depende do selênio para funcionar. O time buscou determinar se a selenometionina simplesmente alimenta essa via ou faz mais do que isso. Eles traçaram como o selênio proveniente da selenometionina pode ser convertido em formas adequadas para a síntese de GPX4, mesmo quando uma rota habitual, chamada via da transsulfuração, estava prejudicada ou bloqueada. Usando silenciamento genético e inibidores químicos de enzimas nessas vias enxofre–selênio, descobriram que a selenometionina ainda aumentava os níveis de GPX4 e protegia as células. Isso mostrou que as células podem recorrer a múltiplas rotas metabólicas para extrair selênio da selenometionina e manter a produção de GPX4, mesmo em tecidos onde a via clássica é fraca.
Proteção que não depende da enzima habitual
Surpreendentemente, quando os pesquisadores removeram completamente o GPX4 das células usando edição gênica CRISPR, a selenometionina continuou a proteger contra a ferroptose. Ainda reduzia o dano lipídico nas membranas e a morte celular, indicando que o GPX4 não explica todo o efeito. Experimentos adicionais sugeriram que parte dessa proteção envolve a incorporação da selenometionina em proteínas recém-sintetizadas, mas isso representa apenas parte do efeito. Os autores, então, focaram na reatividade química da própria selenometionina. Eles descobriram que ela pode neutralizar diretamente espécies reativas de oxigênio (ROS), incluindo peróxido de hidrogênio, sendo convertida em uma forma oxidada — um “sulfoxido”. A espectrometria de massa confirmou esse produto, e fornecer às células a versão sulfoxida também reduziu a ferroptose, o que implica que as células podem reciclá-la de volta à selenometionina ativa em um ciclo redox.
Da cultura celular à proteção renal em animais vivos
Para testar se esses mecanismos são relevantes em um organismo completo, o time recorreu a um modelo murino de lesão renal aguda causada pelo fármaco contra o câncer cisplatina, uma condição conhecida por envolver ferroptose. Camundongos tratados com cisplatina exibiram perda de peso, rim aumentado, função renal prejudicada e níveis elevados de marcadores de ferroptose. Quando os animais receberam selenometionina, muitos desses problemas melhoraram: o peso corporal recuperou, o aumento renal diminuiu, os parâmetros sanguíneos de função renal normalizaram, sinais inflamatórios caíram e marcadores químicos de dano lipídico reduziram. O tecido renal também mostrou níveis mais altos de GPX4 e menos lesões estruturais. Esses benefícios foram comparáveis aos observados com ferrostatina-1, um conhecido bloqueador experimental da ferroptose. 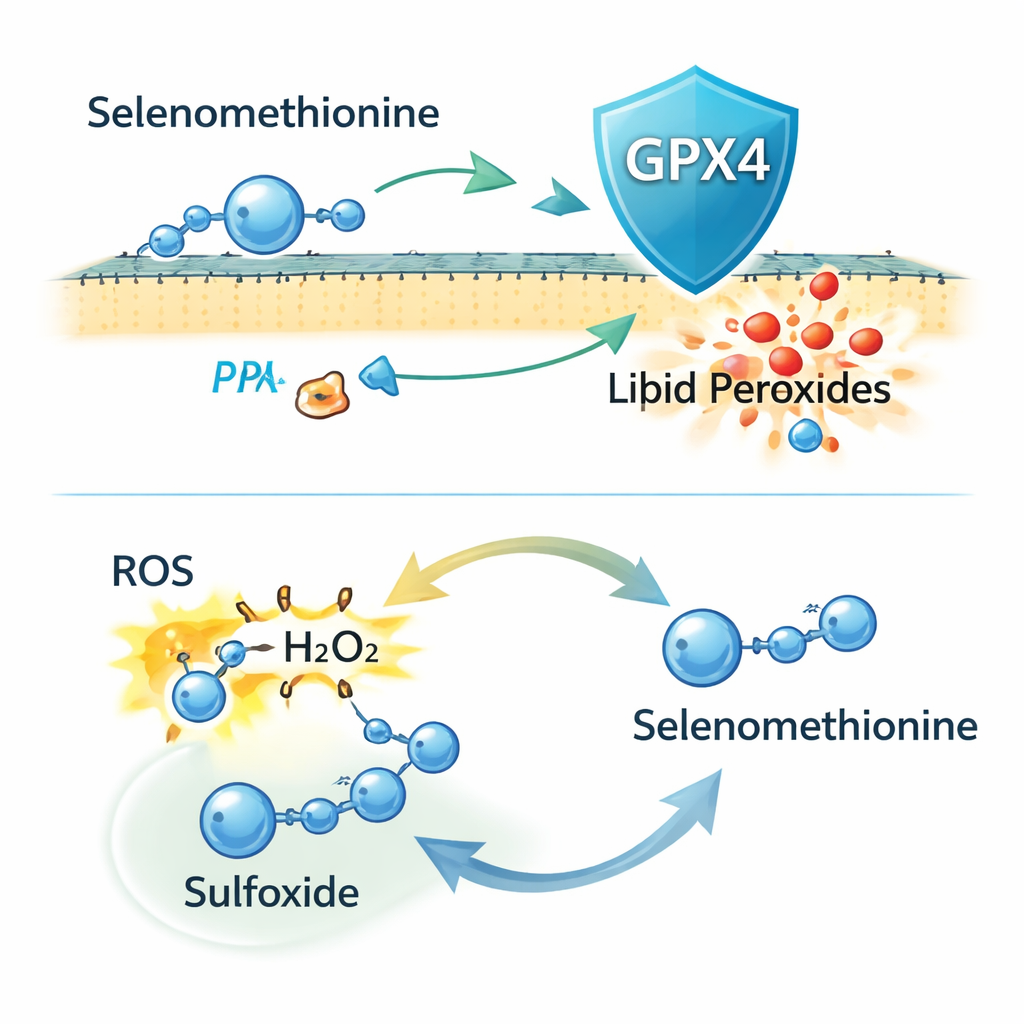
O que isso significa para terapias futuras
Em termos práticos, este trabalho sugere que a selenometionina atua como um extintor de incêndio de dupla função contra um “enferrujamento” das membranas celulares impulsionado por ferro. Por um lado, ela fornece selênio para que as células possam produzir mais da enzima GPX4, que funciona como uma equipe de limpeza interna para lipídios danificados. Por outro, a própria selenometionina pode neutralizar oxidantes nocivos e ser reciclada, oferecendo uma proteção de reserva independente do GPX4. Juntas, essas propriedades tornam a selenometionina uma candidata promissora para prevenir ou tratar doenças nas quais a ferroptose desempenha papel central, como danos renais induzidos por fármacos e, possivelmente, outras condições impulsionadas por estresse oxidativo descontrolado.
Citação: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Palavras-chave: ferroptose, selênio, selenomethionine, estresse oxidativo, lesão renal aguda