Clear Sky Science · pt
O componente da chaperonina TRiC, Cct3, é necessário para o transporte axonal, a mielinização e o refinamento da junção neuromuscular
Quando a fiação nervosa dá errado
Nossos cérebros e corpos dependem de fibras nervosas longas e semelhantes a cabos para transmitir sinais de forma rápida e confiável. Para desempenhar esse papel, muitos nervos são envoltos por mielina isolante, e suas terminações precisam formar contatos precisos com os músculos. Este artigo investiga o que acontece quando um “ajudante” celular crucial para o dobramento de proteínas, chamado Cct3, falha. Usando zebrafish e tecido humano, os autores mostram como esse único componente de uma grande máquina chaperona pode perturbar a mielina, as conexões nervo–músculo e o sistema de transporte interno que mantém os neurônios vivos e funcionais.
Um alfaiate celular para construir nervos
Dentro de cada célula, proteínas recém-sintetizadas devem ser dobradas nas formas corretas, muito parecido com ajustar cuidadosamente um terno. O complexo TRiC, que inclui a subunidade Cct3, é um dos principais “alfaiates”, ajudando cerca de 10% de todas as proteínas celulares — especialmente as proteínas estruturais actina e tubulina — a se dobrarem corretamente. Esses blocos de construção formam o arcabouço interno da célula e as trilhas ao longo das quais cargas vitais são movimentadas. Em pacientes portadores de versões defeituosas de CCT3 e genes relacionados, exames cerebrais revelam redução da matéria branca (a fiação rica em mielina do cérebro) e problemas nos nervos periféricos e músculos. Os autores buscaram entender como a perda de Cct3 atrapalha o desenvolvimento e a função nervosa.
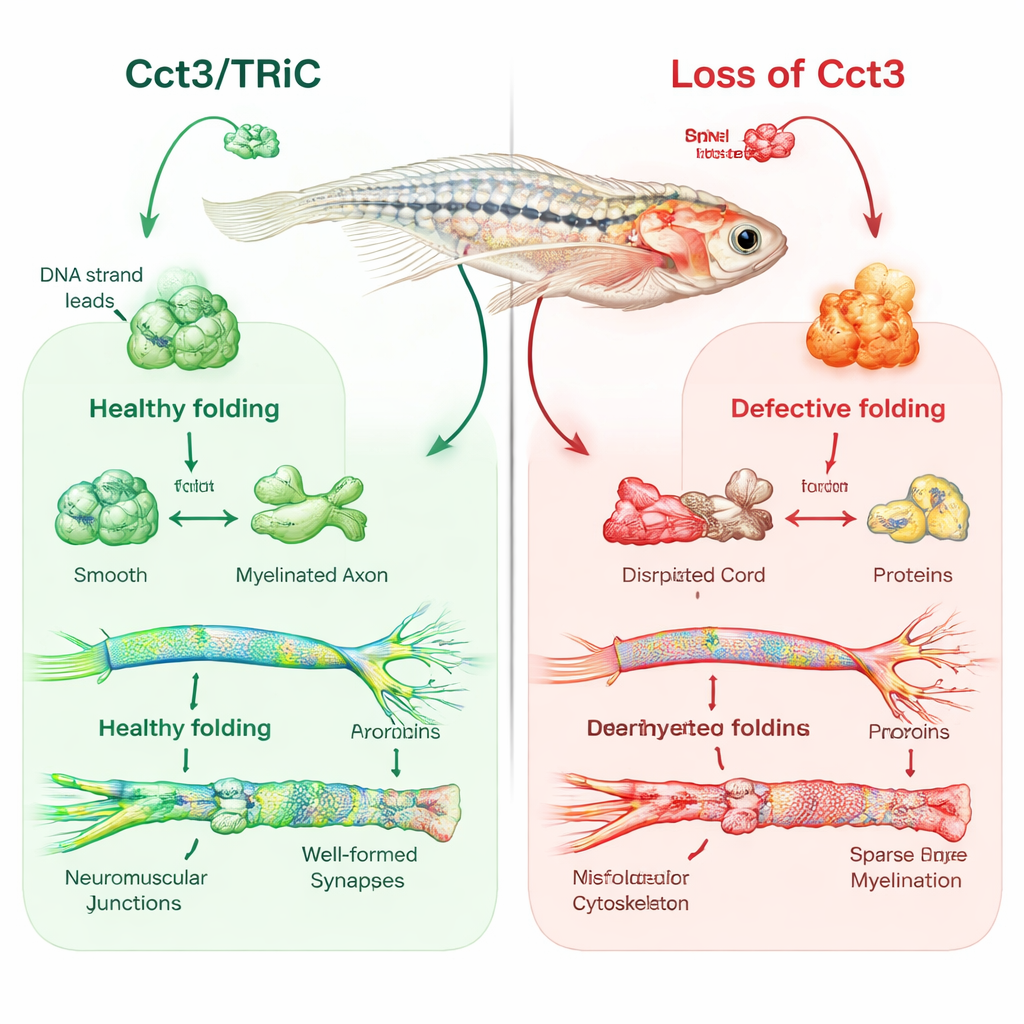
Zebrafish como janela para o isolamento nervoso
A equipe usou edição gênica CRISPR/Cas9 para criar zebrafish que carecem de cct3 funcional. Esses peixinhos apresentaram cérebros e olhos menores, acúmulo de fluido ao redor do coração, respostas táteis fracas e morreram em poucos dias. Quando os pesquisadores restabeleceram cct3 normal injetando seu RNA mensageiro, muitos desses defeitos melhoraram, confirmando que a perda de Cct3 era a causa principal. Focando na mielina, eles usaram marcadores fluorescentes e microscopia eletrônica para visualizar as camadas isolantes ao redor dos nervos. Em peixes normais, as células formadoras de mielina no cérebro e nos nervos periféricos envolviam axônios com bainhas ordenadas e em camadas até o quarto dia de desenvolvimento. Em contraste, os mutantes de cct3 tinham muito menos células mielinizadoras e praticamente nenhuma mielina adequada ao redor de muitos axônios, apesar de esses axônios aparentarem formato normal na superfície.
Células de suporte frágeis e ligações nervo–músculo tensionadas
Para descobrir por que a mielina estava ausente, os autores examinaram células de Schwann e células da crista neural relacionadas — as células de suporte que envolvem os nervos periféricos. Em peixes normais, essas células estendiam processos longos e finos e depois refinavam sua forma ao formar segmentos de mielina. Nos mutantes, elas se arredondaram, encurtaram seus processos e fragmentaram-se. Seus núcleos se desintegraram em um padrão típico de morte celular programada, e um marcador chave de morte (Caspase 3 ativada) apareceu, mostrando que muitas dessas células morriam precocemente. Enquanto isso, nas junções neuromusculares onde os nervos encontram o músculo, o padrão de “pontos quentes” de receptores nos músculos não se refinou. Em vez de muitos aglomerados pequenos e precisos, os mutantes exibiam menos manchas maiores de receptores, ecoando as dobras sinápticas simplificadas vistas em um paciente humano com mutação em CCT3.
Trilhas internas quebradas e tráfego de carga desacelerado
Como o TRiC ajuda a dobrar actina e tubulina, os autores analisaram de perto a estrutura interna dos axônios motores. Eles descobriram que os níveis gerais de tubulina estavam fortemente reduzidos nos mutantes, e o número de microtúbulos normais — os tubos ocos que funcionam como trilhas para o transporte — caiu dramaticamente tanto nos nervos centrais quanto nos periféricos. “Marcas” químicas na tubulina, importantes para microtúbulos estáveis e prontos para o transporte, também foram severamente alteradas. Usando imagem ao vivo de mitocôndrias e endossomos brilhantes dentro de axônios motores, observaram como essas cargas se moviam. Em peixes saudáveis, os orgânulos viajavam rapidamente e de forma direcional ao longo do axônio. Nos mutantes, muitos orgânulos paravam ou apenas oscilavam para frente e para trás, consistente com trilhas danificadas e transporte perturbado.
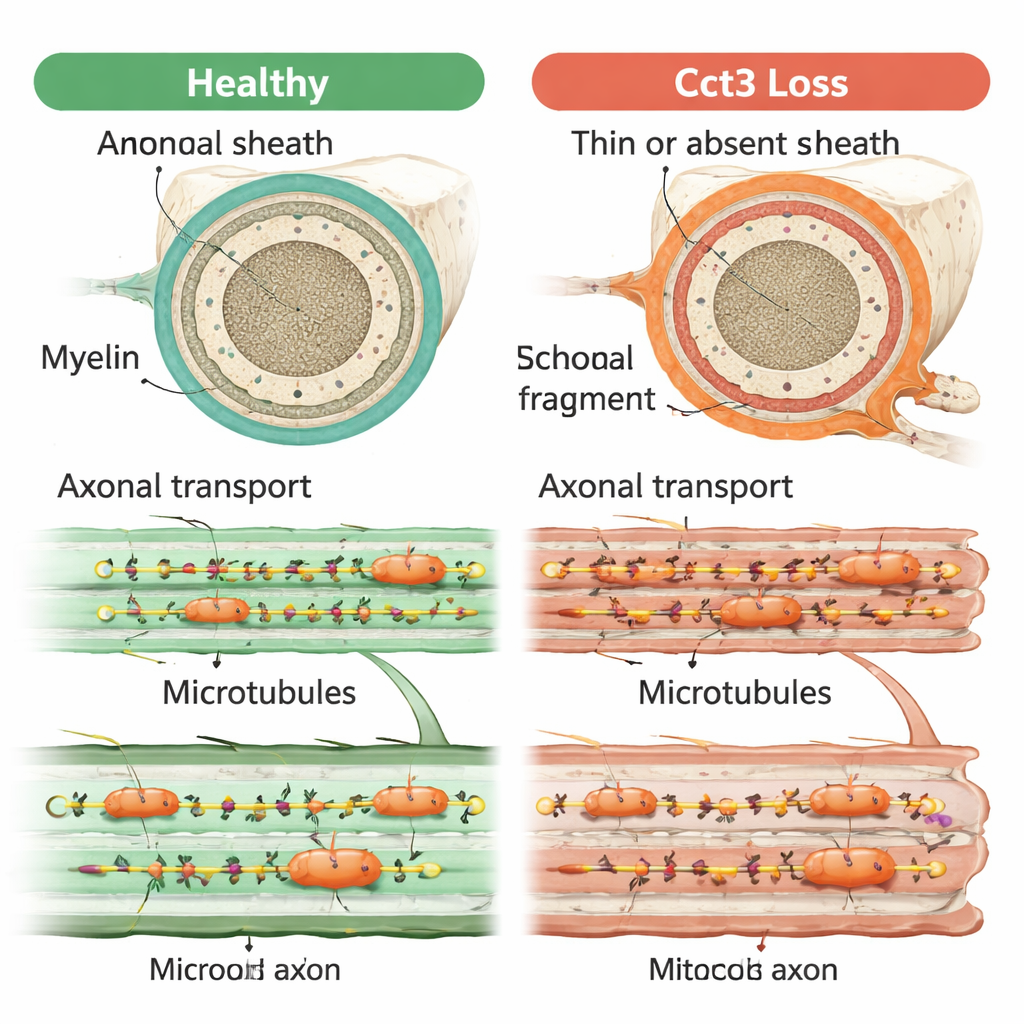
Um problema central por trás de muitos sintomas
Em conjunto, os achados mostram que Cct3 é essencial para vários aspectos interligados da saúde nervosa: ele sustenta a sobrevivência das células de suporte formadoras de mielina, permite o enrolamento adequado da mielina e possibilita que as junções neuromusculares em maturação sejam refinadas. Todas essas funções podem ser rastreadas até seu papel no dobramento e manutenção das proteínas que constroem o citoesqueleto e as trilhas de microtúbulos usadas para o transporte axonal. Quando essas trilhas falham, sinais e materiais essenciais não chegam aos locais corretos ao longo do nervo, provavelmente comprometendo tanto a comunicação com as células formadoras de mielina quanto o formato das conexões nervo–músculo. Este trabalho sugere que o transporte axonal prejudicado pode ser o fio condutor que liga os diversos problemas cerebrais e nervosos observados em distúrbios relacionados ao TRiC.
Citação: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Palavras-chave: mielinização, transporte axonal, junção neuromuscular, chaperonas moleculares, modelo em zebrafish