Clear Sky Science · pt
Tráfego e sinalização BDNF-TrkB prejudicados em neurônios do prosencéfalo basal na síndrome de Down
Por que este estudo cerebral importa
Pessoas com síndrome de Down vivem mais do que nunca, mas também enfrentam um risco muito elevado de desenvolver demência semelhante à Alzheimer ainda na meia-idade. Este estudo investiga o interior de células cerebrais individuais para entender por que certos neurônios são tão vulneráveis. Ao rastrear como essas células movem-se e respondem a uma molécula-chave que funciona como “fertilizante” cerebral, os pesquisadores revelam um engarrafamento de tráfego dentro dos neurônios que pode ajudar a explicar a perda de memória e apontar para novas estratégias terapêuticas.
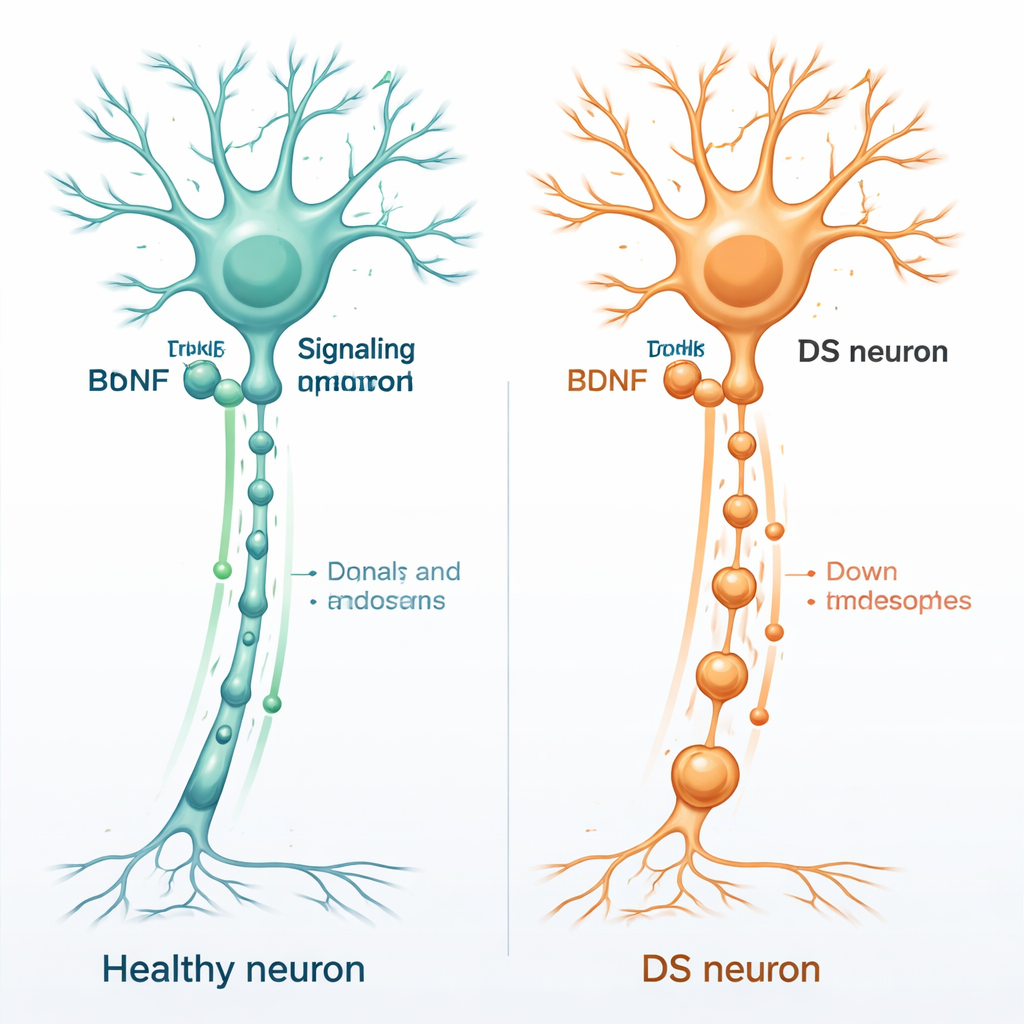
Fertilizante cerebral e saúde dos neurônios
Neurônios saudáveis dependem de um conjunto de moléculas de suporte chamadas neurotrofinas, que atuam como fertilizante para as células nervosas. Uma das mais importantes é o fator neurotrófico derivado do cérebro, ou BDNF. O BDNF liga-se a uma proteína de ancoragem nos neurônios chamada TrkB, geralmente nas extremidades distais das fibras nervosas. Depois que o BDNF se liga, todo o complexo BDNF–TrkB é internalizado em pequenas vesículas de membrana e transportado de volta ao longo da longa fibra nervosa até o corpo celular. Essas vesículas em movimento, conhecidas como endossomos de sinalização, informam ao núcleo quais genes ativar para manter o neurônio vivo, conectado e adaptável.
Quando os contêineres celulares de carga crescem demais
A equipe concentrou-se nos neurônios do prosencéfalo basal, um grupo de células que apoia fortemente a memória e a atenção e está entre os primeiros a degenerar tanto na síndrome de Down quanto na doença de Alzheimer. Usando um modelo murino da síndrome de Down chamado Dp1Tyb, eles marcaram neurônios com um marcador de endossomos precoces e os compararam com neurônios normais. Os neurônios da síndrome de Down continham muito mais endossomos precoces que tinham mais de 50% maiores do que o habitual. Essas estruturas são controladas por Rab5, um interruptor molecular que ajuda a formar e classificar esses “contêineres de carga” internos. Os pesquisadores encontraram Rab5 preso em um estado hiperativo nos neurônios da síndrome de Down, mesmo antes da estimulação por BDNF, o que sugere que o sistema endossomal já estava em sobrecarga.
Engarrafamentos ao longo da fibra nervosa
Em seguida, os cientistas perguntaram se essa paisagem interna distorcida atrapalhava o movimento dos sinais do BDNF. Eles cultivaram neurônios em dispositivos microfluídicos que separam os corpos celulares das terminações axonais, permitindo estimular apenas as pontas dos axônios. Ao seguir traçadores fluorescentes inofensivos que compartilham a mesma rota de transporte que os complexos BDNF–TrkB, mediram quão rápido os endossomos de sinalização viajavam de volta em direção aos corpos celulares. Em neurônios normais, a adição de BDNF tornou os endossomos cerca de 30% mais rápidos e com menos pausas, refletindo uma resposta robusta aos sinais de crescimento. Nos neurônios da síndrome de Down, porém, o BDNF não conseguiu acelerar o transporte nem reduzir as pausas. Um experimento separado que rastreou receptores TrkB reais confirmou que menos deles alcançaram com sucesso o corpo celular nas células da síndrome de Down.
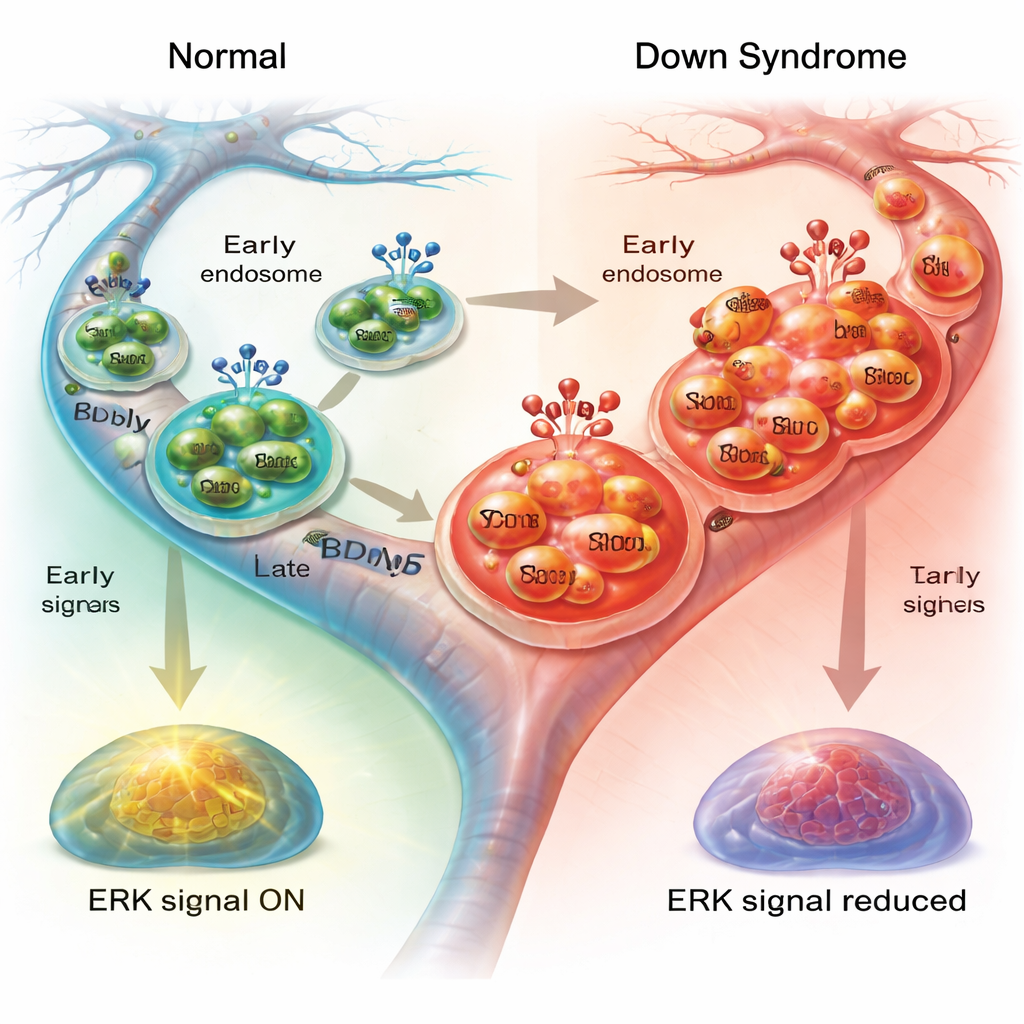
Sinais a jusante atenuados dentro da célula
Para que essas vesículas em trânsito sustentem a saúde neuronal, elas devem ativar vias de sinalização internas ao chegar ao destino. Uma rota-chave envolve ERK1/2, um par de enzimas que retransmitem a mensagem do BDNF ao núcleo e ajudam a regular o esqueleto celular e a maquinaria de transporte. Quando os pesquisadores mediram ERK1/2 ativado após o tratamento com BDNF, encontraram um aumento claro em neurônios normais, mas uma resposta muito mais fraca nos neurônios da síndrome de Down, especialmente nos axônios. Bloquear ERK1/2 em neurônios saudáveis reproduziu parcialmente o transporte lento observado nas células com síndrome de Down, desacelerando os endossomos e aumentando as pausas. Em contraste, o bloqueio de ERK1/2 teve pouco efeito adicional nos neurônios da síndrome de Down, consistente com uma sinalização que já estava atenuada.
O que isso significa para o envelhecimento cerebral na síndrome de Down
Em conjunto, os achados sugerem um problema autorreforçador em neurônios vulneráveis: Rab5 está hiperativo, os endossomos precoces incham e os complexos BDNF–TrkB ficam presos em compartimentos que não se movem eficientemente. Como resultado, menos sinais de crescimento alcançam o corpo celular, a sinalização via ERK1/2 é enfraquecida e a maquinaria que impulsiona o transporte de longa distância fica ainda mais comprometida. Ao longo dos anos, esse sistema de comunicação defeituoso pode contribuir para a perda precoce e grave dos neurônios do prosencéfalo basal observada na doença de Alzheimer relacionada à síndrome de Down. Ao destacar essa ligação entre o “controle de tráfego” endossomal e a sinalização por fatores de crescimento, o estudo aponta para novas ideias terapêuticas que visam normalizar a atividade de Rab5, restaurar a função dos endossomos e fortalecer as respostas ao BDNF para ajudar a proteger esses neurônios críticos.
Citação: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Palavras-chave: Síndrome de Down, Doença de Alzheimer, BDNF, transporte axonal, endossomos