Clear Sky Science · pt
Desubiquitinação de Hexocinase 2 mediada por USP30 controla o destino metabólico da glicose e a progressão tumoral
Como as Células Cancerígenas Reprogramam o Uso do Açúcar
As células cancerígenas são célebres pelo seu “apetite por açúcar”: elas queimam glicose de maneiras incomuns para sustentar crescimento rápido. Este estudo revela um novo botão de controle, uma proteína chamada USP30, que ajuda as células tumorais a decidir como usar a glicose. Ao ajustar outra proteína, a hexocinase 2 (HK2), o USP30 pode empurrar as células cancerígenas a queimar mais açúcar e crescer mais depressa, apontando para um alvo promissor para futuros fármacos anticâncer. 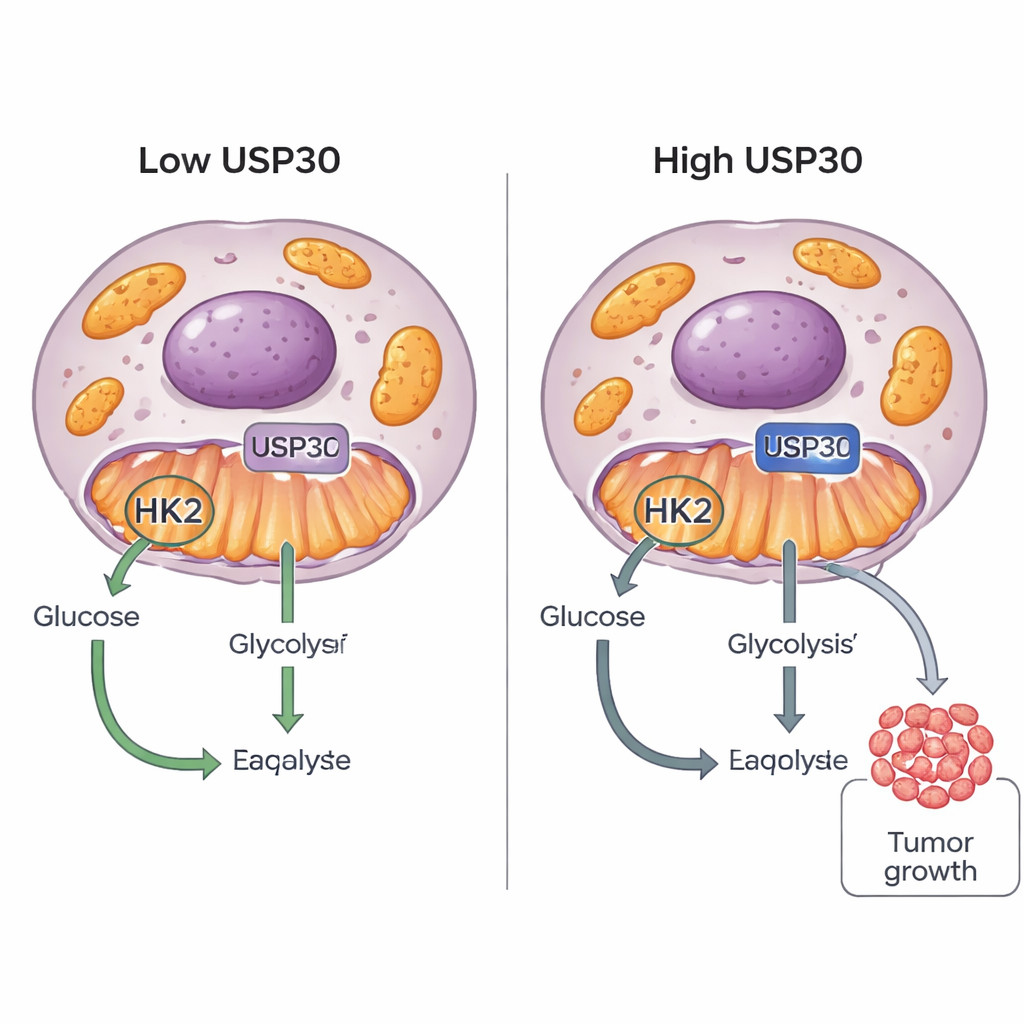
Um Estilo de Vida Faminto por Açúcar Dentro dos Tumores
A maioria das células saudáveis extrai energia dos nutrientes de forma eficiente, mas muitas células cancerosas preferem uma via rápida e menos eficiente chamada glicólise aeróbica, também conhecida como efeito Warburg. Elas captam grandes quantidades de glicose e a convertem rapidamente em lactato, mesmo quando há oxigênio disponível. Essa estratégia faz mais do que gerar energia: fornece blocos de construção para DNA, lipídios e proteínas, ajuda os tumores a resistir ao estresse e pode até enfraquecer ataques do sistema imune. Na entrada dessa via está a hexocinase, uma enzima que adiciona um grupo fosfato à glicose que entra, comprometendo-a com uma rota de degradação e química que sustenta o crescimento.
Uma Enzima Mitocondrial Entra em Cena
USP30 é uma enzima localizada na superfície externa das mitocôndrias, as usinas de energia da célula. Ela pertence a uma família de “desubiquitinases” que removem pequenas marcas protéicas chamadas ubiquitina de outras proteínas, frequentemente alterando sua estabilidade, localização ou atividade. O USP30 já era conhecido por funções em células cerebrais e no controle da qualidade mitocondrial, mas seu impacto no câncer era incerto. Ao explorar grandes bancos de dados genômicos de câncer, os pesquisadores notaram que tumores com níveis mais altos de USP30 tendiam a mostrar assinaturas mais fortes de queima de glicose e mais fracas de oxidação de lipídios, sugerindo que o USP30 poderia ajudar os cânceres a se deslocarem rumo a um estilo de vida alimentado por açúcar.
Conectando o USP30 aos Guardiões do Açúcar da Célula
Para sondar essa ligação, a equipe reduziu ou eliminou o USP30 em várias linhagens celulares cancerosas e mediu como elas processavam energia. Usando instrumentos que acompanham em tempo real a produção de ácido e o consumo de oxigênio, eles descobriram que a perda de USP30 reduziu bruscamente tanto a glicólise quanto a respiração mitocondrial. A produção de lactato e o consumo de glicose diminuíram, indicando que o motor de queima de açúcar das células havia desacelerado. Uma série de experimentos de espectrometria de massa revelou então que o USP30 interage fisicamente com várias enzimas ligadas ao metabolismo da glicose, especialmente as hexocinases HK1 e HK2. Testes complementares mostraram que essa interação depende da atividade catalítica do USP30 e ocorre de forma direta, não apenas por parceiros indiretos.
Uma Alavanca Molecular Precisa sobre a Hexocinase 2
Aprofundando-se, os pesquisadores descobriram que o USP30 remove tipos específicos de cadeias de ubiquitina — chamadas ligações atípicas — de HK1 e HK2. No caso da HK2, essa edição ocorre em um único aminoácido crucial, a lisina 144 (K144). Quando K144 é mutada de modo que não possa mais carregar ubiquitina, a HK2 se torna mais estável, se liga com mais afinidade a uma proteína de canal chamada VDAC1 nas mitocôndrias e apresenta maior atividade enzimática. Células geneticamente modificadas para portar essa alteração K144 levaram mais HK2 para as mitocôndrias, queimaram mais glicose, liberaram mais lactato e exibiram crescimento e migração mais rápidos em cultura. Em camundongos, tumores originados de células com a HK2 mutante K144 cresceram maiores e mais rápidos do que aqueles com HK2 normal, reforçando o impacto desse pequeno interruptor molecular. 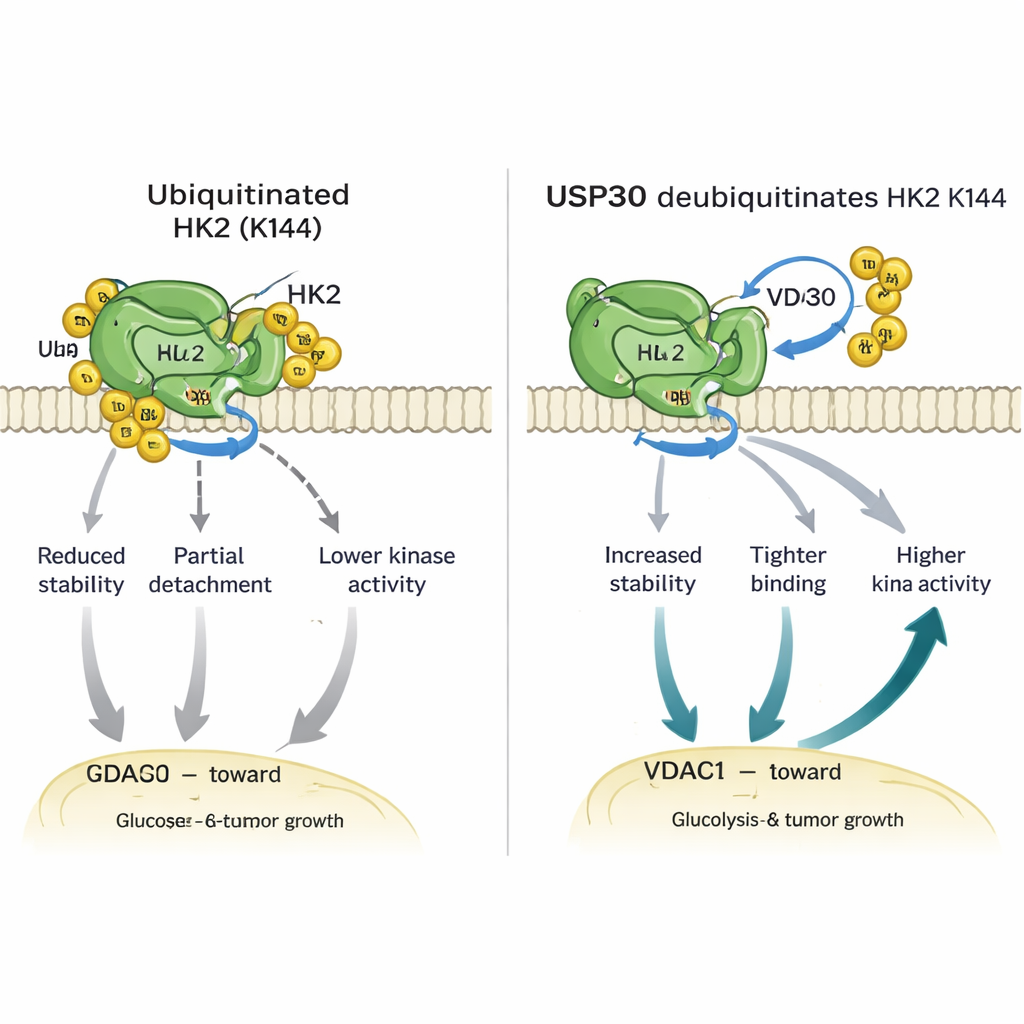
Transformando um Interruptor Metabólico em Vantagem de Crescimento
Esses resultados traçam uma cadeia clara de eventos: o USP30 se liga à HK2, remove as marcas de ubiquitina de K144 e, ao fazê-lo, mantém a HK2 ativa e ancorada às mitocôndrias. Isso aumenta a glicólise, alimenta a divisão e a migração das células tumorais e, em última instância, acelera o crescimento tumoral. Quando o USP30 está ausente ou inativo, a HK2 torna-se menos estável e menos eficaz, e as células cancerosas perdem parte de sua vantagem metabólica. Em termos leigos, o USP30 age como um mecânico que mantém o motor de açúcar da célula cancerosa afinado e fixo — retire o mecânico, e o motor falha.
O Que Isso Significa para Tratamentos Futuros do Câncer
Para um público não especializado, a conclusão principal é que as células cancerosas dependem de um controle fino sobre como queimam açúcar, e o USP30 é um botão recém-descoberto nesse painel de controle. Ao estabilizar a HK2 em um sítio específico, o USP30 ajuda os tumores a manter um metabolismo guloso por glicose e a crescer de forma mais agressiva. Drogas que bloqueiem o USP30, ou que perturbem sua ligação à HK2 na lisina 144, poderiam enfraquecer tumores ao privá-los do motor de açúcar sem necessariamente prejudicar tanto as células normais. Este trabalho, portanto, acrescenta uma peça importante ao quebra-cabeça de como o câncer redesenha o metabolismo e sugere um ângulo promissor para terapias direcionadas.
Citação: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Palavras-chave: metabolismo do câncer, glicólise, hexocinase 2, USP30, efeito Warburg