Clear Sky Science · pt
Knockout específico em oócitos das subunidades de eIF2 causa apoptose de oócitos de camundongo em folículos em início de crescimento via disfunções mitocondriais e dano ao DNA
Por que a vida das células-ovo importa
Mulheres nascem com todas as células-ovo que terão ao longo da vida, armazenadas dentro de pequenas estruturas no ovário chamadas folículos. Quando esses folículos são perdidos rápido demais, pode surgir insuficiência ovariana prematura (IOP), condição que leva à infertilidade precoce e frequentemente a sintomas semelhantes à menopausa em idade jovem. Este estudo em camundongos investiga uma questão básica, porém crucial: o que acontece dentro das células-ovo quando uma etapa chave na fabricação de novas proteínas falha, e como isso pode levar à perda precoce da fertilidade?
O interruptor inicial da produção de proteínas da célula
Para se manterem saudáveis, as células-ovo precisam constantemente produzir as proteínas certas no momento certo. Uma parte central desse processo é uma máquina molecular de três componentes chamada eIF2, que ajuda a iniciar a produção de proteínas a partir das mensagens genéticas. Os pesquisadores desativaram seletivamente duas das partes do eIF2, chamadas eIF2α e eIF2β, apenas em oócitos de camundongos nos estágios iniciais de crescimento folicular. Quando qualquer uma das subunidades estava ausente, as fêmeas se tornaram completamente inférteis. Seus ovários eram menores e a progressão normal de folículos iniciais para folículos maduros e ovulatórios ficou amplamente estagnada, com muito menos folículos em cada estágio subsequente. Com o tempo, praticamente todos os folículos foram esgotados, mimetizando uma condição grave de IO P de início precoce.
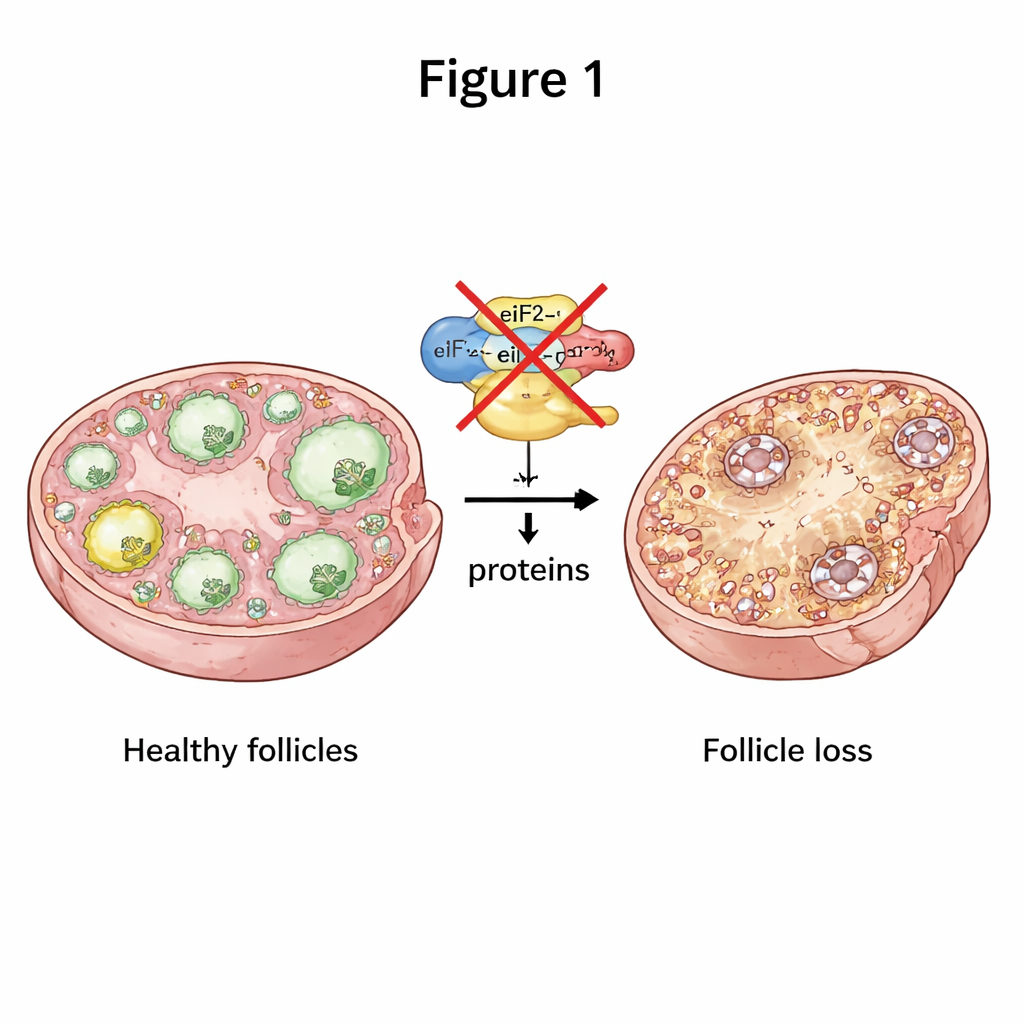
Quando a comunicação no ovário se rompe
Folículos não são apenas células-ovo isoladas; são parcerias estreitas entre o óvulo e células “auxiliares” ao redor chamadas células da granulosa. A equipe constatou que, sem eIF2β, os oócitos produziram muito menos de várias proteínas de sinalização cruciais que normalmente sustentam o crescimento das células da granulosa e a entrega de nutrientes. As pontes físicas entre oócito e células da granulosa estavam desorganizadas e encurtadas, e as microvilosidades da superfície do óvulo pareciam atrofiadas e danificadas no microscópio eletrônico. As células da granulosa nesses folículos proliferaram menos e morreram com mais frequência. Essa ruptura na comunicação bidirecional impediu o crescimento adequado dos folículos, empurrando o ovário rumo à perda folicular.
Falha de energia nas "baterias" do oócito
Mitocôndrias, frequentemente chamadas de usinas de energia da célula, são especialmente importantes em oócitos porque fornecem a energia necessária para o crescimento e o desenvolvimento embrionário posterior. Em oócitos deficientes em eIF2β, a taxa geral de produção de novas proteínas caiu e muitas proteínas relacionadas às mitocôndrias foram reduzidas. As mitocôndrias tornaram-se anormalmente longas, agrupadas perto da superfície celular, e mostraram potencial de membrana reduzido, níveis menores de energia (ATP) e menos cópias de DNA mitocondrial. Ao mesmo tempo, as células acumularam altos níveis de espécies reativas de oxigênio (ROS), moléculas agressivas baseadas em oxigênio que podem danificar componentes celulares. Juntas, essas alterações revelaram um colapso profundo na dinâmica e na função mitocondrial.
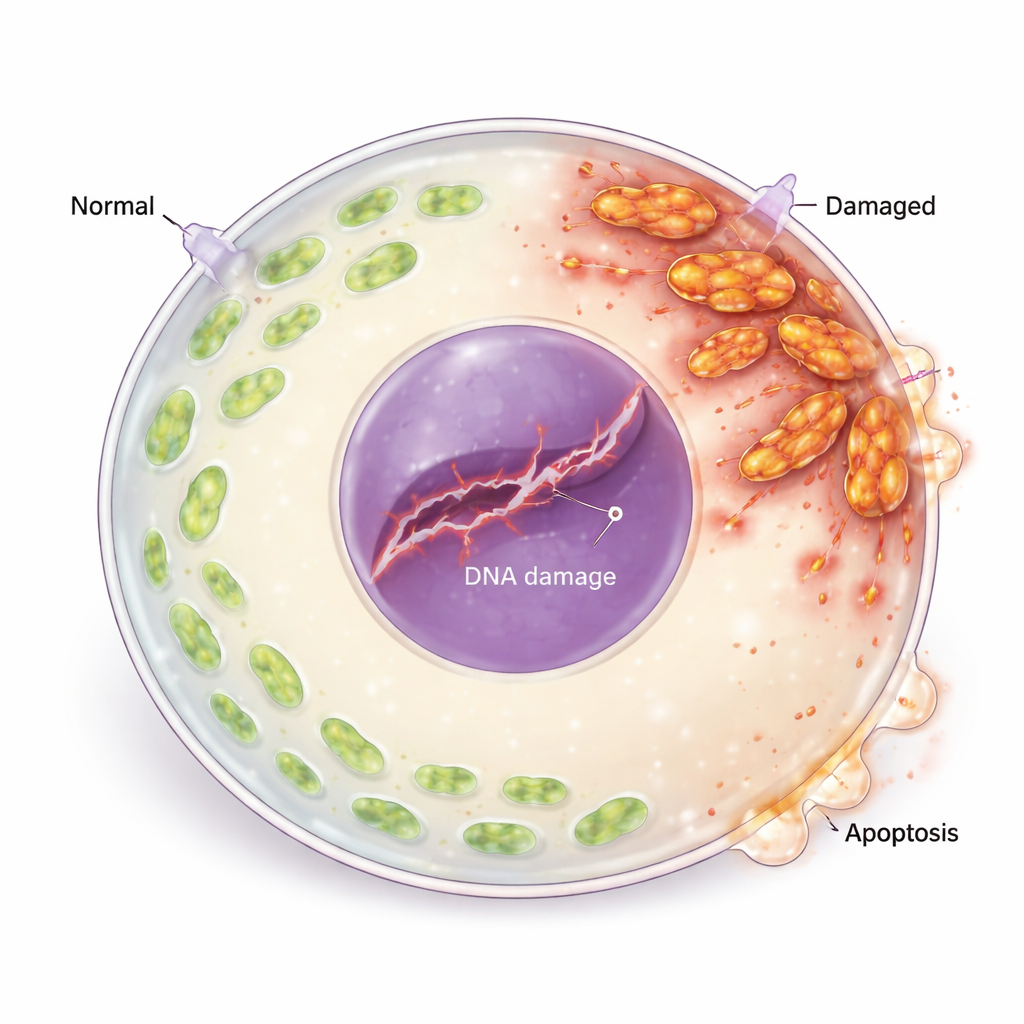
Do estresse oxidativo ao dano ao DNA e à morte celular
O excesso de ROS não prejudicou apenas as mitocôndrias; também lesionou o material genético do oócito. Os pesquisadores observaram aumento de marcadores de quebras na fita de DNA e ativação da maquinaria de resposta ao dano do DNA da célula, incluindo proteínas que detectam e sinalizam lesões genéticas. Uma proteína de reparo chave estava reduzida, sugerindo que o dano não estava sendo eficientemente reparado. A jusante, o equilíbrio entre reguladores de vida e morte mudou: proteínas pró-morte aumentaram enquanto proteínas protetoras diminuíram, e os oócitos exibiram sinais claros de morte celular programada (apoptose). Quando a equipe tratou os oócitos com um antioxidante (N-acetilcisteína), os níveis de ROS caíram, os marcadores de dano ao DNA e de apoptose diminuíram, e a maturação dos óvulos melhorou, ligando diretamente o estresse oxidativo à perda de oócitos.
O que isso significa para a falência ovariana precoce
Ao acompanhar os eventos desde um único complexo molecular (eIF2) até produção proteica defeituosa, colapso mitocondrial, estresse oxidativo, dano ao DNA e, finalmente, morte das células-ovo, este trabalho delineia uma cadeia detalhada de eventos que pode destruir a reserva ovariana. O estudo reforça a ideia de que mutações em fatores iniciadores da tradução, já observadas em algumas mulheres com IOP, podem diretamente prejudicar os oócitos por essa via. Também aponta para maneiras potenciais de intervenção: antioxidantes, moduladores da resposta ao estresse ou tratamentos que protejam folículos precoces (como o hormônio anti-Mülleriano, que preservou parcialmente folículos dormentes nesses camundongos) podem, um dia, apoiar a fertilidade em pacientes cujos ovários são vulneráveis a estresses similares.
Citação: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Palavras-chave: insuficiência ovariana prematura, apoptose de oócito, disfunção mitocondrial, tradução proteica, espécies reativas de oxigênio