Clear Sky Science · pt
Transglutaminase 2 agrava a sobrevivência do câncer de ovário ao inativar diretamente a GSK3β
Por que esta pesquisa importa para a saúde das mulheres
O câncer de ovário é um dos mais letais entre as mulheres porque costuma ser detectado tardiamente e frequentemente retorna mesmo após quimioterapia intensa. Este estudo revela como uma proteína pouco conhecida, a transglutaminase 2 (TGase 2), ajuda as células do câncer de ovário a sobreviver ao tratamento e a se espalhar pelo corpo. Ao expor essa ajudante oculta do câncer, o trabalho aponta para novas maneiras de tornar drogas existentes mais eficazes e de retardar ou impedir metástases letais.
Um motor oculto dentro de tumores agressivos
Médicos há muito observam que muitos cânceres de ovário desenvolvem resistência à quimioterapia e se disseminam amplamente na cavidade abdominal. Um culpado importante é um processo chamado transição epitélio–mesenquimal (EMT), no qual as células cancerosas afrouxam suas conexões, tornam-se mais móveis e passam a se comportar mais como “viajantes” invasivos do que como células organizadas de tecido. Os autores mostram que a TGase 2, que está em níveis muito baixos no ovário normal, mas muito mais alta nos tumores ovarianos, está fortemente associada a essa mudança. Em um grande painel de amostras humanas, os níveis de TGase 2 aumentaram de forma constante desde tumores em estágio inicial até doença avançada e metastática, e sua abundância acompanhou de perto a atividade de muitos genes relacionados à EMT que controlam movimento celular, crescimento e formação de vasos sanguíneos. 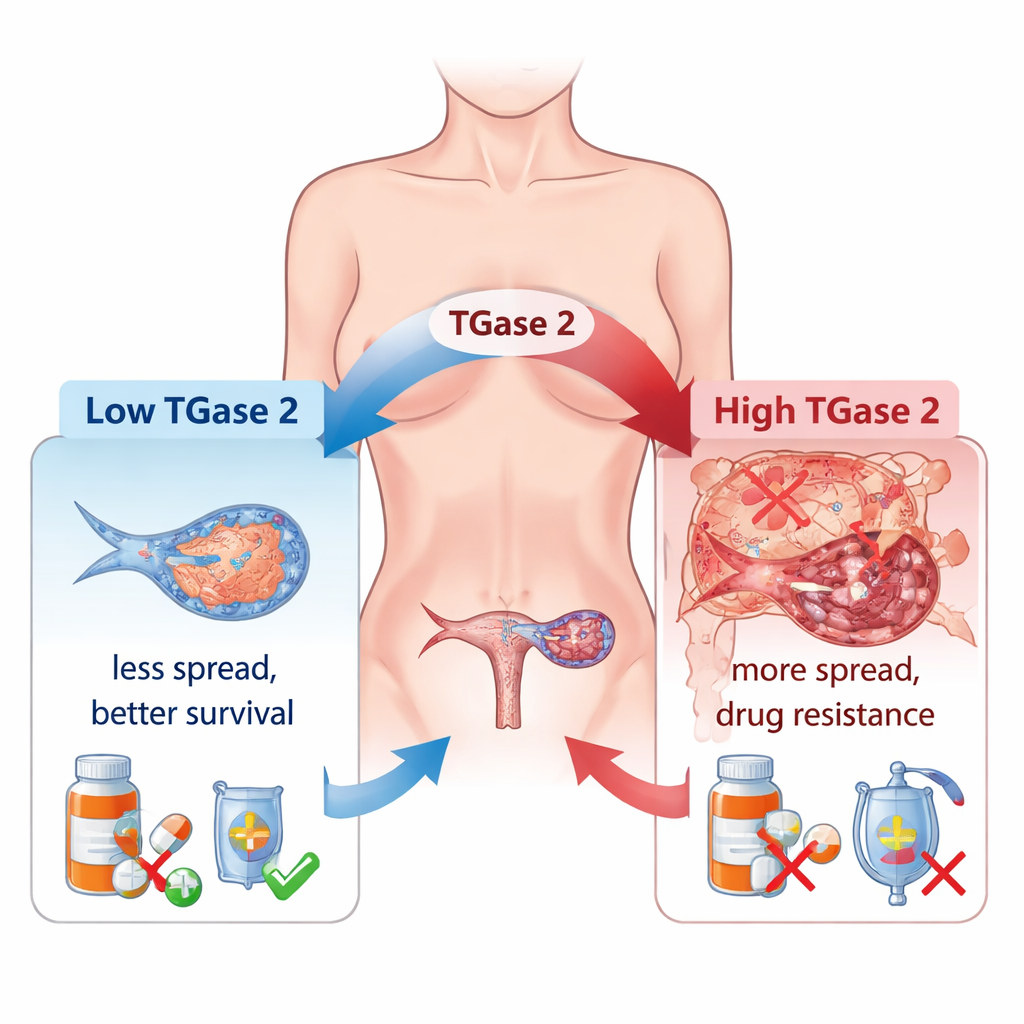
Como a TGase 2 desliga um interruptor de segurança chave
Para entender o que a TGase 2 realmente faz dentro das células cancerosas, os pesquisadores focaram sua relação com outra proteína, a GSK3β. Em condições saudáveis, a GSK3β funciona como um freio à invasão: mantém baixos os níveis de uma molécula de sinalização chamada β-catenina, que por sua vez reprime genes que promovem a EMT. A equipe descobriu que a TGase 2 se liga fisicamente à GSK3β e tanto enfraquece sua atividade quanto facilita seu envio para destruição pelo sistema de reciclagem da célula, uma via chamada autofagia. Quando a TGase 2 era abundante, as células de câncer de ovário migravam mais facilmente e apresentavam níveis maiores de marcadores clássicos de EMT, como fibronectina, vimentina e β-catenina. Quando os pesquisadores reduziram a TGase 2 com ferramentas genéticas, essas características invasivas caíram e a sinalização de β-catenina foi atenuada, mostrando que a TGase 2 desativa um interruptor de segurança crucial contra a metástase.
Das células cancerosas a animais vivos
A equipe perguntou a seguir se bloquear a TGase 2 poderia realmente retardar o câncer em animais. Eles criaram células de câncer de ovário sem o gene da TGase 2 e as implantaram em camundongos. Em comparação com camundongos que receberam células cancerosas normais, os animais que receberam células deficientes em TGase 2 desenvolveram menor carga tumoral e viveram mais tempo. Em um modelo separado que imita a disseminação do câncer pela corrente sanguínea, camundongos injetados com células deficientes em TGase 2 desenvolveram muito menos e menores metástases pulmonares. Importante, esses focos metastáticos mostraram níveis mais altos de GSK3β, em concordância com a ideia de que remover a TGase 2 restaura o freio natural contra a invasão e ajuda a conter a doença.
Transformando uma pista de laboratório em estratégia medicamentosa
Como deletar um gene não é prático em pacientes, os autores testaram uma pequena molécula chamada estreptonigrina, conhecida por se ligar à mesma extremidade da TGase 2 usada para agarrar outras proteínas. Eles descobriram que a estreptonigrina podia interromper a interação TGase 2–GSK3β nas células, reduzir sua colocalização e limitar a migração das células cancerosas. Em modelos murinos de câncer de ovário, o tratamento oral com estreptonigrina retardou o crescimento tumoral, encolheu lesões metastáticas e prolongou a sobrevivência. Mais impressionante, quando a estreptonigrina foi combinada com quimioterápicos padrão como cisplatina ou paclitaxel, os camundongos viveram semanas a mais do que com a quimioterapia isolada. A quimioterapia por si só tendia a elevar os níveis de TGase 2 e reduzir a GSK3β, empurrando indiretamente as células rumo à EMT, mas adicionar o bloqueador de TGase 2 reverteu essa tendência e conteve a nova mobilidade das células. 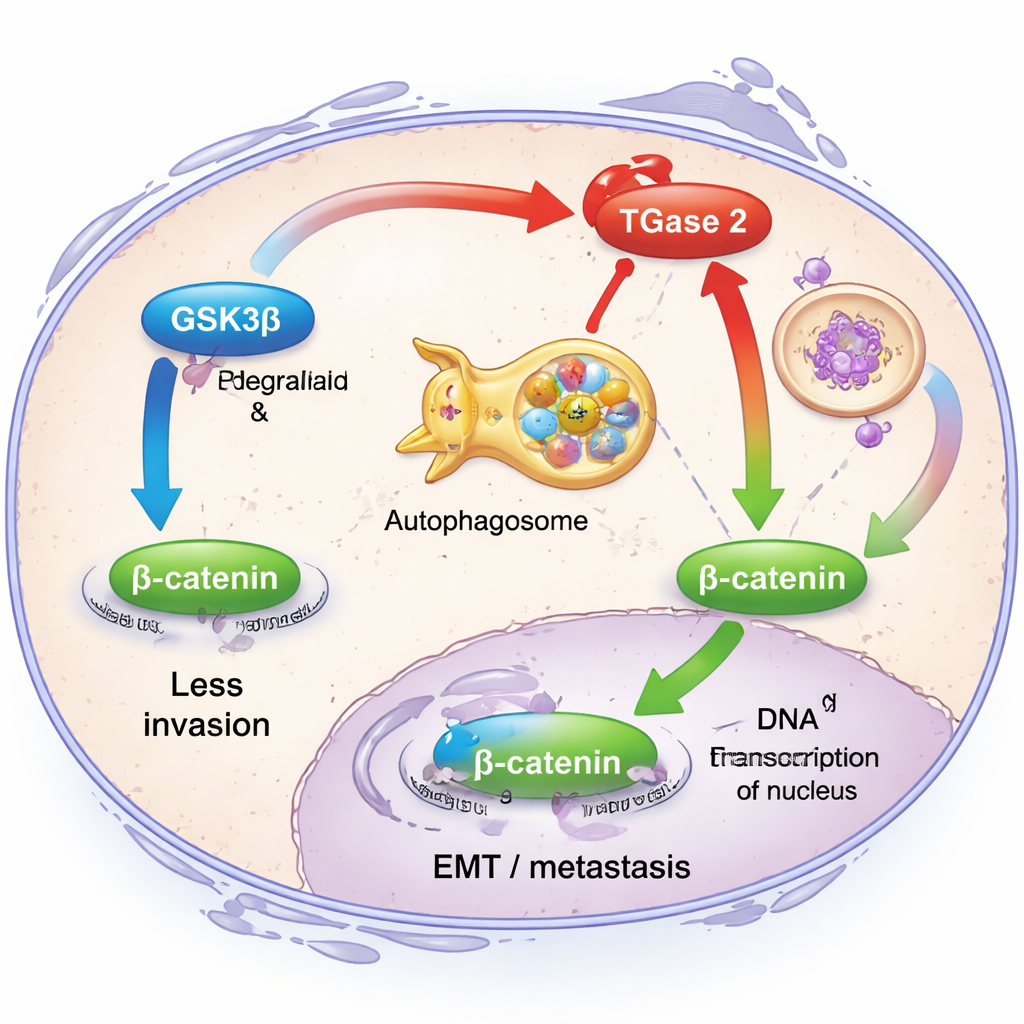
O que isso pode significar para tratamentos futuros
Para um público não especializado, a mensagem principal é que as células do câncer de ovário exploram a TGase 2 para desligar um freio antimetástase embutido e resistir à tempestade da quimioterapia. Ao inativar diretamente a GSK3β e estabilizar a β-catenina, a TGase 2 ajuda os tumores a se tornarem mais invasivos e resistentes a drogas. Este trabalho sugere que fármacos direcionados à região N-terminal da TGase 2 — como a estreptonigrina ou futuros compostos mais seguros modelados a partir dela — poderiam tornar as quimioterapias existentes mais eficazes, reduzir a chance de recaída e melhorar a sobrevida. Em termos simples, direcionar a TGase 2 pode fechar uma “rota de fuga” do câncer, mantendo os tumores de ovário mais sensíveis ao tratamento e menos capazes de se espalhar.
Citação: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Palavras-chave: câncer de ovário, resistência a medicamentos, metástase, transição epitélio-mesenquimal, terapia direcionada