Clear Sky Science · pt
Inibição da internalização do receptor de célula B (BCR) induzida por autoantígeno como estratégia terapêutica no linfoma difuso de grandes células B (LDGCB)
Por que isso importa para os pacientes
O linfoma difuso de grandes células B (LDGCB) é o câncer sanguíneo de crescimento rápido mais comum em adultos, e muitos pacientes ainda têm recidiva após a quimioimunoterapia padrão. Este estudo explora uma vulnerabilidade surpreendente em um grande subconjunto desses tumores: a dependência de uma antena na superfície celular chamada receptor de célula B (BCR). Ao mostrar que bloquear a forma como essa antena é internalizada pode prejudicar a sobrevivência das células cancerosas, o trabalho abre caminho para redestinar medicamentos anti‑náusea e antipsicóticos usados há muito tempo como auxiliares direcionados contra o linfoma.
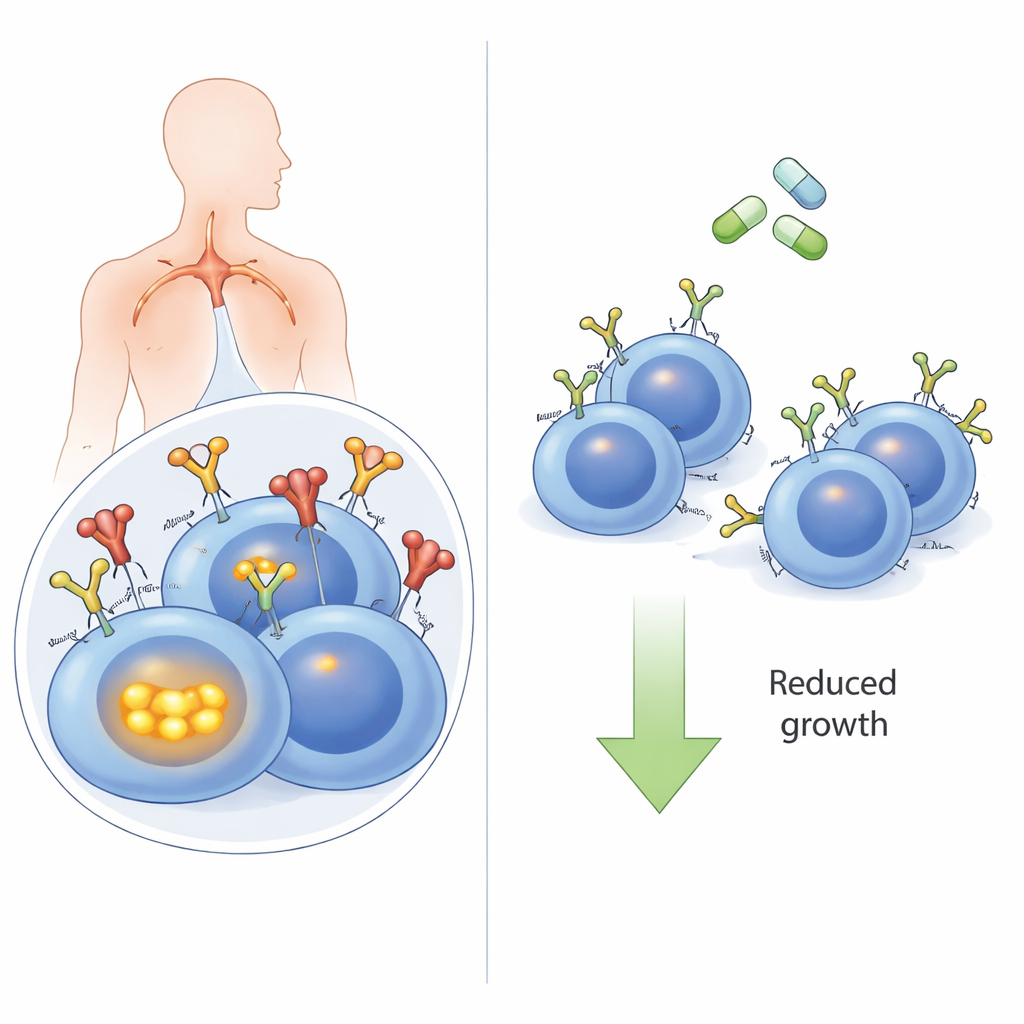
A antena da célula cancerosa
As células B, um tipo de glóbulo branco, usam o receptor de célula B em sua superfície para reconhecer ameaças. Em muitos LDGCBs, especialmente no subtipo de alto risco “célula B ativada” (ABC), esse mesmo receptor é sequestrado para enviar mensagens constantes de “permaneça vivo e cresça”. Frequentemente, esses BCRs reconhecem moléculas próprias do corpo (autoantígenos), que agem como uma campainha travada. Quando autoantígenos se ligam, o BCR faz mais do que apenas sinalizar na superfície: ele é puxado para dentro da célula e se junta a um aglomerado proteico interno com sensores chamados TLR9 e MYD88. Esse supercomplexo então ativa o NFκB, uma potente via de sinalização promotora de crescimento. Até agora, não estava claro se essa jornada interna do receptor era realmente necessária para os sinais que impulsionam o câncer.
Reconfigurando a antena para testar seus limites
Para responder a essa questão, os pesquisadores usaram edição gênica por CRISPR para alterar precisamente as “pontas” do BCR em linhagens de células de linfoma. Eles substituíram as regiões naturais de reconhecimento autorreativas por versões que reconhecem ovalbumina, uma proteína de ovo inofensiva usada como ferramenta de laboratório. Esses receptores modificados não capturavam mais seus autoantígenos habituais, mas ainda podiam ser ativados de forma controlada com adição de ovalbumina. Em células de linfoma do tipo ABC que normalmente dependem da ligação por autoantígeno, essa troca reduziu fortemente a atividade de muitas quinases de sinalização chave e atenuou genes responsivos ao NFκB. As células cresceram mais lentamente, apesar de apresentarem, na verdade, mais BCR na superfície, demonstrando que o engajamento contínuo por autoantígenos e a subsequente sinalização interna são críticos para a sua sobrevivência.
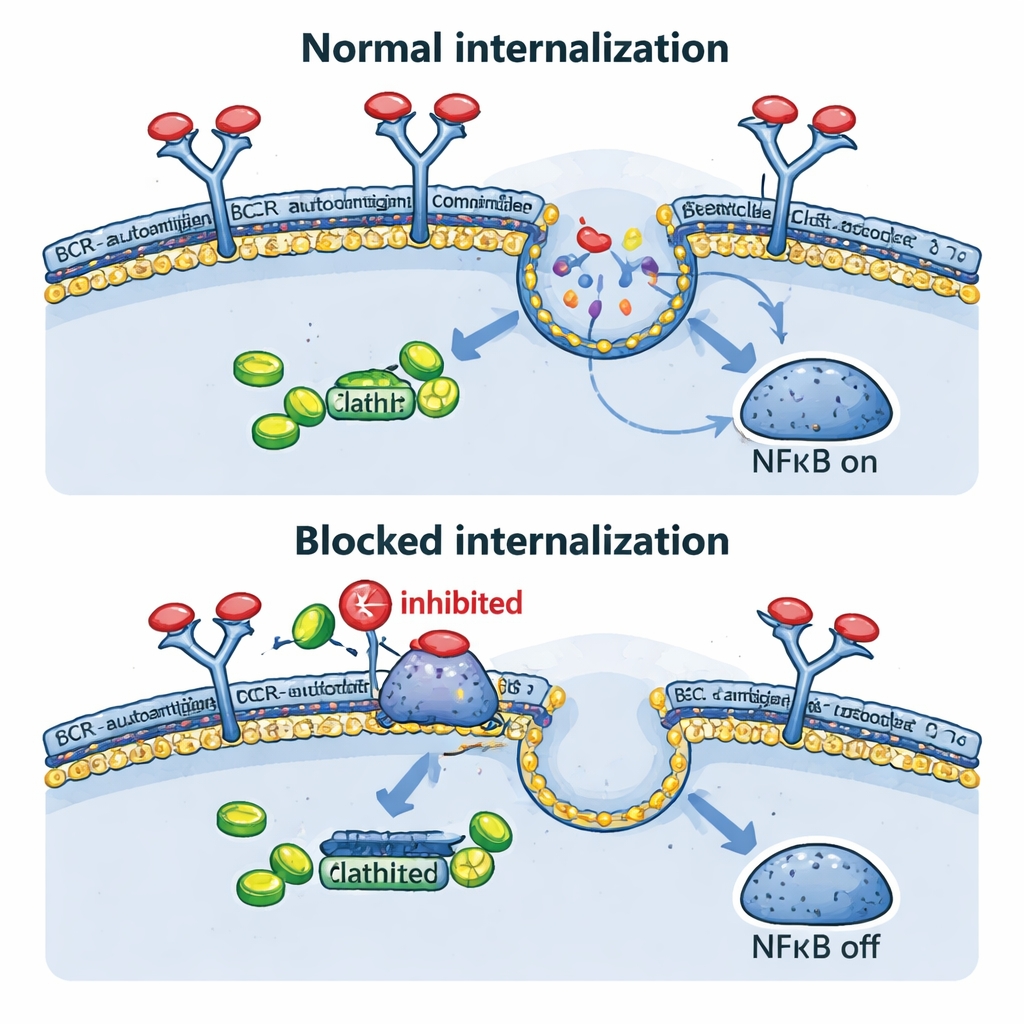
Puxando receptores para dentro: um passo crucial
A equipe então examinou diretamente o que acontece ao BCR depois que ele encontra seu antígeno. Em seus modelos engenheirados, tanto gatilhos baseados em anticorpos quanto a ovalbumina fizeram o receptor desaparecer da superfície celular em poucos minutos, confirmando a internalização rápida. Isso ocorreu não apenas quando o antígeno estava livre fora da célula, mas também quando era artificialmente exibido na membrana da própria célula, imitando certas situações reais de tumor. Bloquear esse tráfego interno geneticamente, usando uma forma dominante‑negativa de uma proteína chamada dinamina‑2, essencial para a endocitose mediada por clatrina, manteve o BCR na superfície, encolheu os complexos internos BCR–TLR9–NFκB, reduziu genes alvo do NFκB e desacelerou o crescimento celular. Curiosamente, quando a endocitose foi bloqueada, alguns sinais “de fundo” do BCR na superfície aumentaram, sugerindo que as células cancerosas podem tentar compensar ativando um modo de sinalização tônica mais fraco.
Remédios antigos, novos truques
Como desenvolver novos fármacos é lento e caro, os autores perguntaram se medicamentos existentes que bloqueiam a endocitose poderiam imitar os experimentos genéticos. Fenotiazinas, uma família de antipsicóticos e anti‑náusea, são conhecidas por inibir a dinamina‑2 e a captação dependente de clatrina de receptores. Em células de linfoma, compostos como proclorperazina e clorpromazina aumentaram os níveis de BCR na superfície e reduziram fortemente a internalização induzida por antígeno. Isso levou a menor atividade de genes dirigidos por NFκB e redução da viabilidade de células LDGCB do tipo ABC, particularmente aquelas com componentes de BCR intactos. Em camundongos portadores de enxertos de linfoma humano, a proclorperazina em doses clinicamente alcançáveis retardou significativamente o crescimento tumoral. Além disso, a combinação de fenotiazinas com drogas que bloqueiam outras enzimas ligadas ao BCR, como SYK e PI3Kδ, produziu efeitos anti‑tumorais mais fortes do que cada tratamento isolado.
O que isso pode significar para o tratamento
No geral, o estudo mostra que, para um subgrupo substancial de LDGCBs, os sinais que impulsionam o câncer não provêm simplesmente dos receptores na superfície celular; eles dependem criticamente de puxar o complexo BCR–antígeno para dentro por uma via específica de endocitose. Interromper essa etapa — seja por artifícios genéticos ou por drogas fenotiazínicas — enfraquece a sinalização NFκB e prejudica a sobrevivência das células tumorais, além de possivelmente sensibilizar as células aos inibidores já existentes da via do BCR. Como as fenotiazinas já têm posologia e segurança bem compreendidas como medicamentos anti‑náusea, este trabalho fornece um roteiro realista para testes clínicos que as avaliem, isoladamente ou em combinação, em pacientes cujos linfomas apresentem atividade de BCR dependente de autoantígeno.
Citação: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Palavras-chave: linfoma difuso de grandes células B, receptor de célula B, endocitose, fenotiazinas, sinalização NFkB