Clear Sky Science · pt
Análise multiómica resolvida no tempo da exposição a paclitaxel em neurônios sensoriais humanos derivados de iPSC revela mecanismos da neuropatia periférica induzida por quimioterapia
Por que alguns medicamentos contra o câncer prejudicam os nervos
A quimioterapia ajudou milhões de pessoas a sobreviver ao câncer, mas muitos pacientes pagam um preço oculto: meses ou anos de dor em queimação, formigamento e dormência nas mãos e pés. Este estudo faz uma pergunta simples, porém importante: o que exatamente o amplamente usado medicamento contra o câncer paclitaxel faz às células nervosas sensoriais humanas, e entender essas mudanças pode apontar caminhos para prevenir e tratar melhor esse dano nervoso?
Das células de pacientes a nervos sensoriais cultivados em laboratório
Em vez de depender de experimentos em animais, os pesquisadores partiram de células de cinco doadores humanos, incluindo pacientes com câncer de mama que tinham recebido paclitaxel. Eles reprogramaram essas células em células-tronco pluripotentes induzidas e então as guiaram para se tornarem neurônios sensoriais — o mesmo tipo de célula nervosa que transmite sinais de toque e dor da pele para a medula espinhal. Esses neurônios cultivados em laboratório formaram fibras longas e delicadas e apresentaram atividade elétrica muito parecida com nervos sensoriais reais do corpo. A equipe então os expôs a doses crescentes de paclitaxel, imitando os níveis de droga observados em pacientes, e acompanhou a saúde celular ao longo de vários dias. Em concentrações baixas os neurônios lidaram bem, mas em uma dose clinicamente relevante (100 nM) a sobrevivência começou a cair após cerca de dois dias, marcando o início do dano nervoso tóxico.
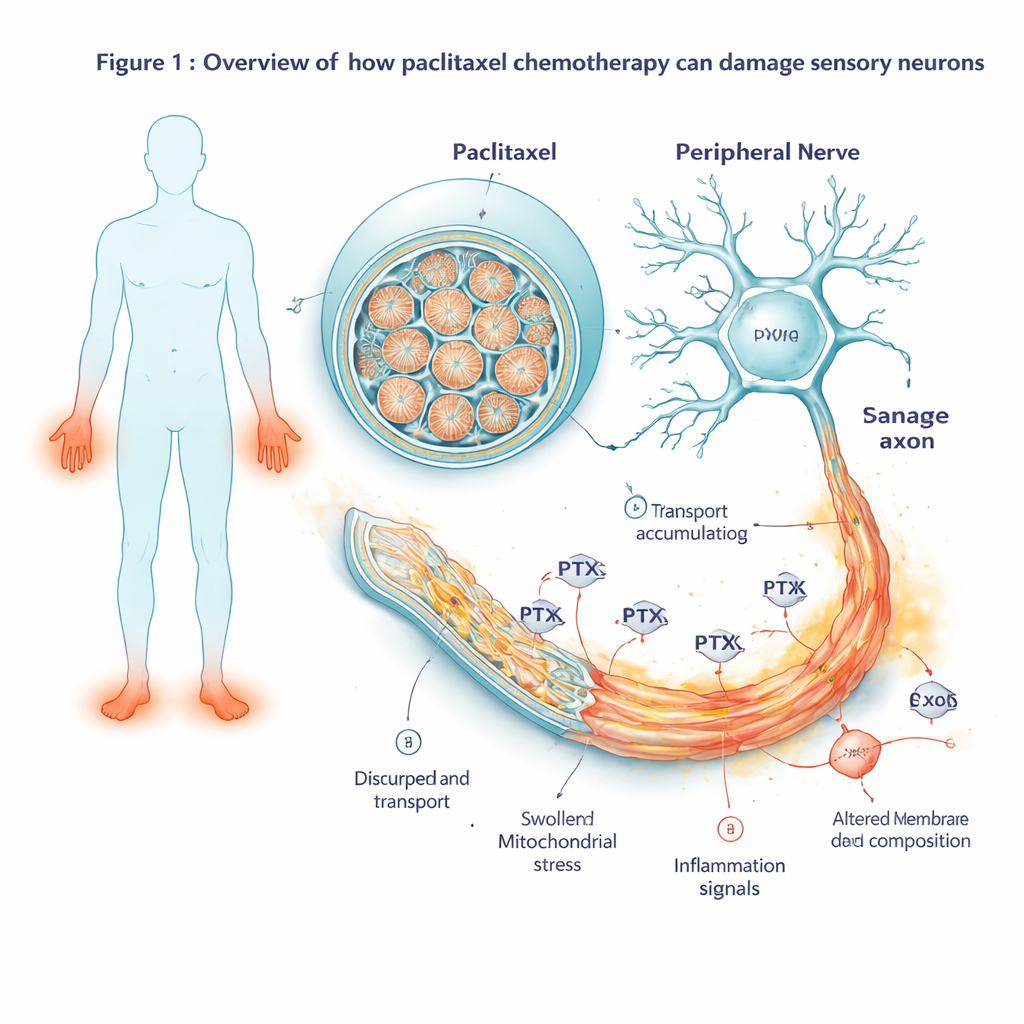
Observando mudanças na atividade gênica ao longo do tempo
Para ver como as células respondiam antes de se deteriorarem visivelmente, os cientistas mediram quais genes eram ligados ou desligados em vários pontos no tempo, desde duas horas após a exposição ao medicamento até vários dias depois da lavagem do fármaco. No início, observaram ativação de um programa celular clássico de estresse centrado em um gene chamado JUN. À medida que a exposição continuou, esse sinal de estresse se alargou para uma cascata de autodestruição completa: genes que empurram as células em direção à morte programada foram fortemente ativados, enquanto parceiros protetores foram sobrepujados. Ao mesmo tempo, genes ligados à inflamação e à sinalização da dor tornaram-se mais ativos. Os neurônios começaram a produzir mais mensageiros inflamatórios, peptídeos relacionados à dor e receptores que tornam as células mais sensíveis a estímulos nocivos — mudanças que espelham o que se vê em distúrbios nervosos dolorosos.
Olhar profundo nas proteínas e lipídios dentro dos neurônios
Porque os genes são apenas plantas, a equipe também examinou as proteínas realmente presentes nos neurônios, bem como sua composição lipídica (gorduras). Após 48 horas de exposição ao paclitaxel, muitos dos mesmos sinais de estresse e inflamatórios detectados ao nível do RNA também apareceram como proteínas aumentadas, confirmando que os neurônios estavam executando esses programas prejudiciais. De forma marcante, proteínas necessárias para o transporte axonal — os motores moleculares e estruturas que movem carga ao longo das longas fibras nervosas — foram fortemente reduzidas. Isso incluiu quinésinas e proteínas regulatórias que mantêm as trilhas de microtúbulos estáveis. No nível lipídico, os neurônios mostraram queda em blocos de construção chave para colesterol e lipídios de membrana, ao mesmo tempo em que houve aumento em gorduras armazenadas chamadas triacilgliceróis. Juntas, essas mudanças sugerem que o paclitaxel não só desencadeia vias de morte celular, mas também enfraquece a estrutura física e o equilíbrio energético das fibras nervosas.
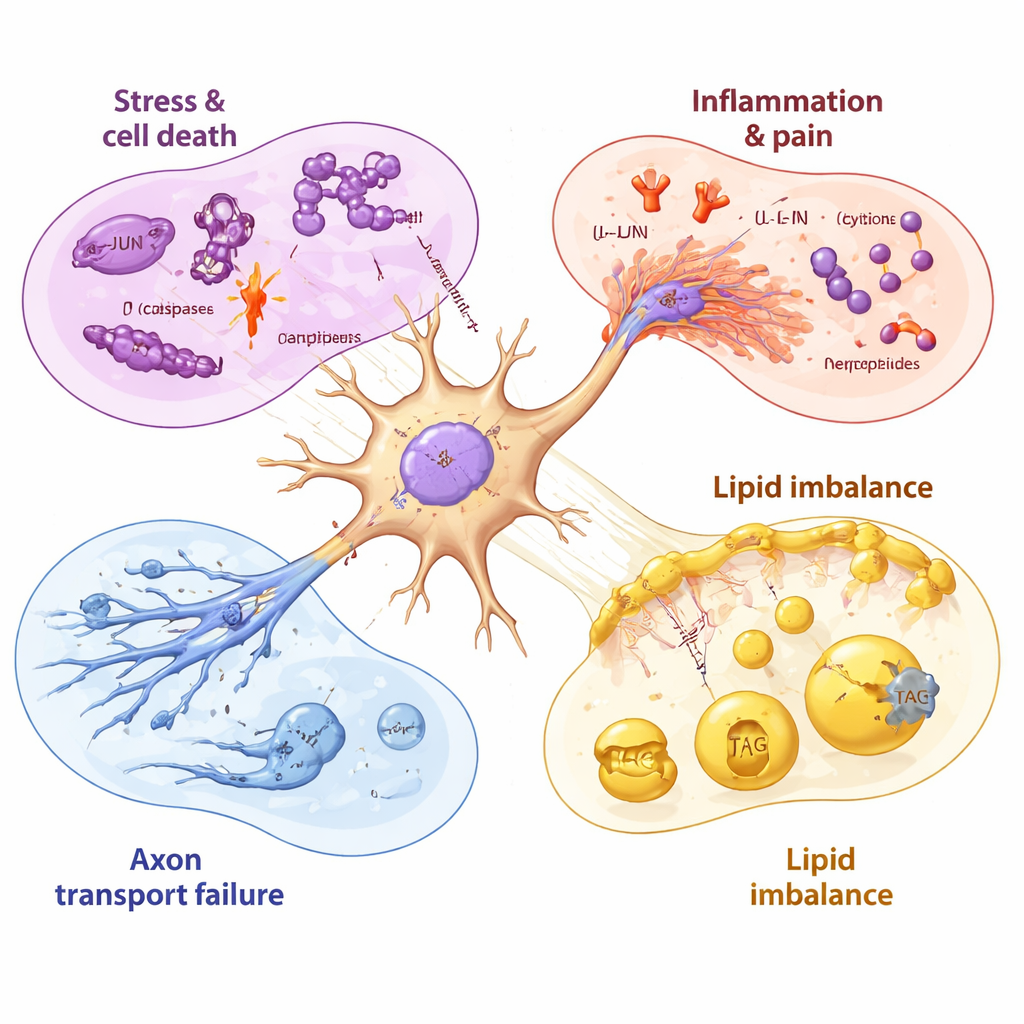
Uma linha do tempo da lesão nervosa e da recuperação incompleta
Ao amostrar os neurônios antes, durante e após a exposição ao medicamento, os pesquisadores puderam ordenar esses eventos no tempo. Genes mitocondriais (relacionados à energia) foram perturbados em poucas horas, seguidos pelo gene de estresse JUN, e então por uma ativação mais forte de programas de morte celular e inflamatórios à medida que a viabilidade começava a cair. Mesmo após a remoção do paclitaxel, muitos sinais nocivos permaneceram elevados por dias, enquanto os genes necessários para fabricar lipídios de membrana saudáveis continuaram a declinar. Algumas moléculas que aumentaram tardiamente, como uma bomba de efluxo de drogas que pode expulsar paclitaxel e certos fatores de crescimento, indicaram que os neurônios tentavam se proteger e reparar — mas essas respostas pareceram relativamente lentas e incompletas em comparação com o empurrão rápido e inicial em direção ao dano.
O que isso significa para pacientes que vivem com dor nervosa
Para um público leigo, a mensagem é que o paclitaxel prejudica os nervos sensoriais por meio de uma série coordenada de golpes: ele estressa os sistemas energéticos, vira interruptores genéticos em direção à morte celular, provoca inflamação e sinalização de dor, desorganiza as “rodovias de transporte” internas dentro das fibras nervosas e altera as gorduras que mantêm a membrana nervosa estável. Ao mapear essas mudanças em neurônios derivados de humanos com grande detalhe, o estudo destaca alvos concretos e potencialmente tratáveis — como reguladores específicos de estresse, receptores inflamatórios e enzimas de síntese lipídica — que poderiam ser bloqueados ou apoiados para proteger os nervos sem enfraquecer o tratamento do câncer. Embora novas terapias exijam mais testes, este trabalho oferece um roteiro mais claro para prevenir ou aliviar o dano nervoso induzido pela quimioterapia, melhorando a qualidade de vida dos sobreviventes de câncer.
Citação: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Palavras-chave: neuropatia periférica induzida por quimioterapia, paclitaxel, neurônios sensoriais, neuroinflamação, degeneração axonal