Clear Sky Science · pt
Metilação reversível de arginina regula a atividade mitocondrial de IDH2: controle coordenado por CARM1 e KDM3A/4A
Ajustando com Precisão as Usinas de Energia da Célula
As mitocôndrias, frequentemente chamadas de usinas de energia das nossas células, fazem muito mais do que apenas gerar energia. Elas ajustam constantemente a forma como queimam combustíveis para atender às necessidades do organismo e, quando esse ajuste falha, pode contribuir para doenças como diabetes, insuficiência cardíaca e câncer. Este estudo revela um “dimmer” oculto dentro das mitocôndrias: uma pequena marca química em um único bloco construtor de uma enzima chave, IDH2, que ajuda a determinar se as mitocôndrias funcionam em baixa ou aumentam sua produção de energia.
Uma Pequena Marca com Grandes Consequências
As proteínas em nossas células não são estáticas; elas costumam ser modificadas com pequenos grupos químicos que alteram seu comportamento. Enquanto muitas dessas modificações no núcleo celular e no citosol são bem conhecidas, as que ocorrem dentro das mitocôndrias são menos exploradas. Os autores focaram em um tipo particular de marca chamado metilação de arginina e perguntaram se ela poderia controlar o funcionamento das enzimas mitocondriais. Eles se concentraram na enzima IDH2, uma peça central do ciclo do ácido tricarboxílico (TCA), que ajuda a converter nutrientes em energia e em blocos metabólicos importantes. Usando ferramentas bioquímicas e espectrometria de massa, descobriram que IDH2 carrega uma marca metil específica em um aminoácido, a arginina 188, e que essa marca é colocada por uma enzima chamada CARM1, que surpreendentemente atua dentro das mitocôndrias.
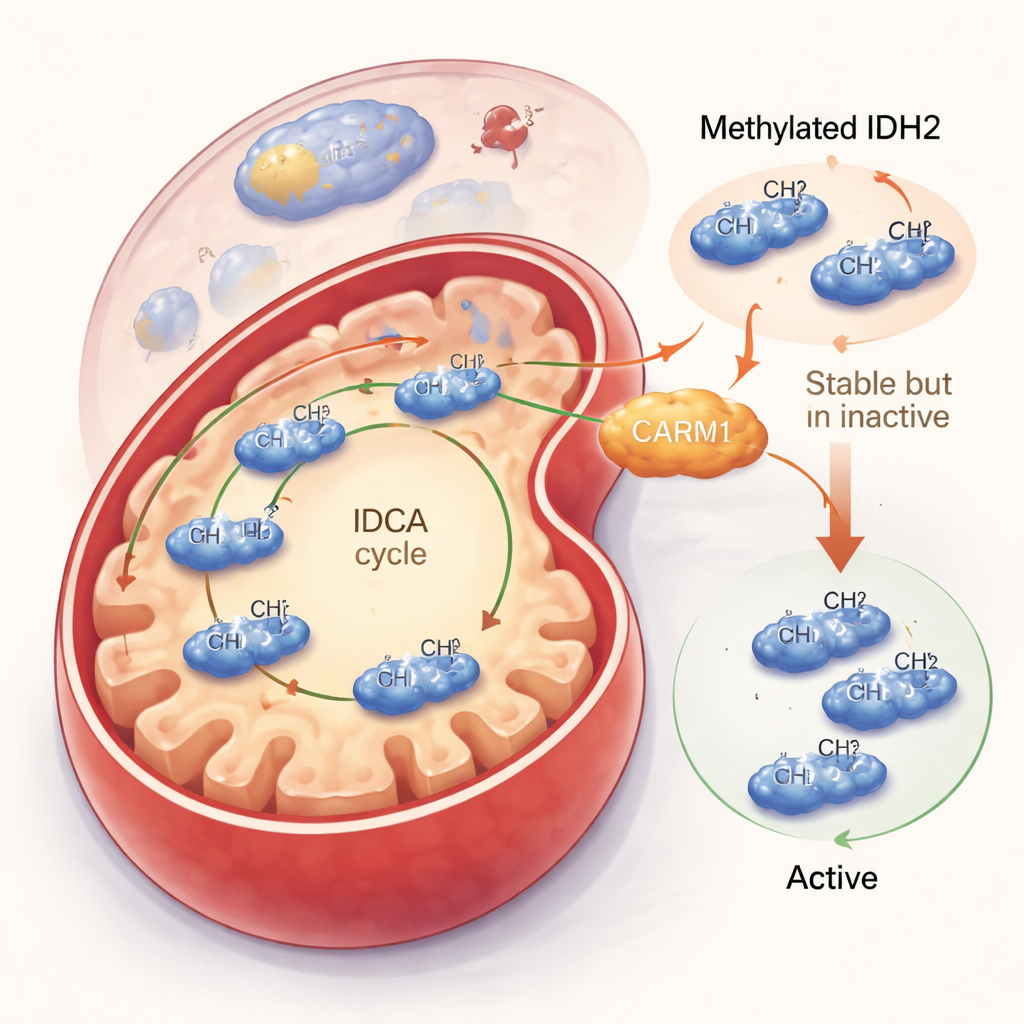
Reduzindo a Atividade de IDH2, mas Aumentando sua Estabilidade
A equipe então investigou o que essa marca de metil realmente faz. Quando a CARM1 estava ativa e podia metilar o IDH2, a proteína IDH2 tornava-se mais estável e permanecia por mais tempo na célula. Mas esse aparente benefício tinha um custo: o IDH2 metilado era menos ativo. Em experimentos celulares e em proteínas purificadas, o IDH2 metilado produzia menos do seu produto principal, o alfa-cetoglutarato, e gerava menos da molécula protetora NADPH. Em contraste, uma versão do IDH2 que não podia ser metilada na arginina 188 formava mais rapidamente a forma dimérica ativa, funcionava mais depressa e aumentava tanto os níveis de alfa-cetoglutarato quanto de NADPH. Mesmo que houvesse menos dessa forma não metilada de IDH2 no total, cada molécula fazia mais trabalho, levando a um aumento líquido na produção mitocondrial.
Um Interruptor Reversível com Dois "Apagadores"
De modo crucial, essa marca de metil não é permanente. Os pesquisadores mostraram que duas enzimas normalmente conhecidas por remover outro tipo de marca, as desmetilases de lisina KDM3A e KDM4A, também podem apagar a metilação de arginina em IDH2. Quando essas desmetilases estavam presentes, a arginina metilada na posição 188 perdeu seus grupos químicos adicionais, o IDH2 tornou-se menos estável, porém mais ativo, e sua forma dimérica aumentou. Células com níveis maiores de KDM3A ou KDM4A exibiram maior potencial de membrana mitocondrial e consumiram mais oxigênio, sinais de que suas mitocôndrias estavam operando com metabolismo oxidativo mais intenso. Quando essas enzimas foram reduzidas, ocorreu o contrário: a atividade de IDH2 caiu e o desempenho mitocondrial declinou, o que reforça que se trata de um sistema de controle reversível e não de uma mudança unidirecional.
Ligando Metabolismo e Doença
Como IDH2 tem sido associado ao câncer e a outros distúrbios, os autores examinaram como esse interruptor de metilação poderia importar em contextos semelhantes à doença. Em diversas linhas celulares normais e cancerosas, observaram que níveis mais altos de proteína IDH2 frequentemente acompanhavam maior metilação e, surpreendentemente, menor atividade enzimática, sugerindo que “mais proteína” nem sempre significa “mais função”. Em conjuntos de dados de câncer de mama, pacientes com níveis mais elevados de proteína IDH2 tenderam a ter pior sobrevida, apesar de a atividade do gene IDH2 não correlacionar com o desfecho. Os resultados sustentam um modelo em que a metilação dirigida por CARM1 desacelera o ciclo do TCA e inclina as células para vias alternativas de uso de nutrientes favoráveis ao câncer, enquanto desmetilases como KDM3A e KDM4A podem empurrar as células de volta para uma produção de energia mais eficiente.
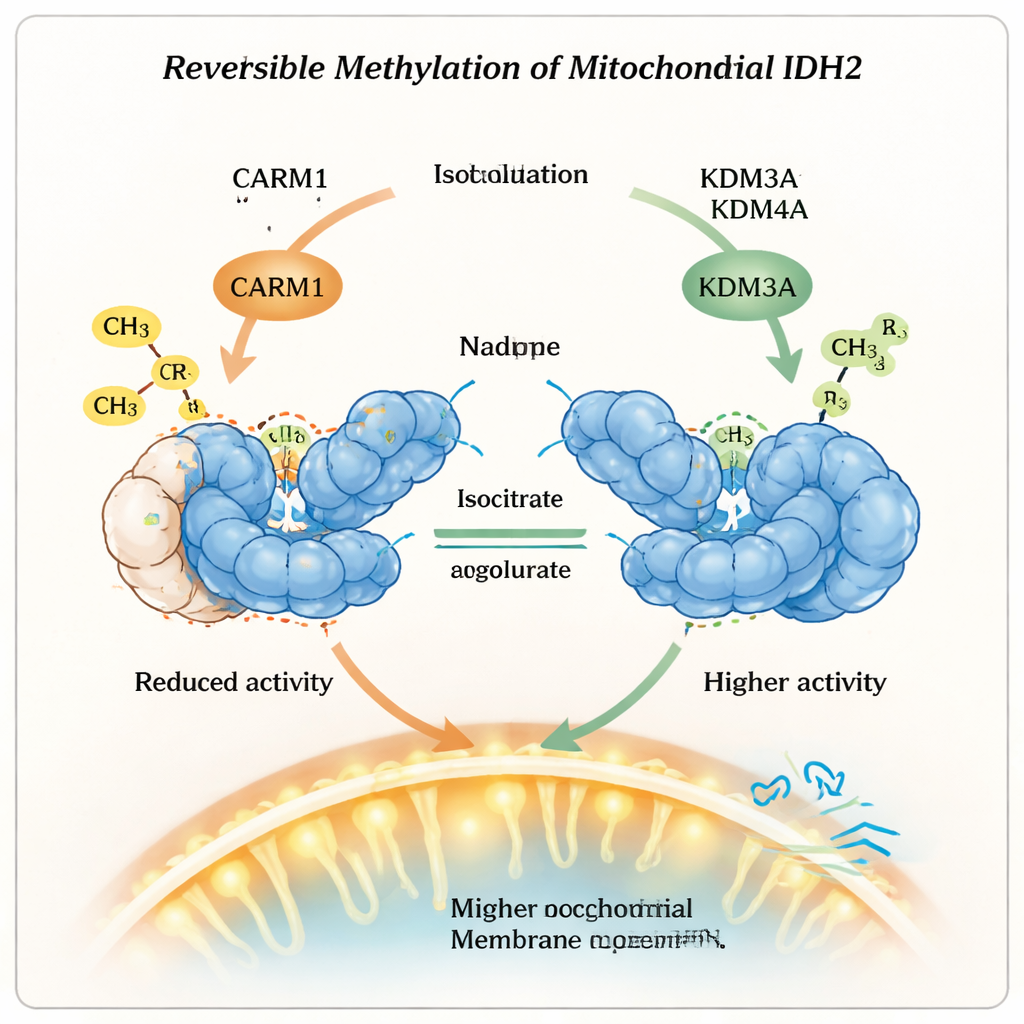
O Que Isso Significa para Saúde e Terapia
Em termos cotidianos, este trabalho mostra que as mitocôndrias não simplesmente ligam ou desligam enzimas, mas usam marcas químicas reversíveis como botões de ajuste fino. Ao adicionar um grupo metil, CARM1 transforma o IDH2 em uma forma mais duradoura, porém menos ativa; ao remover essa marca, KDM3A e KDM4A sacrificam parte da estabilidade para ganhar maior potência de saída. Esse equilíbrio influencia como as células escolhem entre queima rápida porém ineficiente de açúcar e produção de energia mais lenta e eficiente. Compreender esse “dimmer” de metilação em IDH2 abre novas possibilidades terapêuticas para corrigir o metabolismo mitocondrial defeituoso em condições como câncer e doenças metabólicas, ao mirar as enzimas que escrevem e apagam essas marcas químicas pequenas, porém poderosas.
Citação: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Palavras-chave: mitocôndrias, IDH2, metilação de arginina, metabolismo celular, CARM1