Clear Sky Science · pt
Um circuito inflamatório MIF-p38-GSDMD em queratinócitos fundamenta o lúpus cutâneo induzido por UVB
Por que a luz solar pode ser um problema sério no lúpus
Para a maioria das pessoas, o sol provoca apenas um bronzeado ou, no pior cenário, uma queimadura. Mas para muitos pacientes com lúpus, alguns minutos de radiação ultravioleta B (UVB) podem desencadear erupções dolorosas e duradouras e até agravar a doença sistêmica. Este estudo revela um “circuito de retroalimentação” oculto dentro das células da pele que ajuda a explicar por que a pele desses pacientes é tão sensível à luz — e aponta para tratamentos locais promissores que poderiam acalmar a reação sem suprimir todo o sistema imunológico.
Células da pele como agentes problemáticos inesperados
Médicos já sabiam que o lúpus cutâneo eritematoso (LCE) envolve inflamação crônica e cicatrização da pele, mas a atenção costumava se concentrar nas células imunes invasoras. Usando sequenciamento de RNA de célula única, os autores focaram nas próprias células estruturais da pele — queratinócitos na camada externa e fibroblastos na derme. Eles constataram que, em pacientes com lúpus, subpopulações específicas de queratinócitos estão expandidas e apresentam uma forte “assinatura de interferon”, um padrão de genes de alarme antiviral permanentemente ativados. Dentro desses queratinócitos anormais, uma proteína mensageira se destacou: o fator inibitório da migração de macrófagos, ou MIF, produzido em níveis muito mais elevados do que moléculas inflamatórias mais conhecidas, como TNF ou IL‑6.
Um mensageiro oculto liberado pela luz solar
Detectar altos níveis de MIF dentro dos queratinócitos ainda não explicava por que a luz solar é tão perigosa. Quando a equipe expôs queratinócitos cultivados à luz UVB, descobriram que a quantidade total de MIF nas células mal mudou — mas a proteína foi liberada para o fluido circundante de forma dependente da dose. Quanto mais UVB aplicado, mais MIF vazou, acompanhando de perto um marcador de dano de membrana. Quando esse fluido enriquecido em MIF foi aplicado a queratinócitos e fibroblastos frescos, provocou alterações clássicas semelhantes ao LCE: mais citocinas inflamatórias e enzimas que degradam e remodelam a matriz de suporte da pele. Silenciar o MIF com ferramentas genéticas ou bloqueá‑lo com um fármaco de pequena molécula reduziu fortemente essas reações nocivas, demonstrando que o MIF derivado dos queratinócitos não é um mero espectador, mas um amplificador chave do dano induzido por UVB. 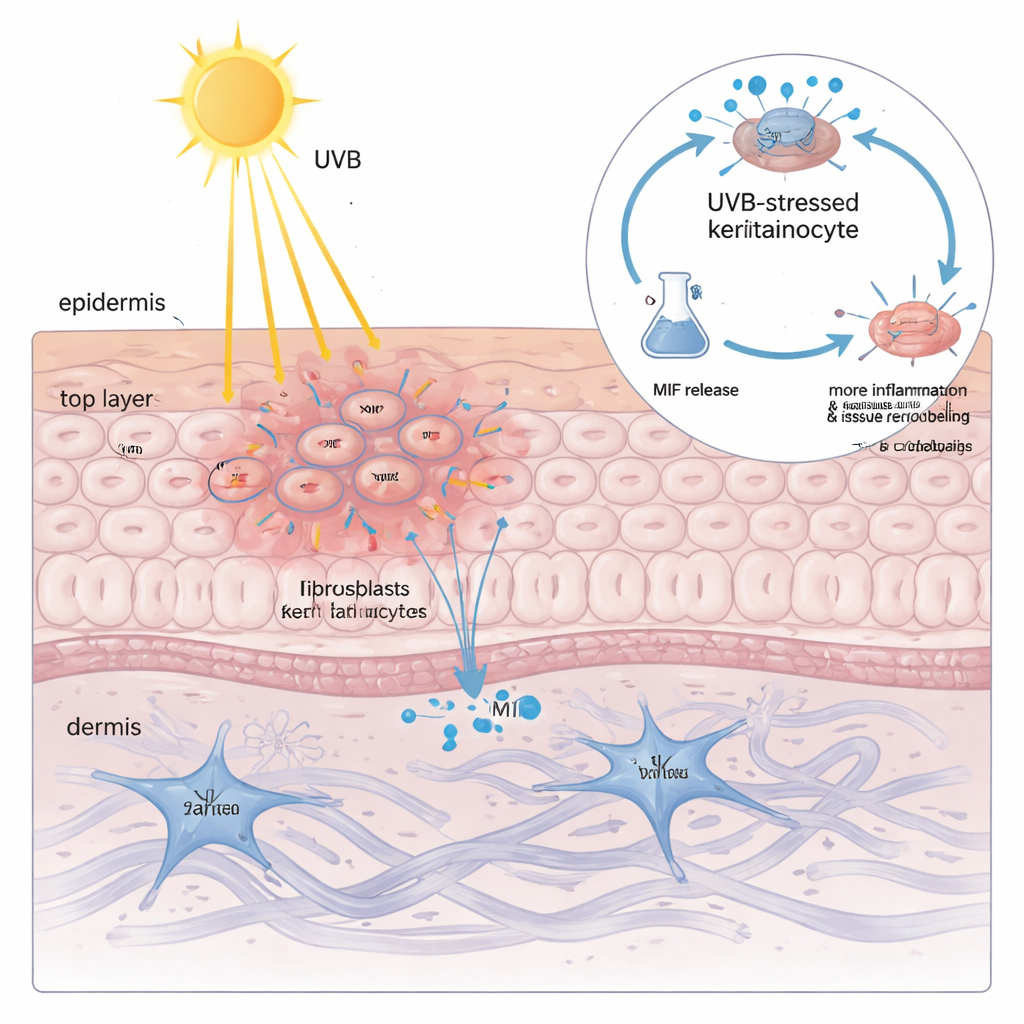
Um ciclo inflamatório auto‑sustentado dentro dos queratinócitos
Para entender como o UVB força os queratinócitos a liberar MIF, os pesquisadores construíram um modelo de queratinócito “semelhante ao lúpus” ao carregar as células com seu próprio DNA e RNA, imitando os detritos genéticos mal gerenciados observados no lúpus. Nesse estado primado, o UVB ativou a chamada resposta ao estresse ribotóxico: um sinal de dano oriundo dos ribossomos que ativou uma quinase chamada ZAKα e, por sua vez, a enzima de estresse p38. Essa via aumentou outra proteína, o fator de transcrição C/EBPβ, que se ligou à região de controle do gene NLRP3 e o ativou. O NLRP3 então impulsionou a clivagem de GSDMD, uma proteína formadora de poros que perfura a membrana celular e causa uma forma inflamatória de morte celular conhecida como piroptose. De forma crucial, o MIF escapou principalmente por esses poros formados por GSDMD — não via vesículas secretoras normais. Uma vez fora da célula, o MIF ligou‑se ao seu receptor de superfície CD74 em queratinócitos, reativando p38, NLRP3 e GSDMD e assim fechando um círculo vicioso: UVB → p38 → NLRP3 → poros GSDMD → liberação de MIF → mais ativação de p38.
Da descoberta molecular a novos tratamentos locais
Esse circuito não era apenas uma curiosidade de laboratório. Em uma linhagem de camundongos propensa ao lúpus, a exposição ao UVB produziu lesões cutâneas severas com altos níveis de MIF, ativação de p38, NLRP3 e GSDMD clivado na epiderme. Quando os pesquisadores usaram um vírus de terapia gênica para silenciar o gene Mif especificamente na pele, as erupções induzidas por UVB ficaram muito mais brandas, e os marcadores de inflamação e remodelamento tecidual caíram tanto em queratinócitos quanto em fibroblastos. Para evitar efeitos colaterais sistêmicos dos medicamentos, eles também desenvolveram adesivos de microagulhas solúveis carregados com o inibidor de MIF ISO‑1. Pressionadas brevemente na pele, essas minúsculas agulhas entregaram o fármaco sem dor nas camadas superiores. Camundongos propensos ao lúpus tratados assim desenvolveram bem menos e menos graves lesões após UVB, e a assinatura molecular do circuito MIF‑p38‑GSDMD foi marcadamente atenuada. 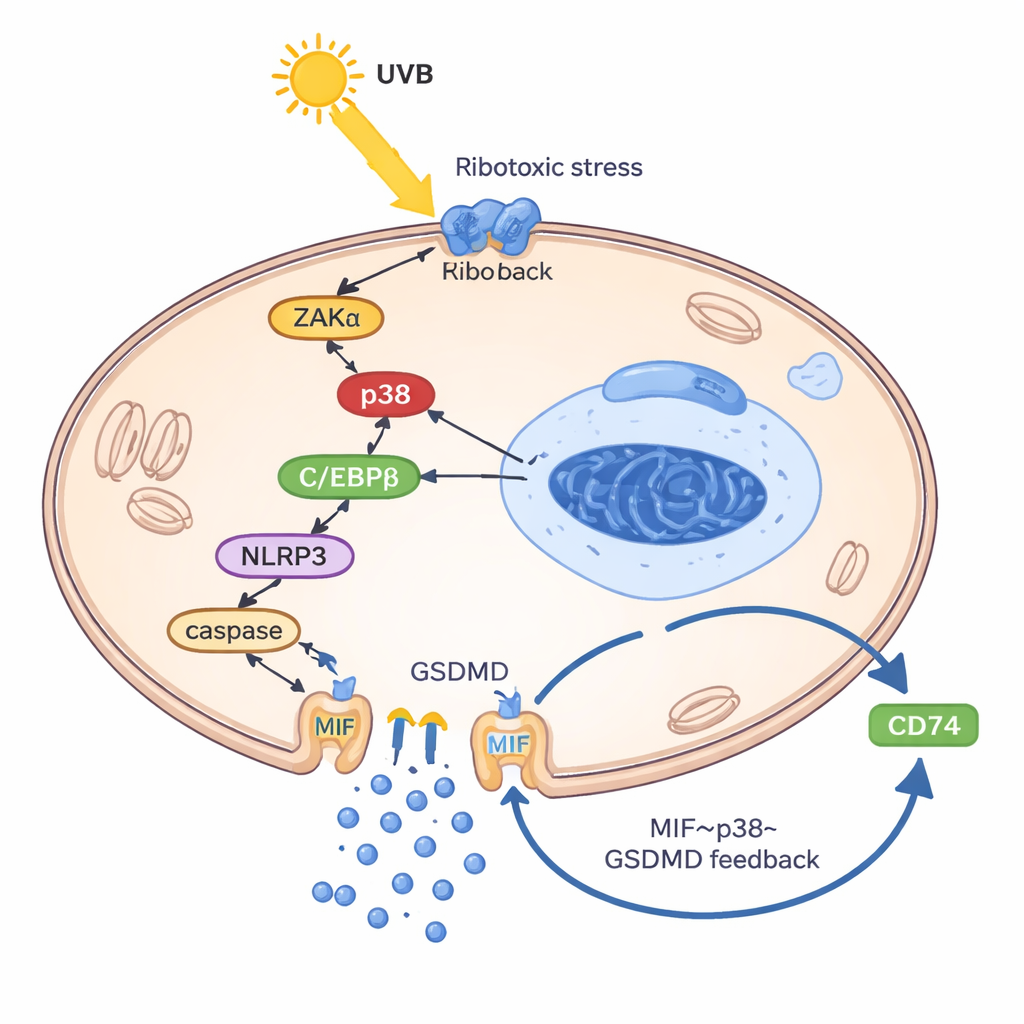
O que isso significa para pessoas com lúpus
Em termos simples, este trabalho mostra que, no lúpus, certas células da pele estão programadas para reagir em excesso ao UVB liberando uma poderosa molécula “amplificadora”, o MIF, através de poros que elas próprias formam na membrana. Esse impulso retroalimenta a maquinaria inflamatória, mantendo a reação mesmo após o término da exposição inicial à luz. Ao mapear esse circuito passo a passo, o estudo sugere que bloquear o MIF diretamente na pele — usando silenciamento gênico ou sistemas de entrega inteligentes como adesivos de microagulhas — poderia interromper o ciclo de surtos fotosensíveis sem suprimir amplamente o sistema imunológico. Se estratégias semelhantes se mostrarem seguras e eficazes em humanos, elas poderão oferecer às pessoas com lúpus novas maneiras de conviver mais confortavelmente com a luz.
Citação: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Palavras-chave: lúpus cutâneo, fotossensibilidade, queratinócitos, circuito inflamatório, terapia com microagulhas