Clear Sky Science · pt
Pneumonite relacionada a inibidores de checkpoint imunológico: avanços atuais e o papel putativo da terapia com células-tronco mesenquimais
Quando o tratamento do câncer volta-se contra os pulmões
Medicamentos que liberam o sistema imune contra o câncer transformaram o tratamento de doenças como câncer de pulmão e melanoma. No entanto, esse novo poder tem um custo: em alguns pacientes, o mesmo ataque imune que mira os tumores também se volta para os pulmões, causando uma condição chamada pneumonite relacionada a inibidores de checkpoint imunológico (ICIP). Esta revisão explica o que é ICIP, por que ocorre, como os médicos a tratam atualmente e por que um tipo especial de célula-tronco — as células-tronco mesenquimais (MSCs) — pode um dia oferecer uma maneira mais segura e precisa de acalmar a tempestade sem comprometer o controle do câncer. 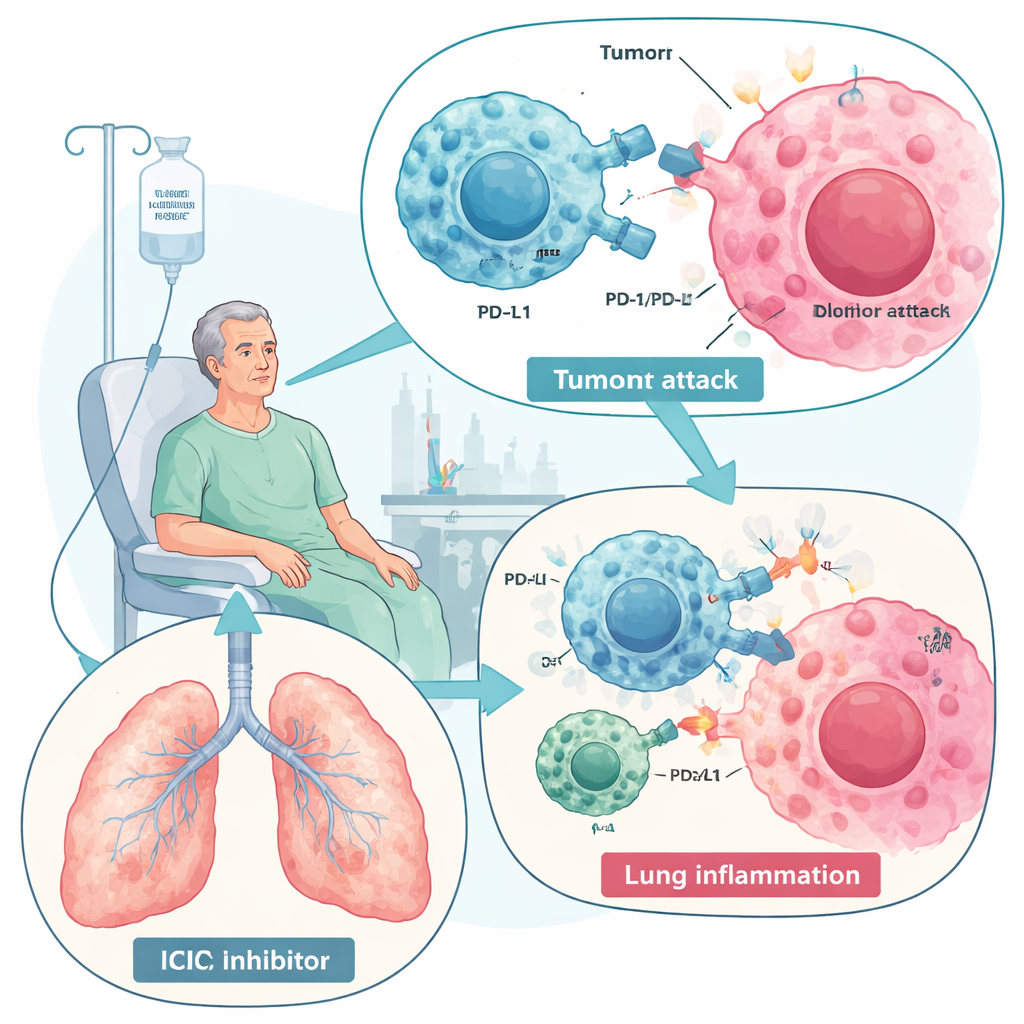
Medicamentos poderosos contra o câncer com um risco oculto para os pulmões
Os inibidores de checkpoint imunológico, especialmente os que bloqueiam PD-1 e PD-L1, atuam removendo os “freios” moleculares que normalmente mantêm as respostas imunes sob controle. Com os freios desativados, as células T conseguem reconhecer e destruir melhor as células cancerígenas, melhorando a sobrevida em muitos tipos de tumor. Mas esse mesmo impulso pode romper a tolerância normal e desencadear efeitos colaterais imunes em múltiplos órgãos. A ICIP é a complicação pulmonar mais grave desses medicamentos e uma das principais causas relacionadas ao sistema imune de morte associada ao tratamento. Afeta desde alguns por cento até quase um terço dos pacientes em alguns estudos do cotidiano, particularmente aqueles com câncer de pulmão ou doença pulmonar pré-existente, como DPOC ou doença pulmonar intersticial. Os sintomas variam de tosse leve e falta de ar a insuficiência respiratória potencialmente fatal.
Como o sistema imune danifica o pulmão
A revisão descreve a ICIP como resultado de um equilíbrio imune perturbado dentro dos pulmões. Células “combatentes” hiperativas — células T CD8, certos linfócitos T auxiliares, macrófagos inflamatórios, neutrófilos e células natural killer — invadem o tecido pulmonar e liberam proteínas sinalizadoras agressivas, incluindo interferon-gama, TNF-alfa e interleucinas como IL-6 e IL-17. Ao mesmo tempo, células normalmente protetoras que atenuam a inflamação, como células T reguladoras e macrófagos orientados para a reparação, estão reduzidas. Alguns pacientes também apresentam aumento de anticorpos autorreativos antes ou durante o tratamento, o que sugere que a ICIP pode, em parte, se assemelhar a uma doença autoimune. No líquido lavado dos pulmões, os médicos encontram um padrão inflamatório rico em células T e uma mistura de citocinas distinta de infecção ou progressão tumoral, o que pode ajudar no diagnóstico.
Detectando, classificando e tratando o dano
Em tomografias computadorizadas, a ICIP frequentemente aparece como áreas nebulosas em “vidro fosco” ou consolidações heterogêneas espalhadas por ambos os pulmões, padrões que diferem do dano por radiação, o qual permanece confinado ao campo irradiado. Os médicos diagnosticam a ICIP combinando achados de imagem, sintomas e uma exclusão cuidadosa de infecção e outras causas. Diretrizes internacionais então classificam a gravidade de 1 (leve, muitas vezes apenas radiológica) a 4 (insuficiência respiratória com risco de vida). O tratamento padrão atual são glucocorticoides — esteroides anti-inflamatórios potentes — às vezes combinados com outros agentes imunossupressores, como tocilizumabe (que bloqueia IL-6) ou infliximabe (que bloqueia TNF-alfa) em casos graves ou resistentes aos esteroides. Essas abordagens podem salvar vidas, mas são ferramentas pouco refinadas: esteroides acarretam muitos efeitos adversos, alguns pacientes não respondem, e a supressão imunológica ampla pode enfraquecer a própria resposta antitumoral que esses medicamentos visavam potencializar.
Por que as células-tronco entram na conversa
As células-tronco mesenquimais, que podem ser obtidas da medula óssea, tecido adiposo ou do cordão umbilical, emergiram como promissoras “moduladoras imunes” em vez de simples formadoras de tecido. Quando infundidas na corrente sanguínea, muitas dessas células ficam temporariamente aprisionadas nos finos vasos sanguíneos do pulmão — o chamado efeito de primeira passagem — o que é uma desvantagem para tratar órgãos distantes, mas uma vantagem potencial para doenças pulmonares. Em modelos animais e em ensaios humanos iniciais de condições como pneumonia severa, síndrome do desconforto respiratório agudo, doença inflamatória intestinal e doença do enxerto contra hospedeiro, as MSCs atenuam respostas imunes exageradas, deslocam as células imunes para um estado mais equilibrado e secretam fatores de crescimento que incentivam a reparação tecidual enquanto limitam a fibrose. Importante, seus benefícios frequentemente decorrem não de se transformarem em células pulmonares, mas da mistura de moléculas sinalizadoras e pequenas vesículas que liberam. 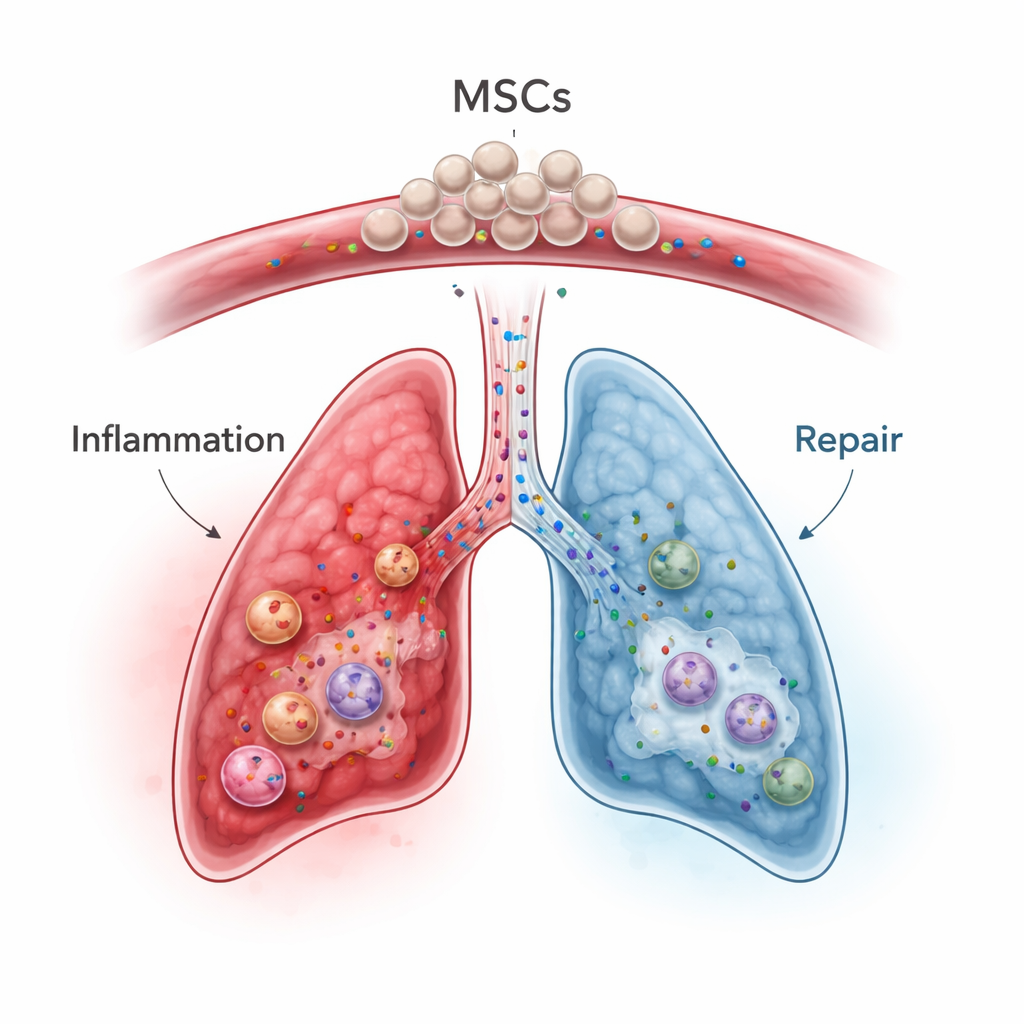
Como as MSCs poderiam acalmar a ICIP sem comprometer a cura
No contexto da ICIP, as MSCs poderiam, em teoria, abordar vários problemas simultaneamente. Elas podem restringir diretamente células T ativadas, promover o crescimento e a função de células T reguladoras e orientar macrófagos de um modo agressivo e prejudicial ao tecido para um perfil mais reparador. Também reduzem mensageiros inflamatórios-chave, como IL-6, IL-1β e TNF-alfa, e aumentam fatores anti-inflamatórios e proteínas protetoras como TSG-6 que ajudam a limitar o dano pulmonar e a fibrose. Trabalhos pré-clínicos sugerem que MSCs ou exossomos derivados de MSCs podem reduzir tempestades de citocinas e danos orgânicos induzidos por inibidores de checkpoint ou radiação, preservando em alguns cenários a atividade antitumoral melhor do que imunossupressores tradicionais. Ainda assim, os autores alertam que as MSCs também podem interagir com tumores e a coagulação sanguínea de maneiras complexas, e que seus efeitos dependem fortemente do ambiente inflamatório circundante e até da fonte das MSCs (medula óssea, tecido adiposo ou cordão umbilical).
Perspectivas: promessa com testes cuidadosos
Para pacientes cujo tratamento do câncer é interrompido ou ameaçado por toxicidade pulmonar severa, terapias à base de MSCs poderiam eventualmente oferecer uma maneira mais direcionada de reduzir a inflamação, reparar o tecido pulmonar e prevenir cicatrização a longo prazo — idealmente sem anular os benefícios que salvam vidas da inibição de checkpoint imune. Entretanto, nenhum ensaio específico de MSC para ICIP foi concluído até o momento. Os autores defendem que estudos animais bem desenhados e ensaios clínicos são urgentemente necessários para definir qual tipo de MSC ou produto de exossomos funciona melhor, quanto administrar, quando aplicar em relação a esteroides e imunoterapia, e como monitorar riscos como crescimento tumoral ou trombose. Até lá, as MSCs permanecem uma opção promissora, porém ainda experimental, no horizonte para manejo desse efeito adverso sério do cuidado oncológico moderno.
Citação: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Palavras-chave: efeitos colaterais da imunoterapia, pneumonite, inibidores de checkpoint, células-tronco mesenquimais, inflamação pulmonar