Clear Sky Science · pt
c-Myc/GRPEL1 mantém a síntese de ácidos graxos via FASN para sustentar a proliferação de células de PDAC
Por que o apetite por gordura das células cancerígenas importa
O câncer de pâncreas é um dos tipos mais letais, em parte porque suas células são especialistas em reprogramar o próprio metabolismo para sobreviver e crescer. Este estudo examina uma parte surpreendente dessa história: como as células tumorais pancreáticas reforçam suas “fábricas internas de gordura” para alimentar um crescimento implacável, e como bloquear esse processo pode abrir novas opções de tratamento para pacientes.
Um câncer difícil com vantagem metabólica
A maioria dos cânceres pancreáticos é do tipo adenocarcinoma ductal pancreático (PDAC), que normalmente é detectado tardiamente e responde mal às terapias atuais. As células de PDAC vivem em um ambiente hostil, com pouco oxigênio e nutrientes escassos, mas prosperam ao reconfigurar o uso de açúcar, gorduras e outros combustíveis. Suas mitocôndrias — pequenas usinas dentro das células — desempenham papel central nessa reprogramação. Para manter essas usinas funcionando, as células monitoram e reparam constantemente milhares de proteínas mitocondriais, um processo conhecido como controle de qualidade de proteínas mitocondriais. Até agora, não estava claro como essa maquinaria de controle de qualidade se conecta à forma como os tumores pancreáticos se alimentam.
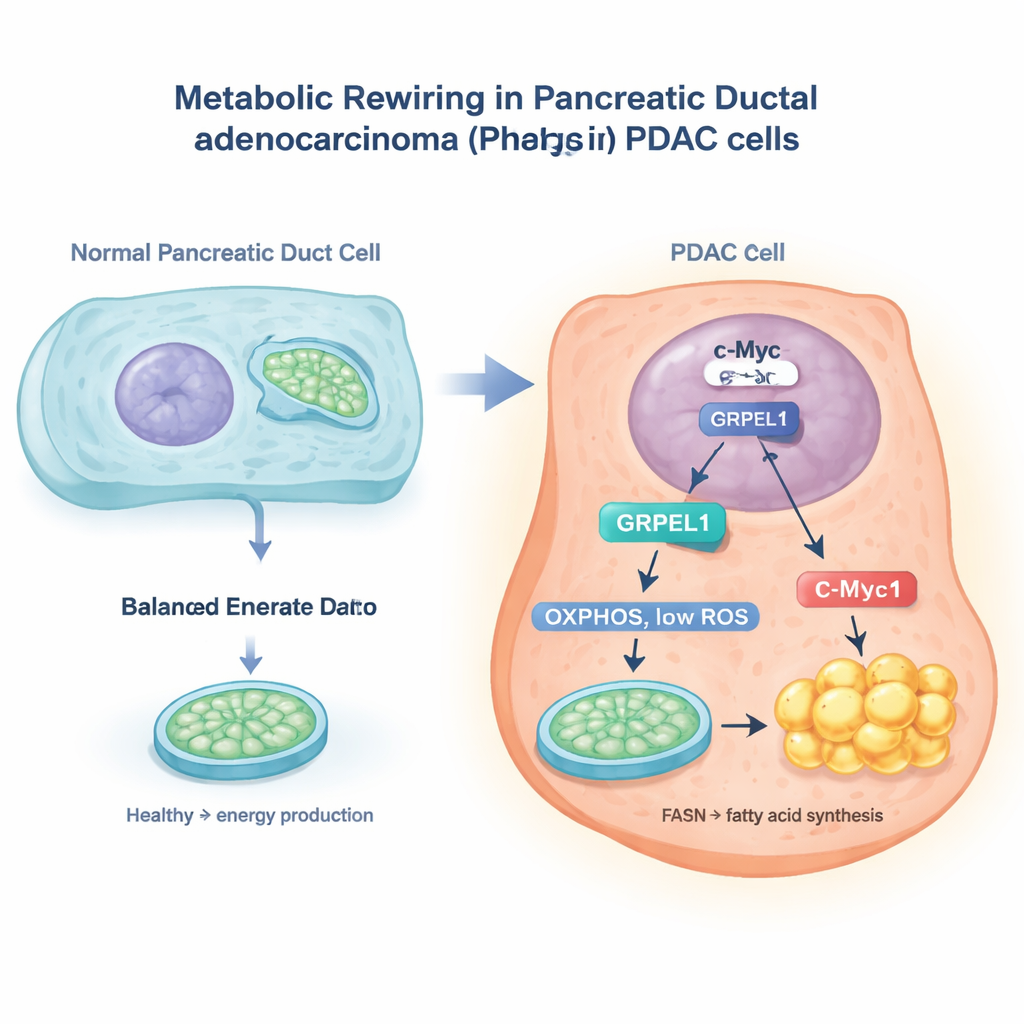
O interruptor c-Myc e um auxiliar mitocondrial
Os pesquisadores usaram grandes bancos de dados de câncer e experimentos em células de câncer pancreático para identificar uma proteína chamada GRPEL1, um auxiliar envolvido no manuseio de proteínas mitocondriais. Descobriram que um gene conhecido do câncer, c-Myc, age como um interruptor molecular no núcleo celular que ativa o gene GRPEL1. Quando os níveis de c-Myc foram reduzidos, os níveis de GRPEL1 caíram; quando c-Myc foi aumentado, GRPEL1 subiu. Amostras de tumores de pacientes também mostraram que c-Myc e GRPEL1 tendem a estar altos em conjunto, e ambos estavam ligados a piores desfechos. Em células de PDAC cultivadas em laboratório, reduzir GRPEL1 desacelerou a divisão celular e o crescimento de colônias, enquanto adicionar GRPEL1 extra ajudou as células a proliferar mais rapidamente, especialmente quando c-Myc estava bloqueado.
Das mitocôndrias à produção de gordura
Ao aprofundar, a equipe descobriu que GRPEL1 faz mais do que apenas manter as proteínas mitocondriais em ordem. Quando GRPEL1 foi depletado, as mitocôndrias nas células de PDAC ficaram menos eficientes na produção de energia, perderam sua forma normal e liberaram mais espécies reativas de oxigênio (ROS) — subprodutos quimicamente reativos às vezes chamados de “ferrugem” celular. Essa onda de ROS teve um efeito em cascata: reduziu os níveis da sintase de ácidos graxos (FASN), uma enzima-chave que constrói novos ácidos graxos dentro das células. Com FASN reduzida, as células produziram menos gorduras, armazenaram menos lipídios e seu crescimento diminuiu. Quando os pesquisadores eliminaram ROS com um antioxidante, os níveis de FASN retornaram, mostrando que a ligação GRPEL1–FASN é impulsionada por ROS. Curiosamente, o próprio c-Myc não pareceu ativar diretamente o gene FASN nesse sistema, mas influenciou FASN indiretamente por meio de GRPEL1 e do estresse mitocondrial.
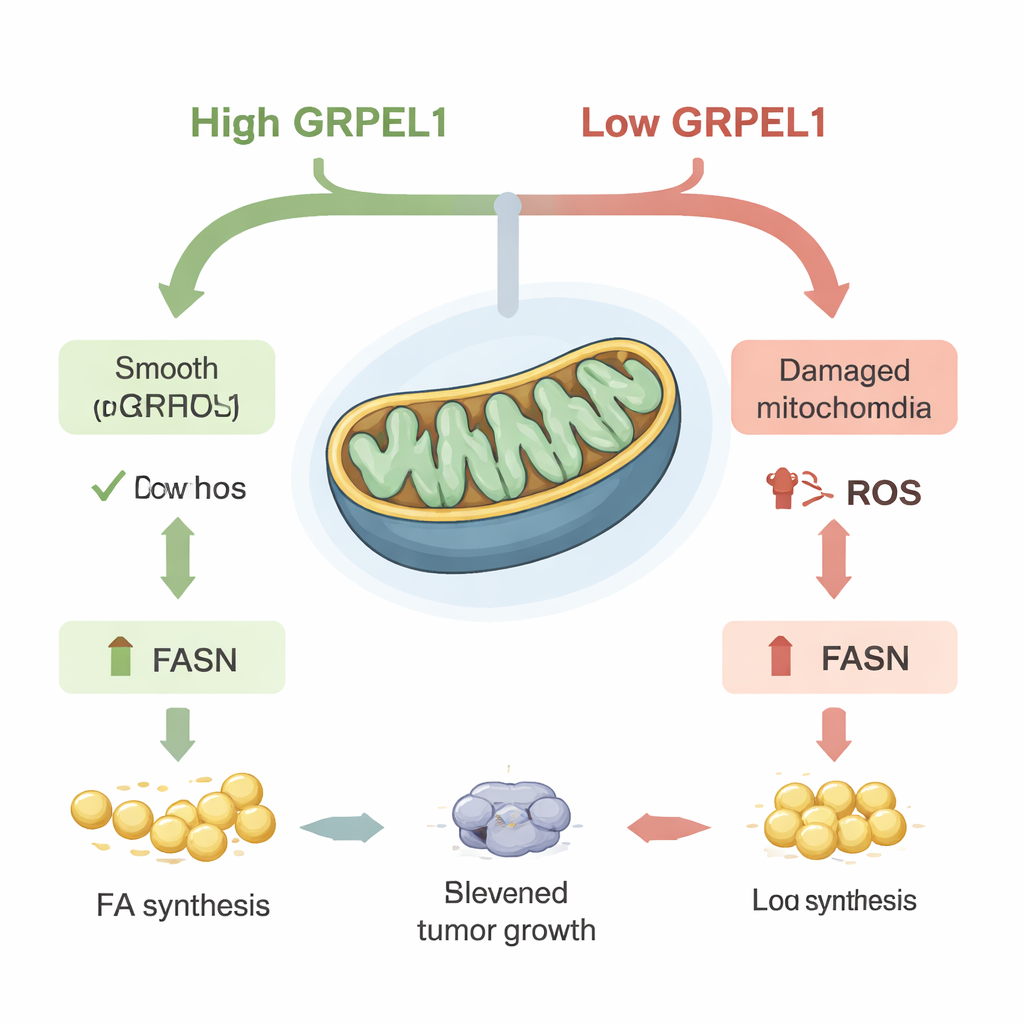
Gordura como combustível para o crescimento tumoral
Como a FASN está no centro da construção de gordura, os cientistas perguntaram se restaurá-la poderia resgatar o crescimento das células tumorais quando GRPEL1 estava baixo. Em culturas celulares, forçar as células a produzir mais FASN reverteu parcialmente a desaceleração do crescimento e da formação de colônias causada pela perda de GRPEL1. O mesmo aconteceu em camundongos: tumores formados por células com depleção de GRPEL1 cresceram mais lentamente, mas a reintrodução de FASN revitalizou tanto o tamanho do tumor quanto o conteúdo de gordura. Análises detalhadas de metabólitos e lipídios mostraram quedas amplas em muitas moléculas relacionadas a gorduras quando GRPEL1 ou c-Myc foram reduzidos. Importante, fornecer ácidos graxos extras ou uma mistura lipídica externamente restaurou parcialmente o crescimento tanto em linhagens celulares cancerígenas quanto em organoides pancreáticos derivados de pacientes — mini-tumores cultivados em 3D — sugerindo que o problema principal era a perda de gorduras recém-sintetizadas.
Transformando uma vulnerabilidade em terapia
No conjunto, o trabalho descreve uma imagem clara: no câncer pancreático, c-Myc aumenta GRPEL1, que ajuda as mitocôndrias a funcionar de forma suave e mantém o controle das ROS. Esse ambiente mitocondrial tranquilo permite que as células mantenham níveis elevados de FASN, produzindo novos ácidos graxos que servem como blocos de construção para membranas, armazenamento de energia e sinais de crescimento. Quando GRPEL1 é bloqueado, as mitocôndrias falham, as ROS sobem, a FASN cai e as células cancerígenas têm dificuldade para crescer — um efeito que pode ser parcialmente contornado se gorduras forem fornecidas externamente. Para leitores não especialistas, a conclusão é que os tumores pancreáticos dependem de um circuito interno de “fábrica de gordura”, impulsionado por c-Myc, GRPEL1 e FASN. Drogas que perturbem esse eixo de produção de ácidos graxos, especialmente em tumores onde ele está altamente ativo, podem oferecer uma nova forma promissora de privar as células de câncer pancreático, afetando menos os tecidos normais.
Citação: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Palavras-chave: câncer pancreático, metabolismo tumoral, síntese de ácidos graxos, mitocôndrias, c-Myc