Clear Sky Science · pt
BCL-xL como alvo terapêutico no câncer colorretal refratário a cetuximabe
Por que isso importa para pessoas com câncer de cólon
O câncer colorretal (cólon e reto) é um dos cânceres mais comuns no mundo, e muitos pacientes com doença avançada recebem um anticorpo dirigido chamado cetuximabe. Esse medicamento pode reduzir tumores inicialmente, mas na maioria dos pacientes o câncer encontra maneiras de escapar dentro de meses, deixando os médicos com poucas opções eficazes. Este estudo faz uma pergunta urgente: quando tumores de cólon deixam de responder ao cetuximabe, existe outro ponto fraco que novas drogas possam explorar para induzir a morte das células cancerígenas?
Quando um fármaco direcionado deixa de funcionar
O cetuximabe funciona bloqueando uma antena na superfície das células cancerosas chamada receptor do fator de crescimento epidérmico (EGFR), que ajuda a impulsionar seu crescimento. A equipe criou um modelo laboratorial de resistência expondo uma linha celular de câncer colorretal sensível (LIM1215) a doses crescentes de cetuximabe ao longo de seis meses. Surgiram duas populações celulares resistentes, obtidas de forma independente, que continuaram a crescer mesmo em níveis elevados do fármaco, mas pareciam igualmente saudáveis e com crescimento rápido como as células originais quando o medicamento era removido. Importante, as células resistentes ainda carregavam o alvo do fármaco em sua superfície e o cetuximabe ainda podia se ligar a ele, sugerindo que o câncer não havia simplesmente “escondido” ou alterado o receptor.
Células resistentes redirecionam seus sinais de crescimento
Para entender como as células contornavam o cetuximabe, os pesquisadores examinaram vias de crescimento chave dentro da célula. Nas células parentais, o cetuximabe normalmente atenuava a via MAPK, um motor principal da divisão celular. Nas células resistentes, a atividade da MAPK permaneceu alta mesmo quando o EGFR foi bloqueado, mostrando que o sinal de crescimento havia sido desacoplado do receptor original. O sequenciamento do RNA celular revelou novas mutações ativadoras em outro gene RAS, HRAS, em subpopulações das células resistentes, mas não em outros suspeitos habituais como KRAS, NRAS ou BRAF. Tentativas de desligar esse sinal redirecionado com um inibidor de MEK (que age a montante de RAS) reduziram o crescimento apenas modestamente. Isso enfatizou que, em vez de perseguir toda nova mutação, pode ser mais eficaz atacar a maquinaria celular de vida ou morte compartilhada entre diferentes clones resistentes. 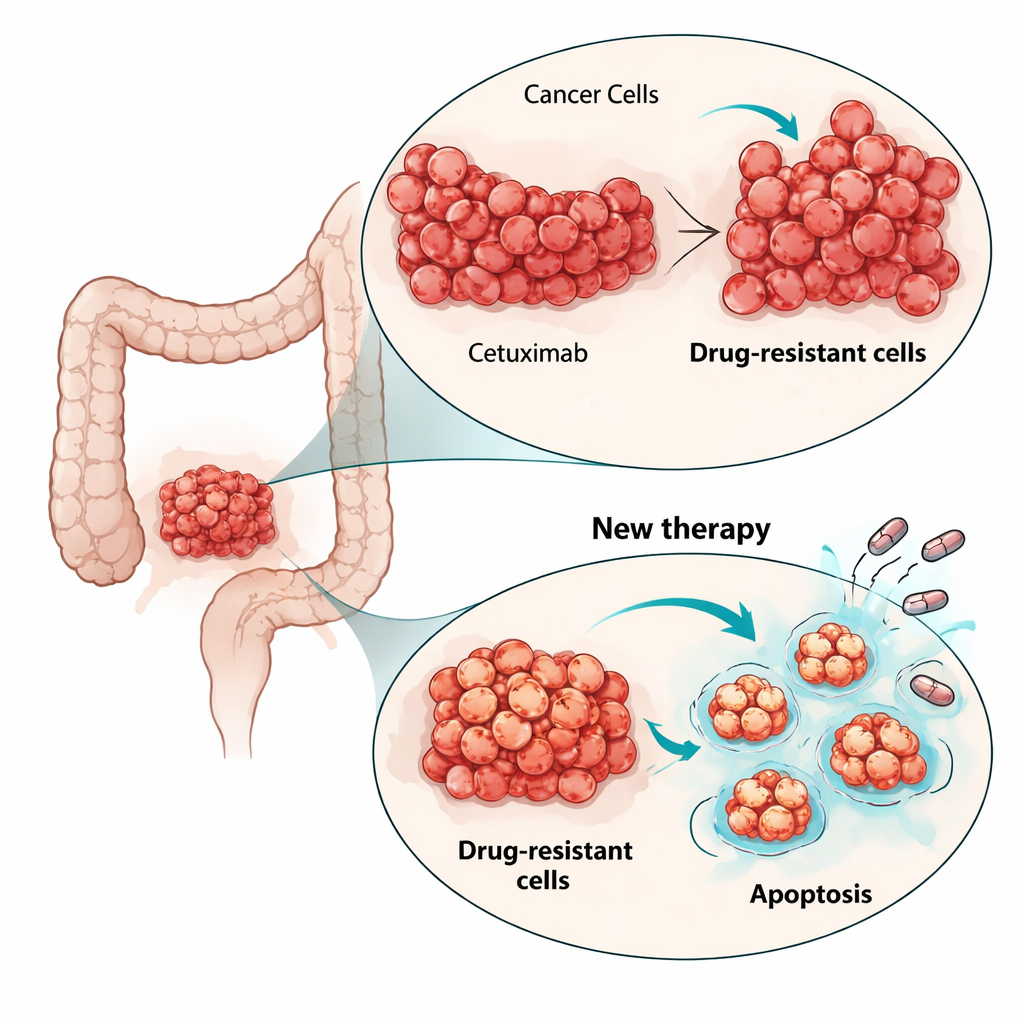
Atingindo o sistema de suporte vital do câncer
Os cientistas voltaram seu foco para a apoptose, o programa interno de suicídio celular que os cânceres frequentemente suprimem. A análise de expressão gênica mostrou que vias relacionadas à apoptose estavam alteradas nas células resistentes. Em particular, a proteína anti-morte BCL-xL estava mais alta em uma população resistente e moderadamente aumentada na outra, enquanto outra proteína de sobrevivência, MCL-1, também estava presente. A equipe testou pequenas moléculas chamadas miméticos BH3, projetadas para bloquear essas proteínas de sobrevivência e liberar a maquinaria da morte. Em culturas celulares bidimensionais, as três linhas celulares—parental e resistentes—eram sensíveis a drogas que bloqueavam BCL-xL ou MCL-1, mas, de forma marcante, doses mais baixas mataram as células resistentes ao cetuximabe com mais eficácia. Adicionar uma baixa dose do inibidor do proteassoma bortezomibe, que ajuda a acumular sinais pró-morte, aumentou ainda mais a letalidade, especialmente quando combinado com o bloqueador de MCL-1.
De placas planas a mini-tumores 3D e tecidos de pacientes
Como camadas celulares planas não reproduzem totalmente tumores no corpo, a equipe cultivou as células como esferoides tridimensionais embebidos em gel, refletindo melhor a arquitetura e os desafios de penetração de drogas de tumores reais. Novamente, bloquear BCL-xL ou MCL-1 reduziu a viabilidade dos esferoides, e combinar esses fármacos com bortezomibe causou quedas dramáticas na atividade metabólica e sinais claros de morte celular. Para testar se essa vulnerabilidade existe em material tumoral humano mais realista, eles usaram fatias finas de cânceres colorretais resistentes a cetuximabe cultivadas em camundongos a partir de tumores de pacientes (xenotransplantes derivados de pacientes). Esses modelos eram todos de tipo selvagem para KRAS, como as células LIM1215 originais, mas carregavam mutações adicionais diversas, incluindo em BRAF e TP53, espelhando a variedade genética observada na clínica. 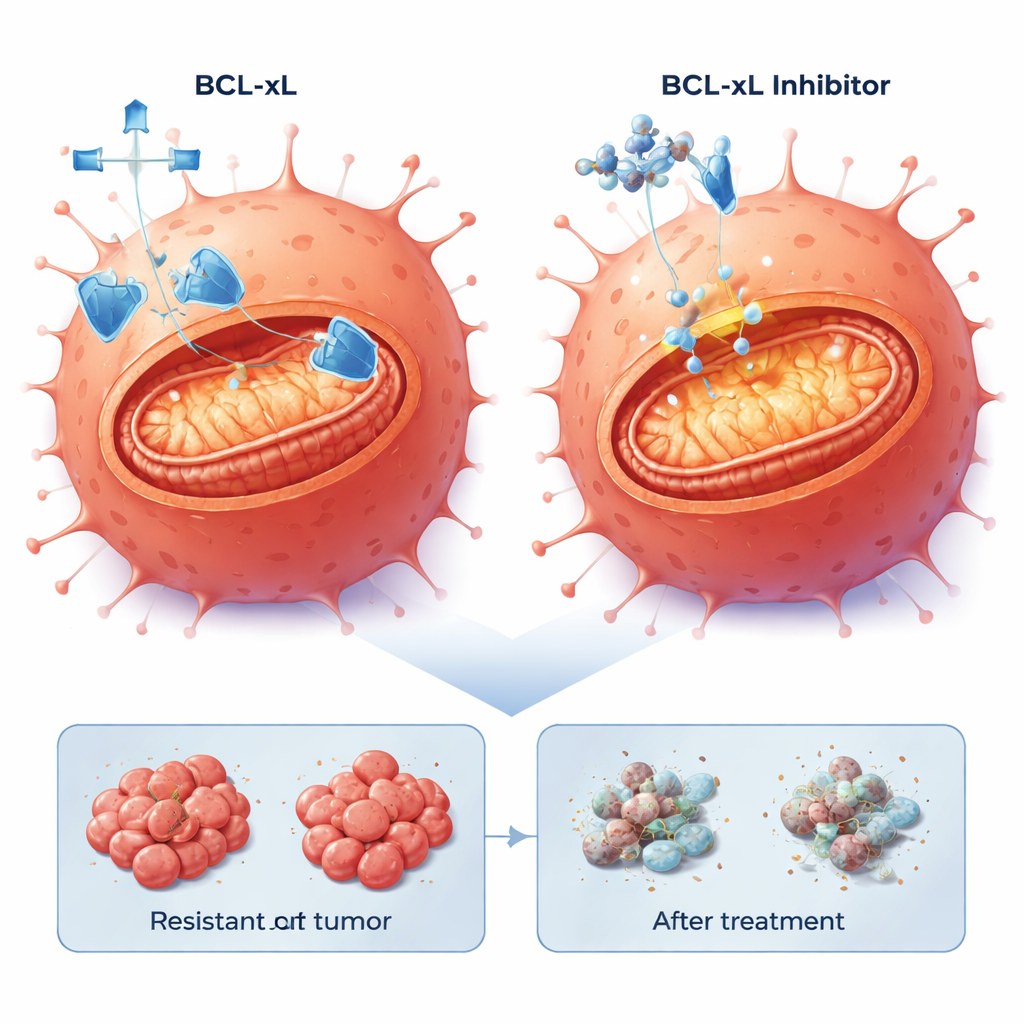
Alvo em BCL-xL funciona em tumores resistentes variados
Nessas fatias tumorais derivadas de pacientes, a combinação de um inibidor de BCL-xL com baixa dose de bortezomibe desencadeou de forma consistente morte celular robusta em 20–40% das células tumorais em quatro modelos diferentes, incluindo aqueles com mutações agressivas em BRAF. Em contraste, bloquear MCL-1 com bortezomibe produziu efeitos fortes apenas em um subconjunto de tumores. Importante, a capacidade das células resistentes de sofrer apoptose foi preservada: uma vez que a rede de segurança BCL-xL foi removida, o programa interno de morte ainda podia ser ativado, independentemente da rota genética específica que o tumor havia adotado para escapar do cetuximabe.
O que isso significa para pacientes
Para pessoas cujo câncer colorretal para de responder ao cetuximabe, este estudo oferece um otimismo cauteloso. Sugere que, mesmo depois que tumores se tornam resistentes à terapia dirigida ao EGFR, muitas células cancerosas permanecem prontas para morrer se uma proteína de sobrevivência chave, BCL-xL, for bloqueada. Embora inibidores de BCL-xL possam ter efeitos colaterais, especialmente nas plaquetas sanguíneas, o trabalho aponta para estratégias de combinação e otimização de dose que poderiam limitar a toxicidade enquanto exploram um calcanhar de Aquiles compartilhado de tumores de difícil tratamento. No futuro, drogas que desarmem o BCL-xL podem formar a espinha dorsal de novos tratamentos de segunda linha para câncer colorretal refratário a cetuximabe, menos dependentes da paisagem mutacional em constante mudança do tumor.
Citação: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Palavras-chave: câncer colorretal, resistência a fármacos, cetuximabe, inibição de BCL-xL, apoptose