Clear Sky Science · pt
LAP2α impulsiona a tumorigenese mamária ao reduzir o estresse de replicação
Por que isso importa para o câncer de mama
Os tumores mamários crescem em parte porque as células cancerosas encontram formas de sobreviver ao estresse constante enquanto copiam seu DNA. Este estudo revela como uma proteína menos conhecida, chamada LAP2α, ajuda as células de câncer de mama a proteger seu DNA durante a replicação, favorecendo assim o crescimento tumoral e tornando os cânceres mais difíceis de tratar. Compreender esse sistema de apoio oculto sugere novas maneiras de enfraquecer tumores e melhorar os efeitos de medicamentos já existentes.
Um ajudante oculto dentro dos núcleos das células tumorais
Cada vez que uma célula se divide, ela precisa copiar seu DNA com precisão. Nas células cancerosas, esse processo sofre tensão extra: sinais de crescimento ficam permanentemente “ligados” e a maquinaria de replicação é levada ao limite. Essa pressão, conhecida como estresse de replicação, deixa trechos de DNA de fita simples que precisam ser rapidamente recobertos e estabilizados por um complexo proteico chamado RPA. Os autores já haviam descoberto que LAP2α, uma proteína ligada à estrutura interna do núcleo, pode se ligar à RPA e ajudá-la a alcançar o DNA danificado. No trabalho atual, eles investigaram se essa parceria LAP2α–RPA realmente alimenta o desenvolvimento do tumor mamário e afeta a resposta dos tumores ao tratamento.
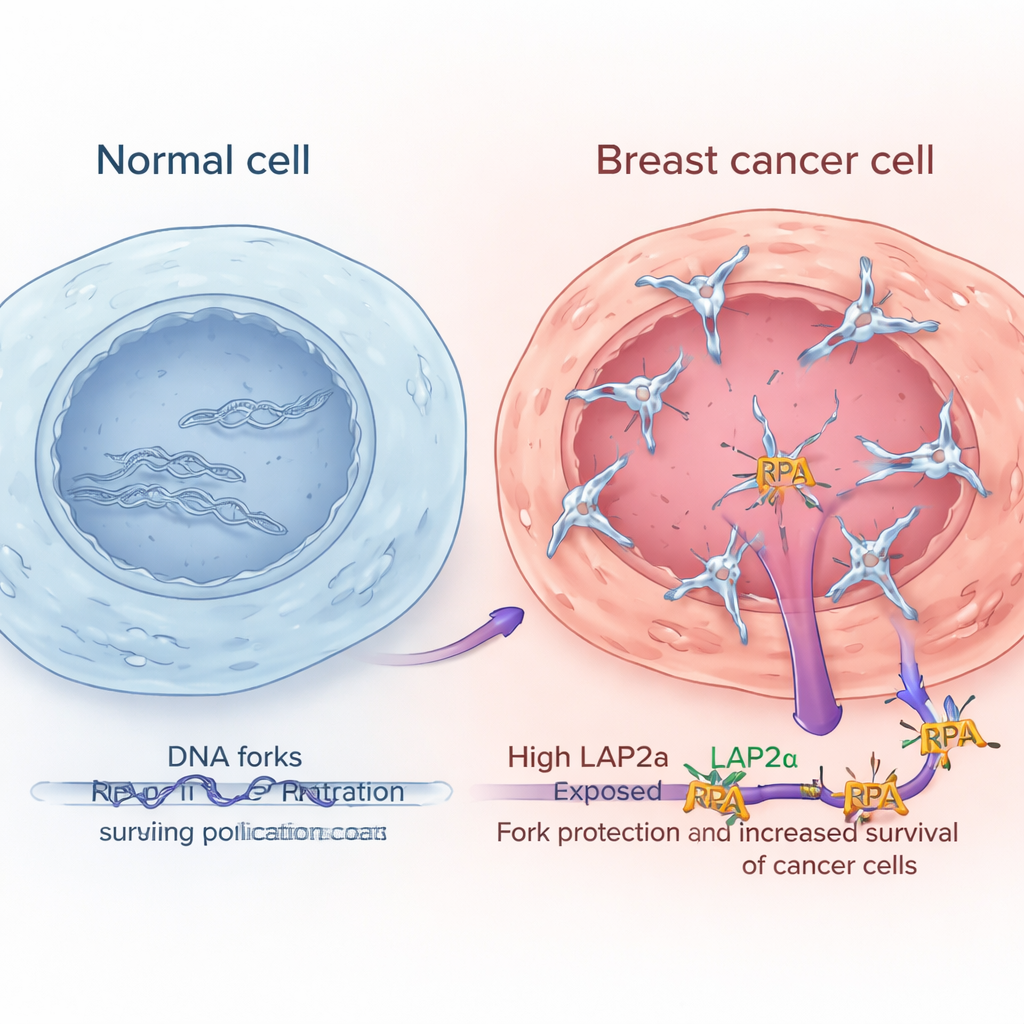
Altos níveis de LAP2α sinalizam tumores mamários mais agressivos
Analisando grandes conjuntos públicos de expressão gênica e examinando amostras tumorais ao microscópio, os pesquisadores mostraram que LAP2α é consistentemente mais alto em tecido de câncer de mama do que no tecido mamário normal adjacente. Seus níveis aumentam com o grau tumoral, ou seja, cânceres mais anormais e agressivos tendem a apresentar mais LAP2α. Esse padrão apareceu em múltiplos subtipos principais de câncer de mama, incluindo tumores com receptores hormonais positivos, enriquecidos por HER2 e triplo negativos. Importante para os pacientes, aqueles cujos tumores apresentavam altos níveis de LAP2α tendiam a ter pior sobrevida. Em contraste, os componentes principais do RPA em si não mostraram mudanças semelhantes nem associações claras com o desfecho, sugerindo que é a função reforçada de LAP2α — e não simplesmente mais RPA — que ajuda as células cancerosas a lidar melhor com o estresse de replicação.
Desligar LAP2α desacelera tumores e expõe pontos fracos
Para ir além das correlações, a equipe usou modelos de camundongos com câncer de mama nos quais LAP2α podia ser removida seletivamente. Uma vez formados os tumores mamários, a deleção genética de LAP2α fez com que os tumores crescessem mais devagar e prolongou a sobrevida dos animais. Células tumorais sem LAP2α dividiram-se menos e apresentaram mais sinais de dano ao DNA, demonstrados pelo aumento da marcação para marcadores de quebras de DNA e pela redução do recobrimento de RPA sobre o DNA. Quando essas células tumorais deficientes em LAP2α foram transplantadas em novos camundongos, novamente formaram tumores menores e mostraram maior sensibilidade à quimioterapia que causa dano ao DNA, incluindo o agente de platina cisplatina e um inibidor de PARP. Experimentos semelhantes em linhagens humanas de câncer de mama confirmaram que reduzir LAP2α tornava as células mais vulneráveis a vários fármacos genotóxicos, enquanto restaurar o LAP2α normal — mas não uma forma mutante incapaz de se ligar à RPA — resgatava tanto a proteção do DNA quanto a resistência ao medicamento.
Como LAP2α ajuda a proteger fitas de DNA frágeis
Para dissecar o mecanismo, os pesquisadores recriaram as etapas de ligação ao DNA em ensaios in vitro. Misturaram RPA purificado, DNA de fita simples e ou LAP2α normal ou uma variante incapaz de interagir com RPA. Descobriram que LAP2α aumentava diretamente a eficiência com que a RPA recobria o DNA de fita simples e ajudava a RPA a estender e estabilizar essas regiões frágeis, atuando muito como um auxiliar de carregamento ou chaperona. Quando o DNA estava presente, a RPA tendia a se desprender de LAP2α e se comprometer completamente a ligar-se à fita simples, mostrando que LAP2α não faz parte do revestimento protetor final, mas sim entrega a RPA ao DNA. Na ausência de uma interação funcional LAP2α–RPA, mais forquilhas de replicação colapsavam, quebras de DNA se acumulavam e as células cancerosas tinham maior probabilidade de morrer, especialmente quando danos adicionais eram induzidos por quimioterapia.
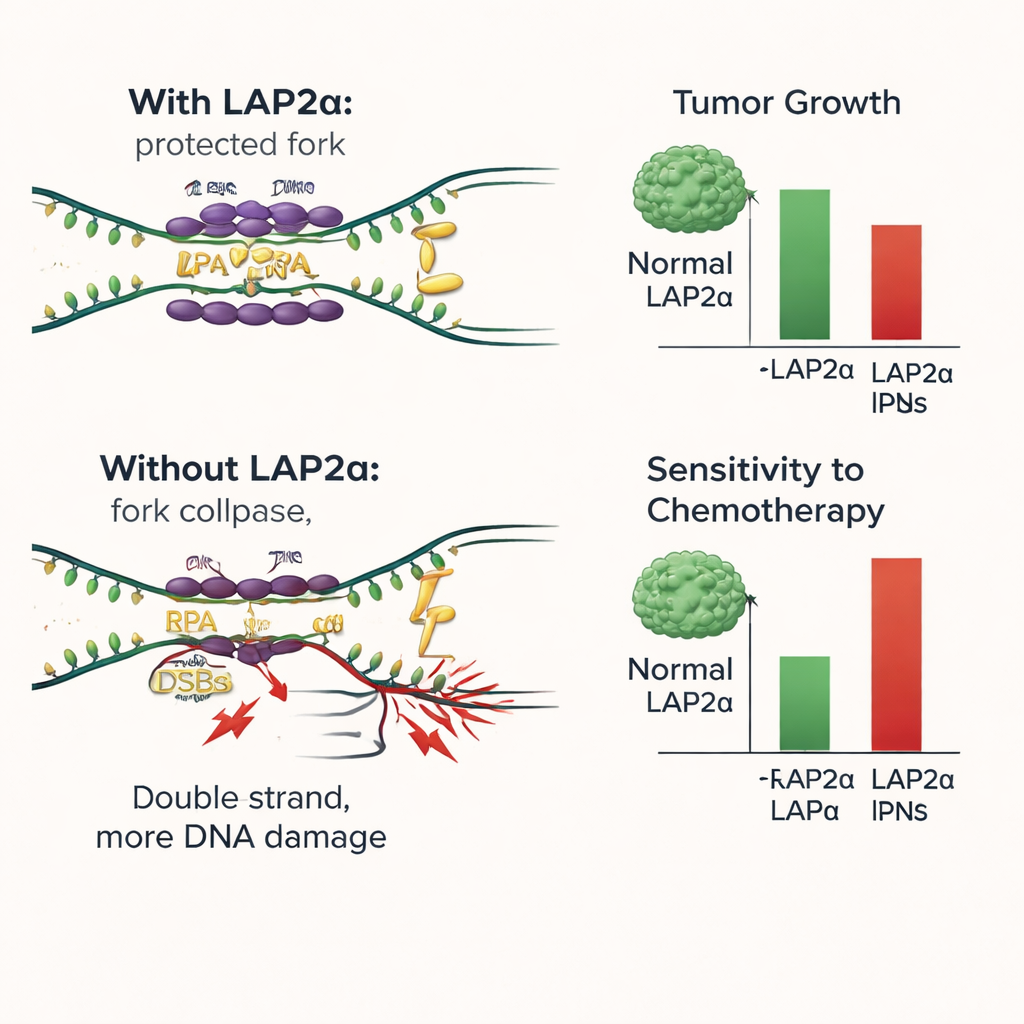
O que isso significa para o futuro do tratamento do câncer de mama
Em termos simples, este estudo mostra que LAP2α funciona como um assistente nos bastidores que ajuda as células de câncer de mama a sobreviver ao esforço de copiar seu DNA. Ao carregar eficientemente a RPA sobre o DNA vulnerável, LAP2α reduz danos e sustenta o crescimento tumoral contínuo. Remover ou desativar LAP2α desequilibra a balança: o dano ao DNA se acumula, as células param de se dividir e medicamentos convencionais que atacam o DNA tornam-se mais eficazes. Esses achados sugerem que LAP2α poderia ser usado como marcador de pior prognóstico e como um novo alvo terapêutico. Fármacos que bloqueiem LAP2α ou sua interação com a RPA podem tornar tratamentos existentes, como agentes de platina e inibidores de PARP, mais eficazes, especialmente em tumores que dependem fortemente desse sistema de amortecimento do estresse.
Citação: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Palavras-chave: câncer de mama, estresse da replicação do DNA, LAP2 alfa, proteína de replicação A, sensibilidade à quimioterapia