Clear Sky Science · pt
Apontar a biossíntese de glicero-fosfolipídios supera a quimiorresistência induzida pela perda de SLFN11 no sarcoma de Ewing
Por que esta pesquisa importa para o câncer infantil
O sarcoma de Ewing é um câncer raro, porém agressivo, que atinge principalmente crianças e adolescentes. Muitos pacientes respondem bem à quimioterapia inicialmente, mas quando o câncer volta, os tratamentos atuais frequentemente falham. Este estudo investiga uma pergunta urgente: quando células do sarcoma de Ewing desenvolvem resistência à quimioterapia, quais mudanças internas as ajudam a sobreviver — e essas mudanças podem se transformar em novas vulnerabilidades que os médicos possam explorar?
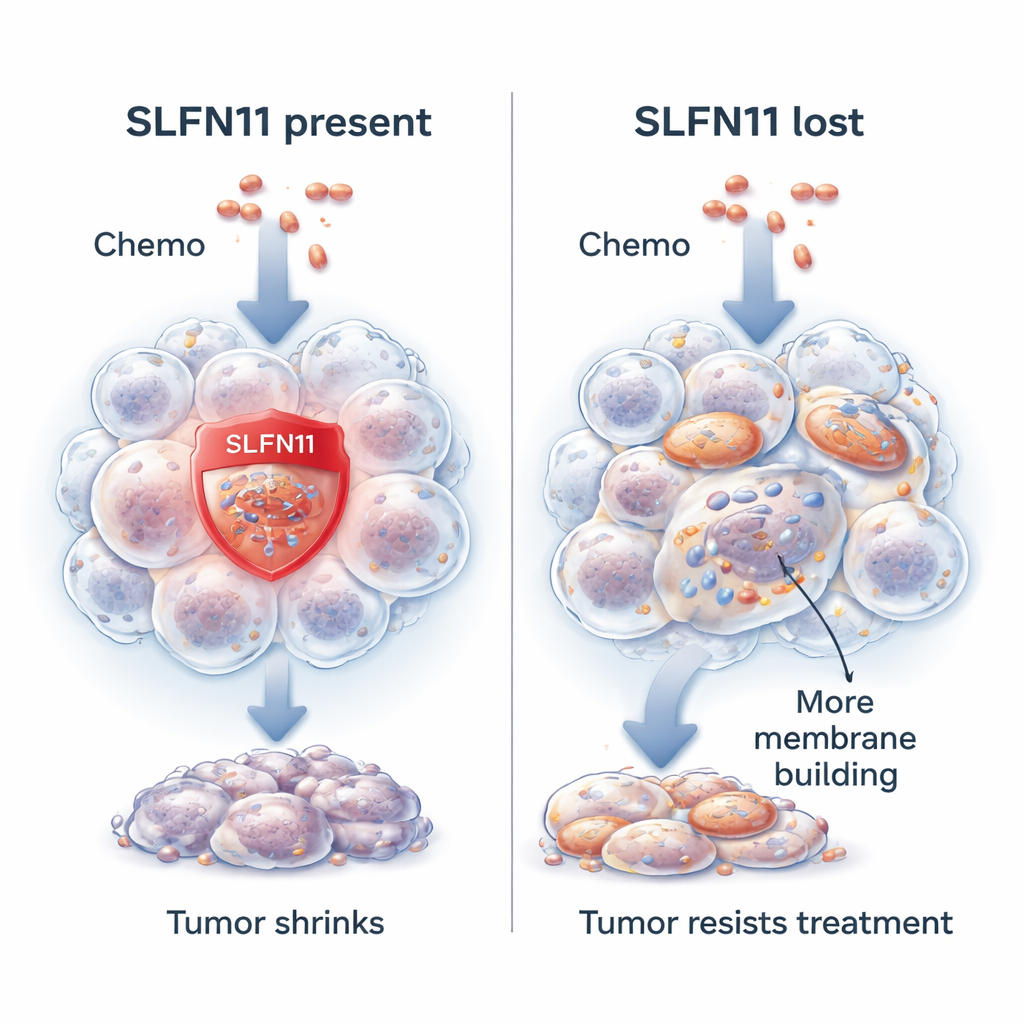
Um gene que torna as células cancerígenas mais fáceis de matar
Os pesquisadores concentram-se em um gene chamado SLFN11. Em muitos tumores de sarcoma de Ewing, o SLFN11 é altamente ativo e torna as células cancerígenas muito mais sensíveis a drogas que danificam o DNA, o material genético da célula. Quando esses medicamentos são administrados, o SLFN11 ajuda a interromper o reparo do DNA e empurra a célula cancerígena na direção da morte. Pacientes cujos tumores apresentam níveis mais altos de SLFN11 tendem a viver mais e a responder melhor ao tratamento. No entanto, cerca de um em cada dez tumores apresenta desde o início pouco ou nenhum SLFN11, ou perde esse gene ao longo da terapia. Quando isso ocorre, a mesma quimioterapia torna-se muito menos eficaz, embora as células cancerígenas continuem perfeitamente capazes de crescer.
Como as células cancerosas recompõem o uso de combustível e gorduras
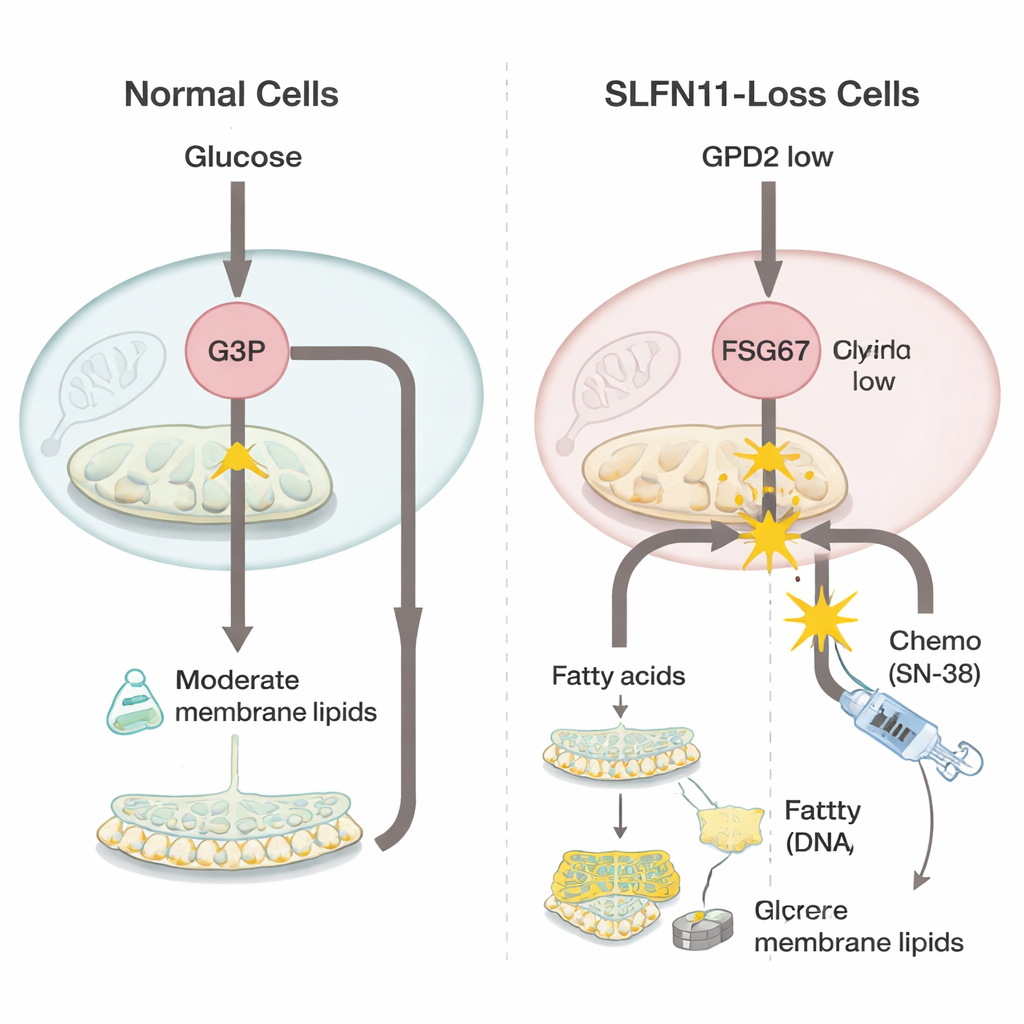
Para entender o que muda quando o SLFN11 é perdido, a equipe comparou células de sarcoma de Ewing com e sem esse gene usando ferramentas “ômicas” potentes que medem milhares de genes e pequenas moléculas simultaneamente. Eles descobriram que células sem SLFN11 reduzem a atividade de uma enzima nas mitocôndrias chamada GPD2, que normalmente ajuda a oxidar uma molécula chamada glicerol‑3‑fosfato como parte da produção de energia. Quando a GPD2 está reduzida, o glicerol‑3‑fosfato se acumula. Em vez de ser desperdiçado, esse bloco de construção extra é desviado para produzir mais moléculas gordurosas que formam as membranas celulares, um grupo conhecido como glicero‑fosfolipídios. As células também apresentaram sinais de produzir gorduras mais flexíveis e insaturadas, o que pode ajudar tumores de crescimento rápido a se adaptar ao estresse.
Transformando um truque de sobrevivência em ponto fraco
Porque essas células deficientes em SLFN11 dependem mais da construção de membranas, os cientistas testaram se bloquear esse processo poderia restaurar a sensibilidade à quimioterapia. Eles usaram um composto chamado FSG67, que inibe uma etapa chave na produção de glicero‑fosfolipídios. Sozinho, o agente padrão que danifica o DNA, SN‑38, havia se tornado muito menos potente em células deficientes em SLFN11, espelhando o problema clínico da resistência. Mas quando SN‑38 foi combinado com FSG67, as células antes resistentes foram atingidas com muito mais força, e os dois fármacos atuaram de forma cooperativa, melhor do que o esperado a partir de seus efeitos individuais. Em contraste, em células que ainda expressavam SLFN11 e já eram altamente sensíveis ao SN‑38, adicionar FSG67 trouxe pouco benefício adicional e poderia até ser ligeiramente contraprodutivo. Esse padrão sugere que a dependência recém‑adquirida de produção de gorduras e membranas é específica ao estado resistente e de baixos níveis de SLFN11.
Um possível sinal não invasivo de tumores de difícil tratamento
Os pesquisadores então perguntaram se essa reprogramação metabólica poderia ser detectada em tumores reais, não apenas em células em cultura. Eles cultivaram tumores de sarcoma de Ewing em camundongos, com e sem SLFN11, e usaram ressonância magnética nuclear (RMN) para examinar a composição química dos extratos tumorais. Tumores sem SLFN11 mostraram uma proporção mais alta de duas moléculas contendo colina relacionadas ao turnover de membrana: fosfocolina e glicerofosfocolina. Uma alta razão fosfocolina/glicerofosfocolina tem sido associada em outros cânceres a comportamento mais agressivo e pior resposta ao tratamento. Como sinais de colina podem ser medidos com técnicas avançadas de imagem, esse tipo de alteração pode, no futuro, servir como marcador não invasivo para identificar tumores de sarcoma de Ewing que adotaram esse modo resistente de construção de membranas.
O que isso pode significar para tratamentos futuros
No conjunto, o estudo mostra que quando células do sarcoma de Ewing perdem SLFN11 e se tornam menos sensíveis à quimioterapia que danifica o DNA, elas compensam reprogramando seu metabolismo para produzir mais lipídios de membrana. Essa mudança não apenas ajuda as células a sobreviver; também cria um novo calcanhar de Aquiles. Bloquear a produção de glicero‑fosfolipídios com um fármaco como o FSG67 pode restaurar parcialmente o poder letal da quimioterapia nessas células resistentes. Embora o FSG67 em si ainda não seja um medicamento clínico, o trabalho aponta para uma estratégia em que, um dia, os médicos possam combinar o status de SLFN11 e características metabólicas dos tumores dos pacientes, e então associar terapias que danificam o DNA a inibidores direcionados da síntese de gorduras e membranas para superar a resistência.
Citação: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Palavras-chave: Sarcoma de Ewing, quimiorresistência, SLFN11, metabolismo do câncer, biossíntese de lipídios