Clear Sky Science · pt
Mirar a IGFBP2 exossomal hipóxica supera a evasão imune mediada por CD47 em glioblastoma
Por que privar tumores de oxigênio pode sair pela culatra
Há muito tempo os médicos sabem que o glioblastoma, um câncer cerebral letal, frequentemente cresce em regiões pobres em oxigênio. Esses bolsões hipóxicos tornam o tumor mais difícil de tratar. Este estudo revela como o baixo oxigênio ajuda as células cancerosas a se esconderem do sistema imunológico e sugere uma nova combinação de tratamentos que pode torná‑las mais vulneráveis ao ataque do organismo.
Um tumor cerebral letal que dribla nossas defesas
O glioblastoma é o tumor cerebral mais agressivo e comum em adultos, com sobrevivência típica medida em meses. Embora células imunes infiltram esses tumores, as células cancerosas frequentemente escapam da destruição. Uma rota importante de fuga é uma proteína de superfície chamada CD47, às vezes chamada de sinal de “não me coma”, que instrui células imunes próximas, como macrófagos, a não engolirem e destruírem a célula tumoral. Drogas que bloqueiam o CD47 já estão em teste, mas os resultados em tumores sólidos como o glioblastoma têm sido variados, sugerindo que outros fatores no microambiente tumoral podem estar minando essas terapias.
Zonas hipóxicas e pequenos pacotes cancerígenos
Usando sequenciamento de RNA de célula única, os pesquisadores mapearam milhares de células de diferentes regiões de amostras de glioblastoma, comparando o núcleo de baixa oxigenação do tumor com sua borda externa. Eles encontraram um subtipo de célula particularmente agressivo no núcleo hipóxico, chamado de células GBM com características mesenquimais, que expressava fortemente CD47 e uma proteína chamada IGFBP2. Ao mesmo tempo, descobriram que essas células centrais liberavam um grande número de vesículas nanométricas conhecidas como exossomos, que carregavam IGFBP2 em sua superfície. Como os exossomos podem viajar pelo cérebro e até entrar na corrente sanguínea, eles podem espalhar sinais muito além de onde foram produzidos. 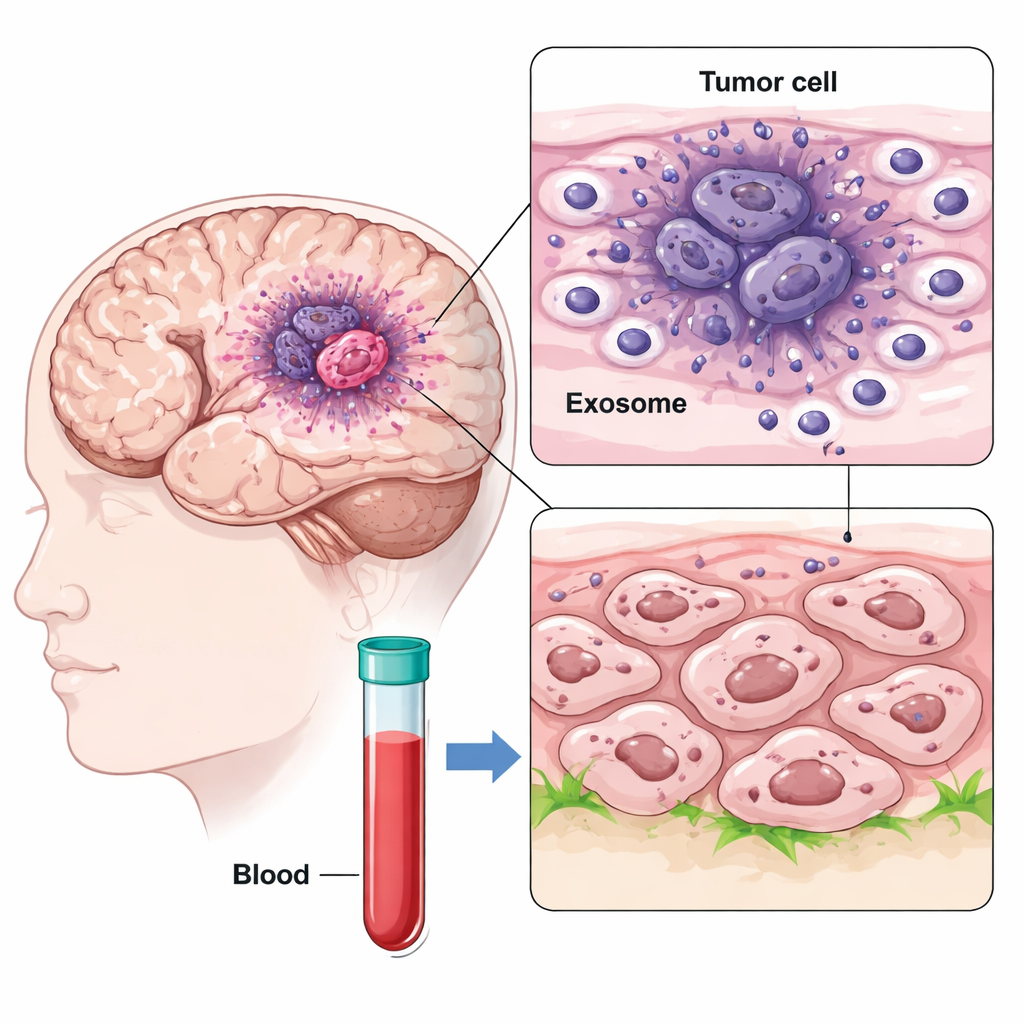
Como uma proteína parceira reforça o sinal de “não me coma”
O grupo então investigou o que a IGFBP2 estava fazendo. Mostraram que, sob baixo oxigênio, uma proteína sensor de hipóxia chamada HIF‑2α ativa o gene IGFBP2 nas células tumorais. A IGFBP2 então se liga a receptores específicos chamados integrinas na superfície dos exossomos, decorando a membrana externa. Quando esses exossomos revestidos por IGFBP2 se fundem com outras células tumorais, eles ativam uma cascata de sinais dentro da célula envolvendo proteínas conhecidas como FAK e STAT3. Essa cascata aumenta, em última instância, a quantidade de CD47 na superfície da célula tumoral, fortalecendo a mensagem de “não me coma” aos macrófagos e protegendo ainda mais as células cancerosas do ataque imune. 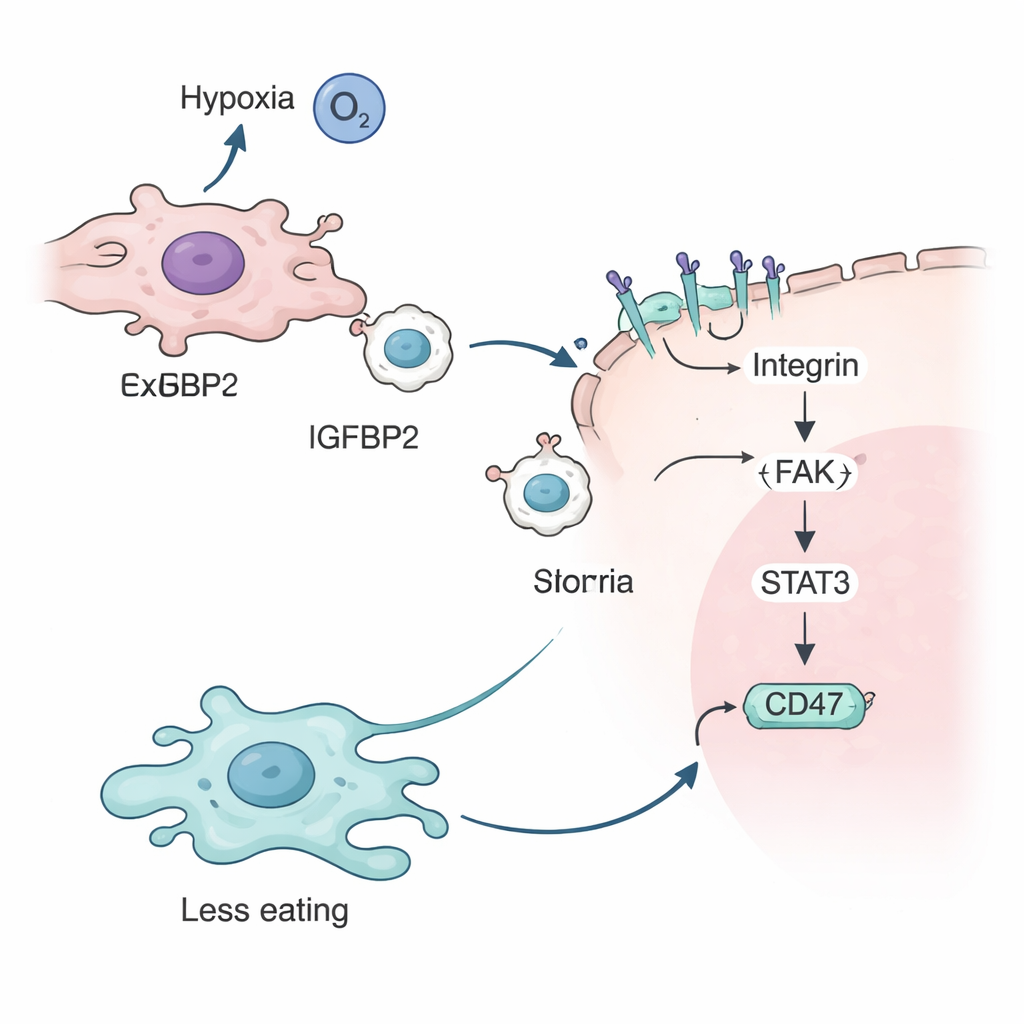
Evidências em amostras de pacientes e modelos animais
Para conectar essas descobertas de laboratório à doença real, os pesquisadores examinaram tecido tumoral e sangue de pessoas com glioma. Eles encontraram níveis mais altos de IGFBP2 tanto em tumores quanto em exossomos sanguíneos de pacientes com doença mais avançada, sugerindo que exossomos positivos para IGFBP2 poderiam servir como marcador sanguíneo do grau tumoral. Em modelos de camundongo, reduzir a IGFBP2 em células de glioblastoma as tornou mais vulneráveis a serem engolidas por macrófagos, retardou o crescimento tumoral e prolongou a sobrevivência. Por outro lado, adicionar exossomos ricos em IGFBP2 aumentou os níveis de CD47, reduziu a fagocitose por células imunes e acelerou a progressão tumoral.
Uma combinação terapêutica promissora
Por fim, a equipe testou se bloquear a IGFBP2 poderia tornar a terapia direcionada a CD47 mais eficaz. Em camundongos com tumores cerebrais, o tratamento com anticorpos contra IGFBP2 e CD47 levou a uma atividade maior dos macrófagos, tumores menores e sobrevida mais longa do que qualquer tratamento isolado. Ao cortar o sinal da IGFBP2 induzido pela hipóxia e bloquear diretamente o sinal de “não me coma” do CD47, essa terapia combinada atacou a camuflagem imune do tumor em duas frentes. Para pacientes, esses achados sugerem que medir IGFBP2 em exossomos sanguíneos pode ajudar a identificar aqueles com maior probabilidade de se beneficiar da imunoterapia baseada em CD47, e que combinar inibidores de IGFBP2 e CD47 pode ser uma estratégia mais poderosa contra o glioblastoma do que cada droga isoladamente.
Citação: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Palavras-chave: glioblastoma, exossomos, evasão imune, CD47, hipóxia