Clear Sky Science · pt
HSPA5 promove a estabilidade de YAP/TAZ independentemente da via Hippo e induz transição proneural‑para‑mesenquimal em glioblastoma
Por que este estudo sobre câncer cerebral importa
O glioblastoma é um dos cânceres cerebrais mais letais, em parte porque muitos tumores mudam com o tempo para um estado mais resistente ao tratamento. Este estudo revela como uma proteína comum da resposta ao estresse, HSPA5, ajuda a impulsionar essa mudança e mantém moléculas que promovem o tumor ativas por mais tempo do que deveriam. Entender esse “truque de sobrevivência” sugere novas maneiras de tornar o glioblastoma menos agressivo e mais sensível às terapias existentes.
Um tumor que muda de personalidade
Médicos e cientistas hoje reconhecem que o glioblastoma não é uma doença única, mas uma mistura de subtipos moleculares. Dois perfis principais são a forma “proneural”, que tende a ser um pouco menos agressiva, e a forma “mesenquimal”, que é mais invasiva, resistente ao tratamento e associada a recidiva precoce. Os tumores podem evoluir do estado proneural para o mesenquimal, um processo que os autores chamam de transição proneural‑para‑mesenquimal, ou PMT. A equipe buscou descobrir quais proteínas da resposta ao estresse poderiam estar empurrando os tumores por esse caminho perigoso.
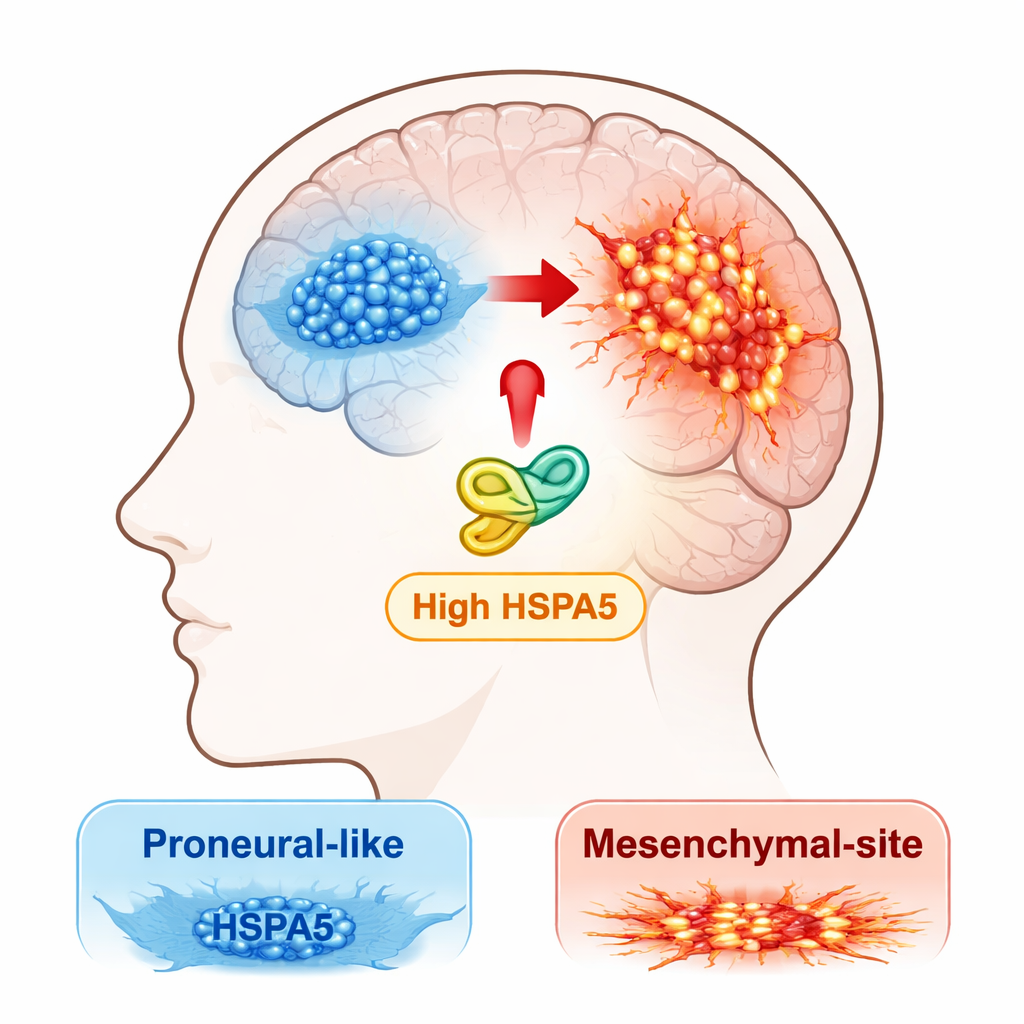
Uma proteína auxiliar de estresse em foco
Os pesquisadores começaram vasculhando grandes conjuntos de dados públicos sobre câncer e suas próprias amostras de pacientes em busca de membros da família HSP70, um grupo de proteínas “chaperonas” que ajudam outras proteínas a dobrar corretamente e a sobreviver sob estresse. Uma chaperona, HSPA5, destacou‑se. Sua atividade foi mais alta no subtipo mesenquimal do glioblastoma e consideravelmente maior em tumores do que no tecido cerebral normal. Pacientes cujos tumores apresentavam mais HSPA5 tendiam a ter sobrevida global pior, o que a aponta como um potencial condutor da doença agressiva, em vez de um espectador passivo.
Forçando células a se tornarem mais agressivas
Para explorar o que HSPA5 realmente faz dentro das células tumorais, a equipe cultivou células primárias de glioblastoma retiradas diretamente de pacientes e as separou em grupos com perfil proneural‑like e mesenquimal‑like. Quando forçaram células proneural a produzir HSPA5 em excesso, essas células passaram a se comportar mais como mesenquimais: dividiram‑se mais rápido, migraram e invadiram com mais facilidade e ativaram marcadores mesenquimais característicos como CD44 e c‑MET, ao mesmo tempo em que reduziram marcadores proneurais como SOX2 e OLIG2. O inverso também ocorreu — reduzir níveis de HSPA5 em células mesenquimais diminuiu seu crescimento e invasividade e parcialmente as empurrou de volta a um perfil menos agressivo.
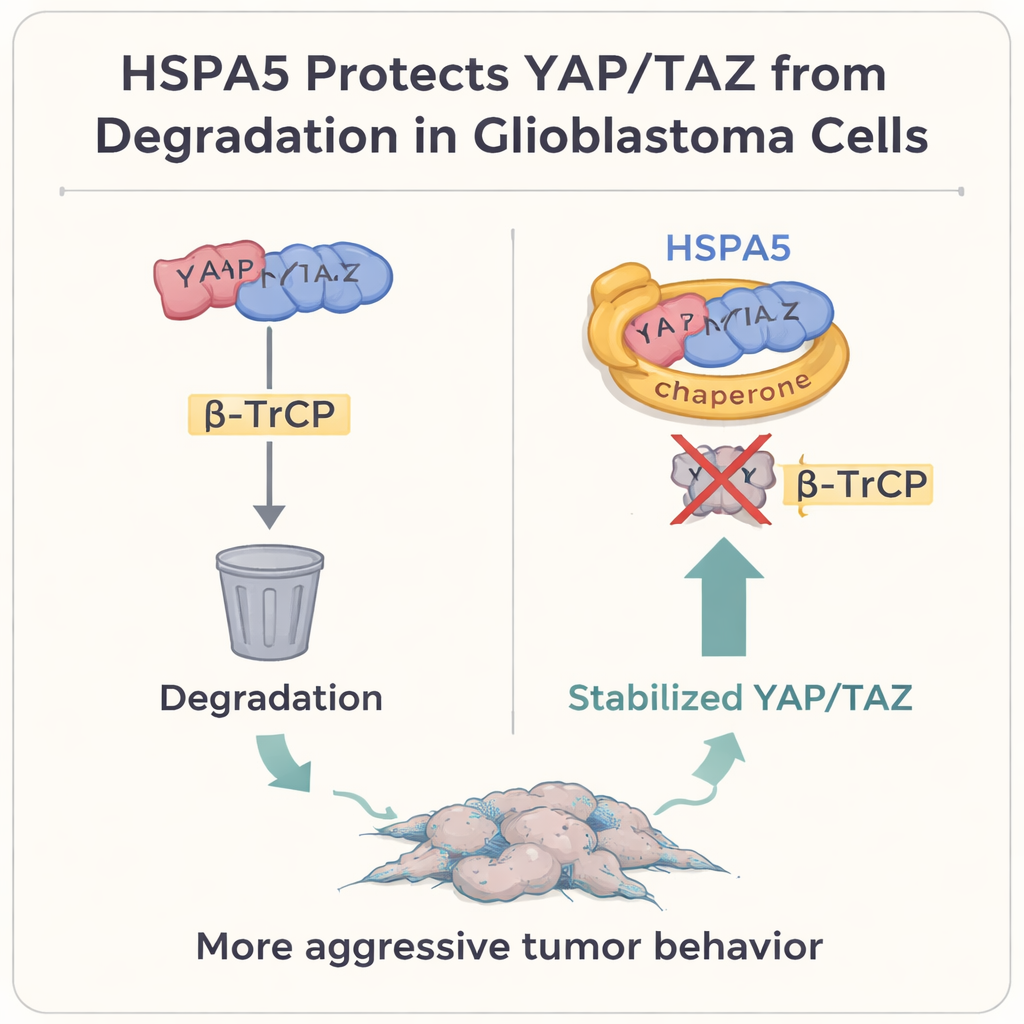
Protegendo chaves de crescimento do “lixo” celular
Aprofundando, os autores focaram em dois poderosos reguladores de crescimento, YAP e TAZ, que estão no centro da via de sinalização Hippo. Em muitos tumores sólidos, incluindo o glioblastoma, essas proteínas atuam como interruptores mestres que promovem crescimento celular, plasticidade e o estado mesenquimal. Normalmente, quando as células querem conter esse programa, elas marcam YAP e TAZ para destruição por meio de uma proteína chamada β‑TrCP, que os escolta até a “lixeira” da célula, o proteassoma. O estudo mostra que HSPA5 se liga fisicamente a YAP e TAZ, usando seu domínio de ligação a substrato como uma luva protetora. Ao fazer isso, impede que β‑TrCP se fixe, evita que YAP/TAZ sejam ubiquitinados e degradados, e permite que se acumulem no núcleo, onde ativam genes mesenquimais, incluindo CD44 e c‑MET.
De placas e camundongos a tumores de pacientes
A equipe confirmou esse mecanismo de várias formas. Bloquear HSPA5 fez com que as proteínas YAP e TAZ desaparecessem mais rápido, a menos que o proteassoma fosse quimicamente inibido, e aumentou os sinais de marcação para descarte sobre elas. Reativar YAP e TAZ resgatou a perda de crescimento e invasão observada quando HSPA5 foi reduzida, enquanto silenciar YAP/TAZ eliminou os efeitos pró‑tumorais da superexpressão de HSPA5. Em modelos de camundongos nos quais células humanas de glioblastoma foram implantadas no cérebro, tumores com alta expressão de HSPA5 cresceram mais e mataram os animais mais rápido; reduzir HSPA5, ou interromper seu suporte a YAP/TAZ, retardou o crescimento e estendeu a sobrevida. Finalmente, em amostras humanas pareadas coletadas dos mesmos pacientes antes e após a recidiva, os tumores recorrentes, mais mesenquimais, mostraram níveis mais altos de HSPA5, YAP, TAZ e marcadores mesenquimais do que os tumores originais com perfil proneural‑like.
O que isso significa para o tratamento futuro do câncer cerebral
Em termos simples, este trabalho sugere que células de glioblastoma exploram uma auxiliar da resposta ao estresse, HSPA5, para proteger interruptores-chave de crescimento (YAP e TAZ) de serem degradados. Essa proteção ajuda os tumores a mudar para e manter uma identidade mais agressiva e resistente ao tratamento. Como já existem inibidores de pequenas moléculas contra HSPA5 e as células tumorais podem depender desta chaperona mais do que as células normais, o eixo HSPA5–YAP/TAZ oferece um alvo novo e atraente. Terapias que enfraqueçam esse escudo protetor poderiam tornar as células do glioblastoma menos adaptáveis, menos invasivas e mais vulneráveis a tratamentos padrão, como quimioterapia e radioterapia.
Citação: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Palavras-chave: glioblastoma, HSPA5, YAP/TAZ, plasticidade tumoral, transição mesenquimal