Clear Sky Science · pt
Interrupção do ciclo celular G0/G1 mediada por p16 leva a SASP e fibrose na distrofia endotelial de Fuchs
Por que essa doença ocular importa
Com o envelhecimento, uma das ameaças menos conhecidas à visão é uma condição chamada distrofia endotelial de Fuchs (FECD), que turva gradualmente a janela frontal normalmente transparente do olho. Este artigo investiga por que certas células na superfície interna da córnea se desgastam e formam cicatrizes ao longo do tempo, e por que mulheres são afetadas com maior frequência. Compreender essas mudanças ocultas pode abrir caminho para medicamentos que retardem ou até evitem a necessidade de transplantes de córnea.
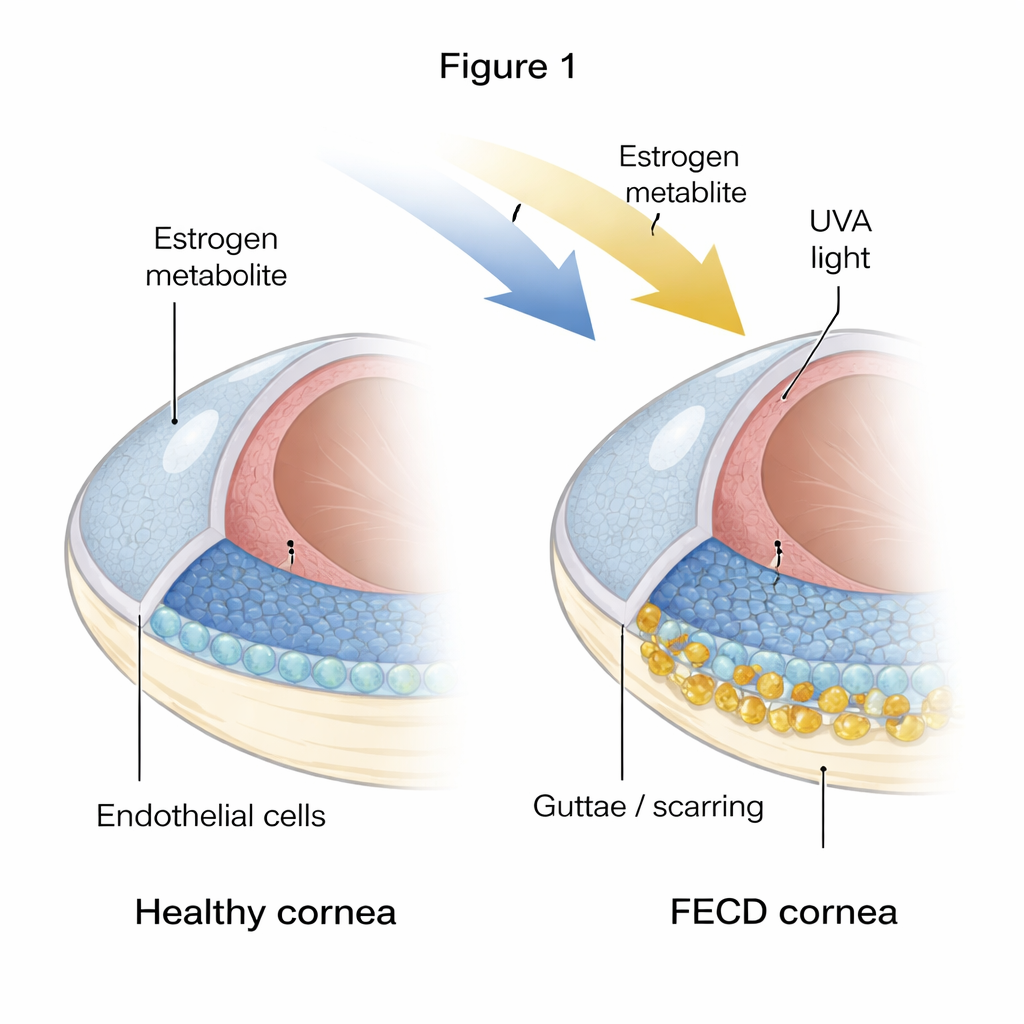
O frágil revestimento interno da córnea
A córnea precisa permanecer precisamente desidratada para ser transparente, tarefa desempenhada por uma única camada de células hexagonais chamadas células endoteliais corneanas. Na FECD, muitas dessas células morrem e a camada torna-se irregular e com lacunas. Ao mesmo tempo, surgem saliências duras e material espessado, conhecidos como guttae e excesso de matriz extracelular, na superfície interna. Os autores compararam córneas de doadores saudáveis com córneas de pacientes com FECD e encontraram fortes indícios de que o tecido doente é tanto “envelhecido” quanto fibrótico: as células exibiram marcadores de senescência (um estado de desligamento permanente) e de fibrose (comportamento mais semelhante a células formadoras de cicatriz e deposição de tecido extra).
Estresse crônico de luz e hormônios empurra as células para um beco sem saída
Para investigar como esse dano começa, os pesquisadores recriaram em laboratório um estresse semelhante ao da FECD. Eles expuseram células endoteliais corneanas saudáveis à luz ultravioleta A (UVA) e à 4-hidroxi-estradiol, um produto oxidado do estrogênio ligado a danos no DNA. Um único episódio curto de estresse fez com que as células entrassem temporariamente em parada em um estágio tardio do ciclo celular e começassem uma transição inicial para um estado mais parecido com fibroblasto, mas ainda mantinham alguma capacidade de recuperação. Em contraste, exposições repetidas e crônicas levaram as células a um estado diferente: elas se acumularam em um estágio inicial do ciclo celular chamado G0/G1 e ativaram um gene chamado p16, que trava o ciclo celular por meio de sua parceira pRB. Essas células tornaram-se grandes, achatadas e inequivocamente senescentes, ao mesmo tempo em que expressaram fortemente marcadores de fibrose e proteínas que compõem os guttae espessados na FECD.
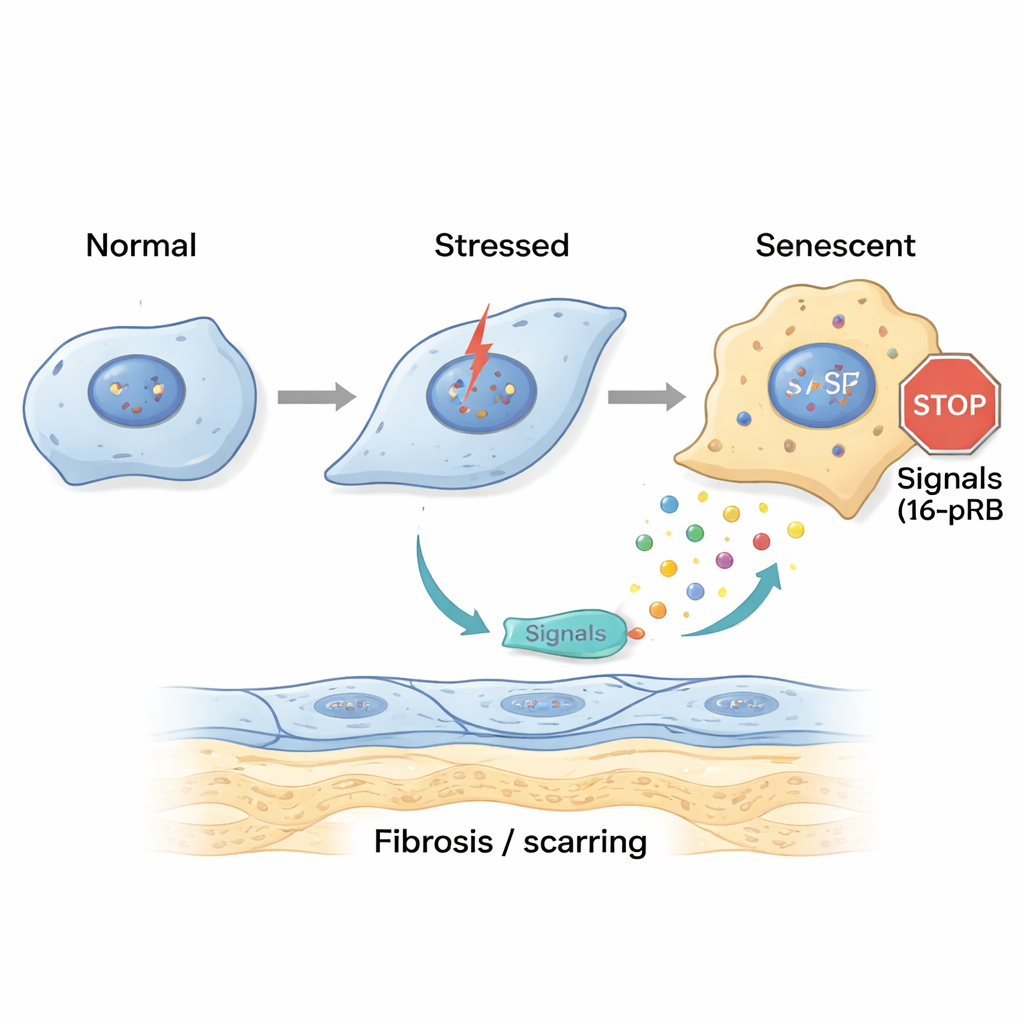
Células senescentes enviam sinais nocivos e disseminam cicatrização
Células senescentes não ficam apenas quietas; elas secretam uma mistura de moléculas sinalizadoras conhecida como fenótipo secretório associado à senescência (SASP). A equipe coletou o fluido de células corneanas estressadas e o aplicou em células frescas e em córneas de doadores saudáveis. O SASP “agudo” causou sinais iniciais de alteração na forma celular, enquanto o SASP “crônico” empurrou muitas células para a senescência e aumentou a expressão de genes ligados à fibrose e à deposição de matriz extra. Testes detalhados mostraram que o SASP crônico era rico em mensageiros inflamatórios como IL-8 e IL-17, conhecidos por promover envelhecimento celular, cicatrização fibrótica e recrutamento de células imunes. Quando os pesquisadores bloquearam a via da IL-17 ou o receptor de IL-8, CXCR2, as células expostas ao SASP crônico exibiram menos marcadores de senescência e menos fibrose, sugerindo que esses sinais são fatores-chave na progressão da doença.
Eliminar células desgastadas para proteger a visão
Como as células senescentes p16-positivas estavam fortemente associadas à cicatrização, os autores testaram se eliminá-las poderia proteger a córnea. Em um modelo de camundongo no qual a luz UVA desencadeia alterações semelhantes às da FECD, trataram os animais com uma combinação de drogas senolíticas, Dasatinibe mais Quercetina, que mata seletivamente células senescentes. Em comparação com os camundongos não tratados, os animais tratados com senolíticos mantiveram um mosaico endotelial mais regular, preservaram mais células no total e exibiram menos marcadores de senescência, fibrose e excesso de matriz. Em outras palavras, remover as células mais danificadas reduziu a carga de secreções nocivas e ajudou a manter uma superfície corneana mais saudável.
O que isso significa para pessoas com FECD
Para pacientes, a FECD frequentemente leva hoje ao transplante de córnea quando a visão se torna demasiado turva. Este estudo sugere um caminho diferente: a doença pode ser impulsionada por um acúmulo lento de células estressadas e não-divisoras que tanto deixam de cumprir sua função quanto envenenam ativamente suas vizinhas com sinais inflamatórios e fibróticos. Alvos terapêuticos contra essas vias, como fármacos que bloqueiem IL-17 ou IL-8, ou o uso de terapias senolíticas para remover seletivamente as células mais comprometidas, poderiam um dia retardar a cicatrização, preservar mais do tecido natural do olho e adiar ou reduzir a necessidade de cirurgia.
Citação: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Palavras-chave: Distrofia de Fuchs, endotélio corneano, senescência celular, fibrose, terapia senolítica