Clear Sky Science · pt
Lactilação de SLC26A3 no microambiente tumoral ácido promove a progressão maligna do carcinoma colorretal
Por que a acidez tumoral importa
O câncer colorretal continua sendo um dos tipos mais letais no mundo, em parte porque os tumores frequentemente retornam, se espalham ou deixam de responder aos medicamentos. Este estudo investiga um vilão pouco apreciado por trás desse comportamento: o ambiente ácido, rico em ácido lático, dentro dos tumores. Ao revelar como esse ambiente hostil desestabiliza uma proteína de membrana protetora chamada SLC26A3, os autores mostram uma nova cadeia de eventos que ajuda as células cancerígenas a se tornarem mais semelhantes a células‑tronco, invasivas e resistentes a medicamentos — oferecendo ideias novas para tratamento.
Um bairro hostil ao redor das células tumorais
Tumores que crescem rapidamente consomem grandes quantidades de açúcar e oxigênio, liberando ácido lático e íons de hidrogênio que tornam o entorno ácido. Usando grandes conjuntos de dados de pacientes e amostras de tecido, os pesquisadores mostram que esse estado ácido, acompanhado por uma proteína marcadora chamada CA9, anda de mãos dadas com tumores colorretais agressivos. Em cânceres mais avançados, os níveis de CA9 são altos, enquanto os de SLC26A3 estão consistentemente baixos. SLC26A3 normalmente se localiza na superfície das células do cólon e ajuda a equilibrar sais e bicarbonato, o que por sua vez contribui para o controle da acidez. Em amostras tumorais, linhas celulares cancerígenas e análises de célula única, a equipe constata que quando a acidez aumenta, os níveis de SLC26A3 caem — especialmente em células cancerígenas malignas e com características de célula‑tronco. 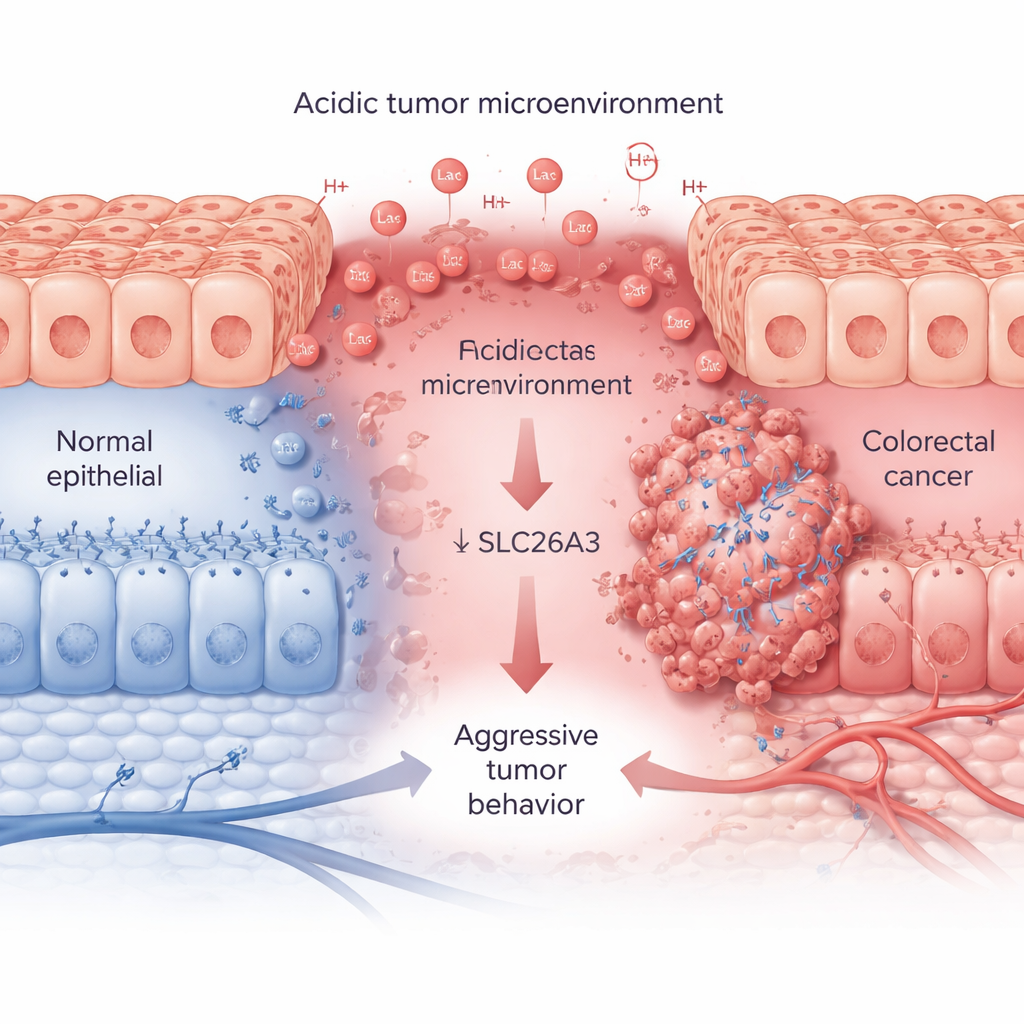
Como o ácido láctico marca um alvo para destruição
Os autores então investigam por que SLC26A3 diminui em tumores ácidos. Eles focam na lactilação, uma marca química recém‑descoberta derivada do ácido lático que pode ser adicionada a proteínas. Quando células de câncer colorretal são expostas ao ácido lático ou cultivadas em condições ácidas, SLC26A3 fica fortemente lactilada. Análises proteicas detalhadas identificam um sítio chave, o aminoácido K536, onde essa marca é adicionada. A lactilação em K536 torna SLC26A3 menos estável: a proteína tem maior probabilidade de ser marcada com ubiquitina, um sinal celular de “descartar isto”, e enviada para a maquinaria de reciclagem da célula. Bloquear a enzima p300, que ajuda a adicionar marcas de lactilação, protege em parte SLC26A3 da degradação. Como resultado, acidez e lactato estabelecem um ciclo de feedback danoso — mais lactato leva a mais lactilação, o que reduz SLC26A3, desregulando ainda mais o equilíbrio de pH e favorecendo um microambiente ainda mais ácido.
Desligando um freio na 'stemness' e na disseminação cancerígena
Com SLC26A3 esgotado, as células cancerígenas se comportam de forma mais agressiva. Em cultura celular, células colorretais com características de célula‑tronco naturalmente expressam menos SLC26A3 do que suas contrapartes não‑tronco. Quando os pesquisadores reduzem intencionalmente os níveis de SLC26A3, as células tumorais formam mais esferas (um marco de pluripotência), renovam‑se com maior eficiência, invadem membranas artificiais e migram mais rapidamente em ensaios de raspagem. Elas também se tornam menos sensíveis a quimioterápicos comuns como oxaliplatina e 5‑fluorouracil. Por outro lado, aumentar SLC26A3 reduz marcadores de stemness e desacelera invasão e migração — mas esse benefício é atenuado quando lactato adicional é adicionado, ressaltando como a acidez pode anular o efeito protetor.
Um elo oculto com o controle gênico
Além de ajudar a regular a acidez, SLC26A3 também atua como um suporte que se liga a duas proteínas ligadoras de RNA, HuR e CUGBP1. Essas proteínas controlam a vida útil de muitos RNAs mensageiros que codificam proteínas relevantes para o câncer. Quando SLC26A3 é abundante, ele sequestra parte de HuR e CUGBP1, limitando o quanto elas podem estabilizar ou desestabilizar certas mensagens relacionadas ao câncer. Quando SLC26A3 é perdido por lactilação e degradação, HuR e CUGBP1 ficam mais livres para se ligar a mRNAs oncogênicos que promovem stemness, transição epitélio‑mesênquima (EMT), invasão e sobrevivência. Experimentos mostram que HuR ajuda a estabilizar mRNAs de marcadores de stemness e proteínas de junção celular, enquanto CUGBP1 pode se opor a HuR em alguns alvos, reduzindo a integridade das junções e incentivando a EMT — ambos favorecendo a disseminação tumoral.
Reequilibrar o ambiente para combater o câncer
Para testar se essas descobertas podem virar estratégias terapêuticas, os pesquisadores usam modelos murinos de câncer colorretal. Neutralizar a acidez tumoral com bicarbonato de sódio, bloquear o transporte de lactato com um inibidor de MCT1 ou superexpressar SLC26A3 retardam o crescimento tumoral. Combinar a restauração de SLC26A3 com quimioterapia reduz ainda mais os tumores. Em dados de pacientes, níveis mais altos de SLC26A3 se correlacionam com melhor sobrevida, menos recidiva, menos metástases e melhores respostas à quimioterapia, sugerindo que essa proteína pode servir tanto como biomarcador quanto como alvo terapêutico. 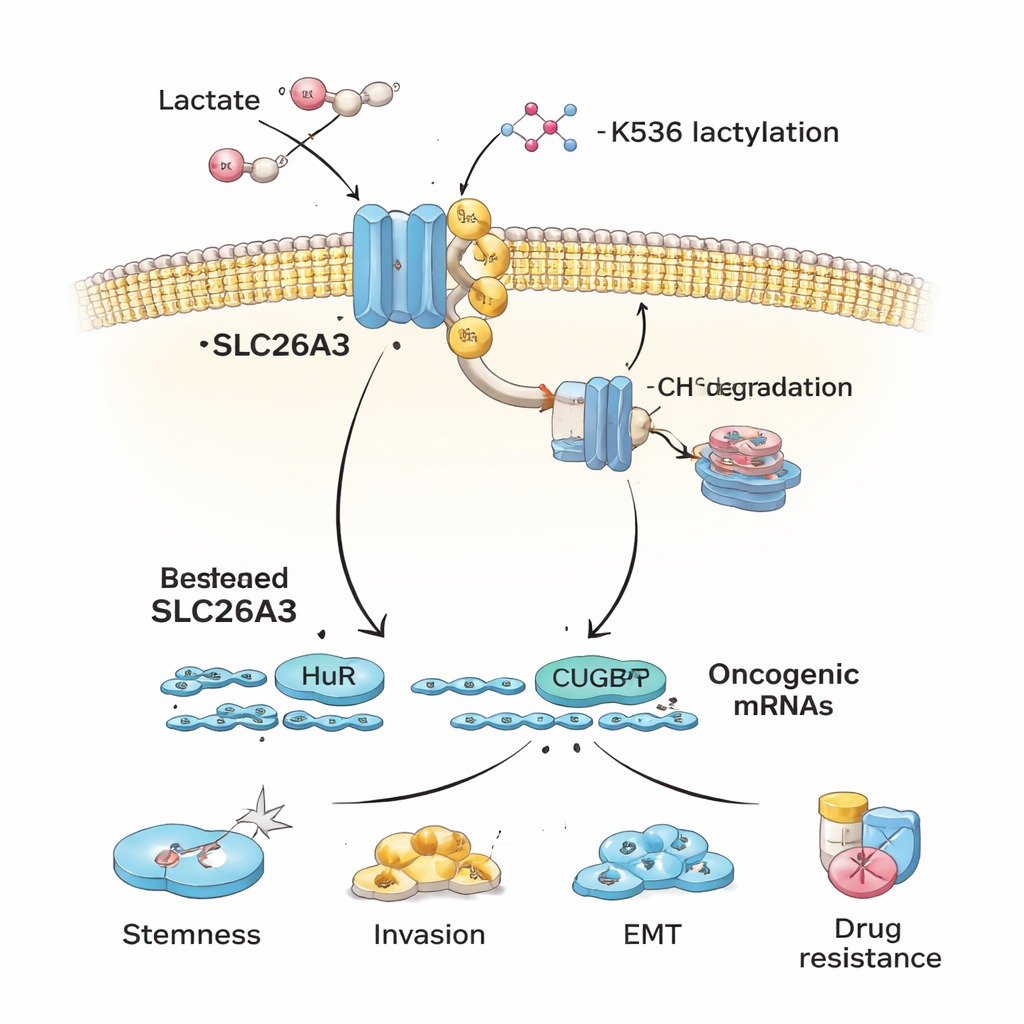
O que isso significa para os pacientes
Em termos práticos, este estudo mostra que tumores colorretais prosperam em um banho ácido, rico em ácido lático, que quimicamente “marca” e destrói um porteiro protetor, SLC26A3. Uma vez que esse porteiro se perde, as células cancerígenas adotam mais facilmente características de célula‑tronco, espalham‑se e resistem ao tratamento, auxiliadas por reguladores poderosos de RNA dentro da célula. Ao tamponar a acidez tumoral, bloquear o manejo de lactato ou restaurar SLC26A3, pode ser possível enfraquecer esse ciclo maligno de realimentação e tornar as terapias padrão mais eficazes. Embora tais abordagens ainda exijam testes clínicos rigorosos, elas abrem um ângulo promissor sobre como o manejo do ambiente químico do tumor pode ajudar a controlar o câncer colorretal.
Citação: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Palavras-chave: câncer colorretal, microambiente tumoral, lactilação, células‑tronco cancerígenas, resistência à quimioterapia