Clear Sky Science · pt
DNA-PKcs orquestra a senescência induzida pela depleção de CTLA-4 em células cancerosas
Transformando o interruptor de crescimento do câncer em um sinal de parada
Medicamentos imunoterápicos contra o câncer costumam mirar uma molécula chamada CTLA-4, presente em células do sistema imune, para ajudar o organismo a atacar tumores. Este estudo revela uma reviravolta surpreendente: a CTLA-4 também é encontrada dentro das próprias células cancerosas e pode agir como um ajudante oculto do crescimento. Quando os cientistas removeram deliberadamente essa CTLA-4 intracelular de células de melanoma, as células tumorais pararam de se multiplicar e entraram em um estado de “aposentadoria” de longo prazo conhecido como senescência celular. Compreender esse papel inesperado abre novas maneiras de desacelerar ou até reduzir tumores ao direcionar a CTLA-4 dentro das células cancerosas, não apenas nas células imunes.
Quando as células escolhem a aposentadoria em vez do crescimento desenfreado
Células normalmente se dividem, se reparan e — quando danificadas além do reparo — ou morrem ou entram em senescência, uma paralisação permanente do crescimento. Células senescentes tipicamente aumentam de tamanho, mudam de forma e produzem marcadores específicos que os pesquisadores podem detectar em laboratório. Os pesquisadores descobriram que, ao reduzir a CTLA-4 dentro de células de melanoma de camundongo e humanas, as células ficaram maiores, sua proliferação caiu drasticamente e sinais clássicos de senescência aumentaram, incluindo enzimas detectáveis por colorações especiais e proteínas como p16 e p21, que bloqueiam o ciclo celular. Essas alterações foram observadas tanto quando a CTLA-4 foi silenciada temporariamente quanto quando foi eliminada permanentemente usando ferramentas de edição gênica.
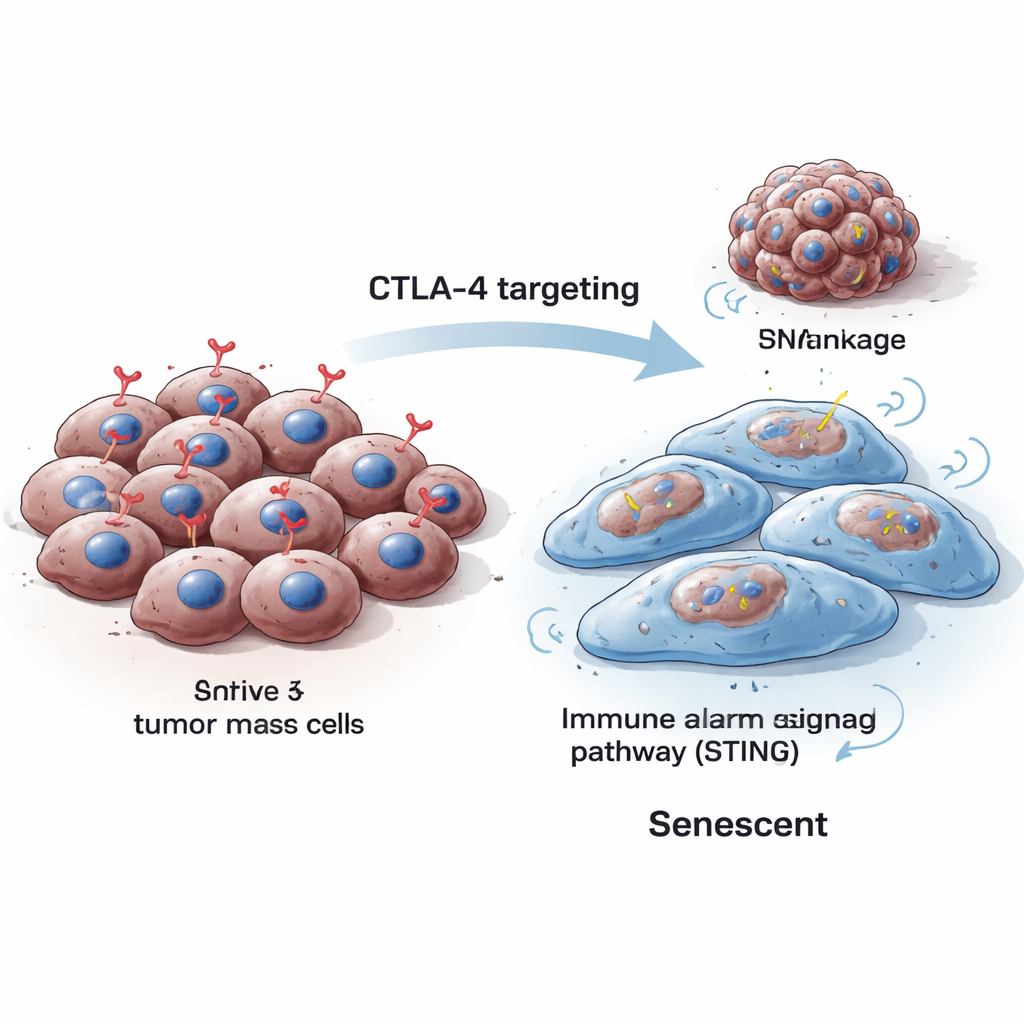
Fissuras no roteiro genético levam a uma paralisação
Para entender por que a perda de CTLA-4 empurra células cancerosas para a senescência, a equipe examinou como essas células lidam com seu DNA durante a divisão. Eles descobriram que a depleção de CTLA-4 reduziu os níveis de Aurora B, uma proteína que ajuda os cromossomos a se separarem corretamente durante a divisão celular. Quando Aurora B caiu, as células desenvolveram instabilidade genômica: surgiram pequenos corpos extras contendo DNA, chamados micronúcleos, e os marcadores de dano ao DNA aumentaram. Esse tipo de estresse no DNA é conhecido por direcionar as células à senescência em vez do crescimento descontrolado. Importante, restaurar Aurora B ajudou a reduzir esses micronúcleos, ligando diretamente a perda de CTLA-4 ao manejo defeituoso dos cromossomos e ao dano ao DNA.
Danos ao DNA disparam uma rede interna de alarme
O DNA quebrado e deslocado em células com CTLA-4 depletada não passou despercebido. Isso ativou DNA-PKcs, um sensor de danos ao DNA, que por sua vez acionou a via STING, um sistema de alarme interno que responde a DNA fora do lugar dentro das células. Uma vez que o STING foi ativado, sinalizou moléculas a jusante, incluindo TBK1 e IRF3, e também reforçou outra via central de controle do crescimento, a via AKT. Em vez de promover crescimento, essa sinalização combinada acabou elevando p21, um forte freio do ciclo celular, reforçando o estado senescente. Quando os cientistas bloquearam DNA-PKcs, a ativação do STING e as características da senescência foram significativamente reduzidas, mostrando que DNA-PKcs ocupa o centro dessa cascata de alarme.
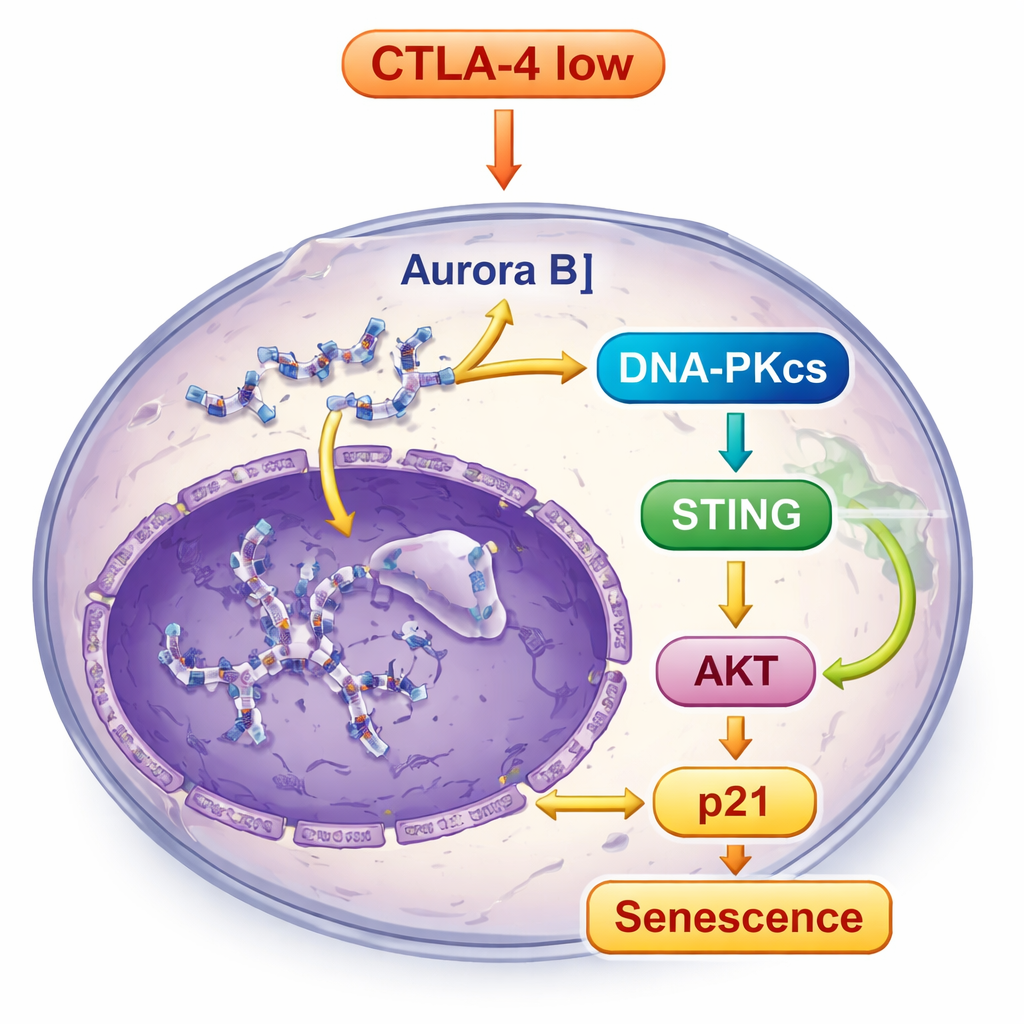
Do cultivo celular a tumores em animais vivos
Placas de cultura contam apenas parte da história, então os pesquisadores testaram se a perda de CTLA-4 afetaria tumores reais em camundongos. Eles implantaram células de melanoma com ou sem CTLA-4 em lados opostos dos mesmos animais. Tumores sem CTLA-4 cresceram mais lentamente, pesaram menos e tiveram menor volume do que seus equivalentes contendo CTLA-4. Esses tumores deficientes em CTLA-4 também mostraram colorações de senescência mais intensas e níveis mais altos de dano ao DNA e ativação da via STING. A análise de dados de pacientes com câncer em grandes bancos públicos reforçou a ligação: em vários tipos de câncer, a expressão de CTLA-4 tende a ser inversamente relacionada a DNA-PKcs e outros componentes de reparo do DNA, ecoando os achados laboratoriais na doença humana.
O que isso significa para tratamentos futuros do câncer
No conjunto, o estudo mostra que a CTLA-4 dentro de células cancerosas as ajuda a manter a estabilidade genética e a continuar se dividindo. Quando a CTLA-4 é removida, os cromossomos ficam instáveis, quebras no DNA se acumulam e uma via de alarme interna — centrada em DNA-PKcs e STING — empurra as células para uma parada permanente do crescimento. Para um leigo, isso significa que desligar a CTLA-4 em células tumorais inclina os cânceres a se afastarem de um comportamento perigoso e de crescimento rápido e em direção a um estado mais seguro de “aposentadoria”. Essas percepções sugerem que terapias futuras contra o câncer poderiam ser projetadas não apenas para liberar o sistema imune bloqueando CTLA-4 em células imunes, mas também para desarmar diretamente tumores ao direcionar a CTLA-4 dentro das células cancerosas e aproveitar a senescência como um freio interno ao crescimento do câncer.
Citação: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Palavras-chave: senescência celular, melanoma, CTLA-4, danos ao DNA, via STING