Clear Sky Science · pt
Transporte citoplasma-núcleo de TET2: um freio intrínseco na progressão do câncer colorretal
Como as células cancerosas carregam seu próprio freio
O câncer colorretal está entre os tipos mais comuns no mundo e frequentemente se torna letal quando as células tumorais aprendem a invadir tecidos vizinhos e se espalhar para outros órgãos. Este estudo revela que muitas dessas células cancerosas, na verdade, carregam um “sistema de freio” interno — uma proteína chamada TET2 — que pode desacelerar seu avanço quando se desloca para o núcleo celular. Entender como esse freio embutido é ligado e desligado pode abrir novas maneiras de conter o crescimento tumoral em vez de apenas tentar eliminar as células cancerosas por completo.
Observando uma proteína-chave se mover dentro das células tumorais
Os pesquisadores concentraram-se no TET2, uma proteína que ajuda a controlar quais genes estão ativados ou desativados removendo certas marcas químicas do DNA. Em amostras de tecido de centenas de pacientes com câncer colorretal, eles mapearam onde o TET2 se localiza dentro das células tumorais. Encontraram quatro padrões principais: predominantemente no núcleo, predominantemente no citoplasma, ou fortemente enviesado para um ou outro. Pacientes cujos tumores apresentavam mais TET2 no núcleo tendiam a viver mais, enquanto aqueles cujos tumores mantinham o TET2 no citoplasma tiveram prognóstico pior. À medida que os cânceres avançavam para estágios clínicos mais avançados, o TET2 nuclear tornou-se mais raro, sugerindo que a perda dessa proteção nuclear faz parte de como os tumores se tornam mais agressivos.
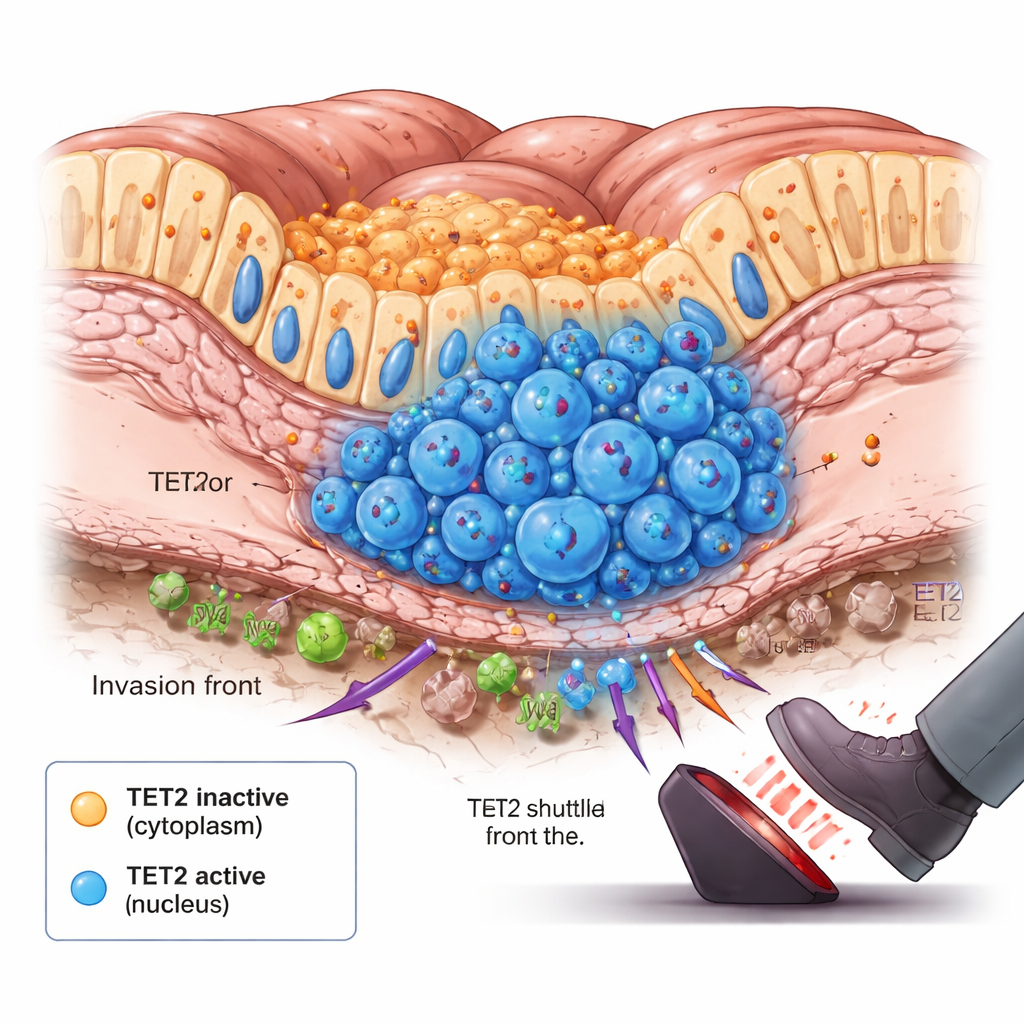
A linha de frente do tumor e o momento da mudança
Ao aprofundar a investigação, a equipe notou algo surpreendente: em tumores que estavam começando a se espalhar, houve um pequeno aumento nas células em que o TET2 havia se deslocado para o núcleo. Essas células se agrupavam na base do revestimento intestinal, a fronteira de invasão onde as células cancerosas começam a penetrar em tecidos mais profundos. Experimentos em animais e modelos de cultura celular de longo prazo que imitam o crescimento tumoral mostraram um padrão semelhante ao longo do tempo. No início, o TET2 permanecia no citoplasma e estava amplamente inativo. À medida que os tumores cresciam e as regiões internas ficavam privadas de oxigênio e nutrientes, sinais intracelulares acionavam o transporte do TET2 para o núcleo em subpopulações específicas. Uma vez lá, o TET2 começou a remover marcas de metilação do DNA e a retardar o crescimento tumoral, atuando como um freio de emergência quando o câncer ultrapassava um limiar perigoso.
Quando sinais de “seguir em frente” também acionam um freio
Os tumores colorretais frequentemente dependem de dois poderosos programas de “seguir em frente”: um processo de mudança de forma chamado transição epitélio‑mesênquima (EMT), que ajuda as células a tornarem-se mais móveis e invasivas, e a via de sinalização WNT, que impulsiona crescimento e sobrevivência. Essas vias costumam ser vistas como puramente prejudiciais no câncer. Contudo, este estudo mostra que, quando EMT e WNT disparam fortemente, elas também ajudam a levar o TET2 ao núcleo. Usando drogas e ferramentas genéticas em culturas celulares, os cientistas demonstraram que ativar EMT ou WNT fez com que mais células deslocassem o TET2 para seus núcleos, enquanto bloquear essas vias teve o efeito oposto. Uma vez no núcleo, o TET2 ativo reduzia então a expressão de genes relacionados à EMT e à WNT, diminuindo a migração celular e retardando a proliferação. Em outras palavras, os mesmos sinais que ajudam os tumores a crescer também despertam uma força contrária interna.
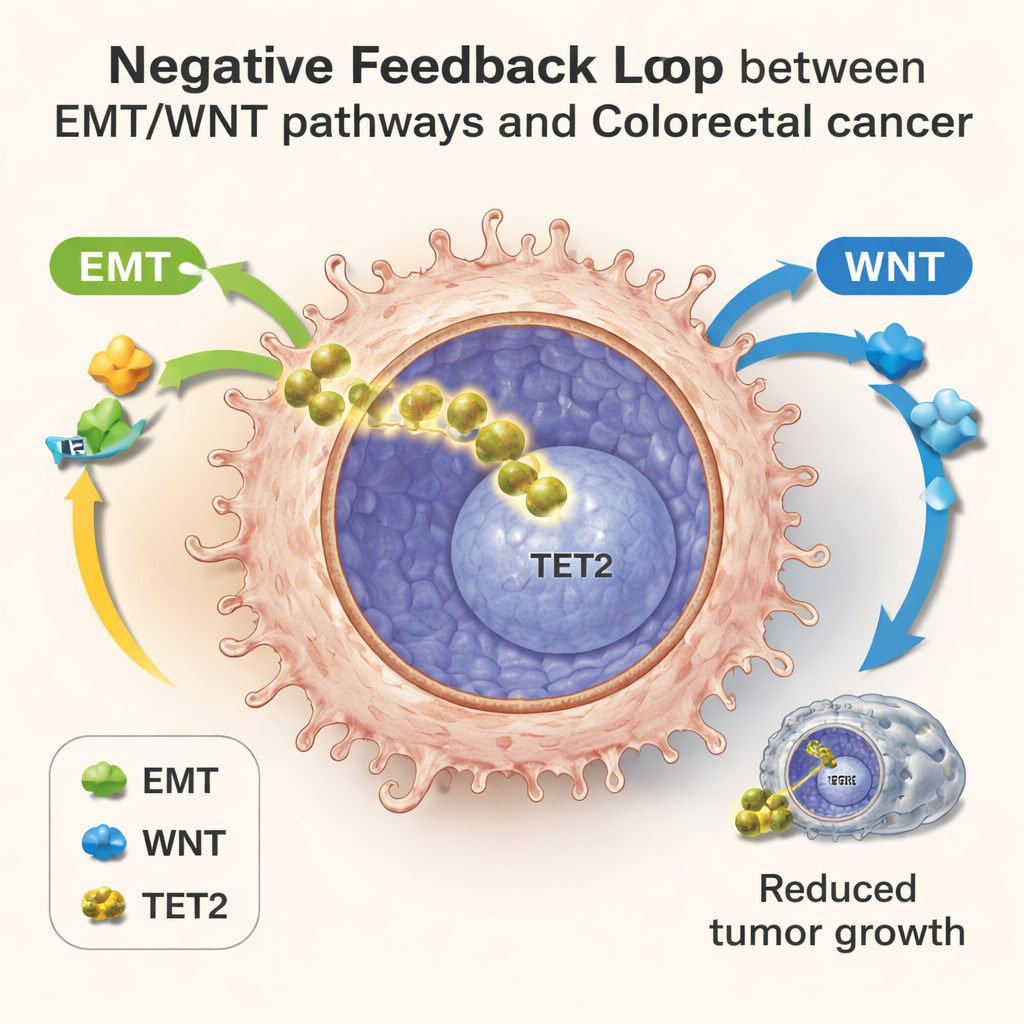
Células únicas revelam um circuito de retroalimentação oculto
Para mapear essa disputa em detalhe, a equipe usou sequenciamento de RNA de célula única, que lê quais genes estão ativos em milhares de células individuais ao mesmo tempo. Em colônias cultivadas em laboratório, em tumores de camundongos e em amostras de pacientes com câncer colorretal, observaram células distribuídas ao longo de uma linha do tempo de progressão. Células iniciais apresentavam uso energético normal e atividade fraca de EMT/WNT; células mais tardias mostravam reorganização metabólica, sinais fortes de EMT/WNT e então aumento dos genes-alvo do TET2. Nessas etapas finais, células com maior atividade de TET2 apresentavam níveis mais baixos de genes relacionados à invasão e associavam‑se a melhores desfechos para os pacientes, mesmo entre tumores que já haviam começado a se espalhar. Esse padrão sustenta a ideia de um laço de retroalimentação negativa: estresse metabólico e ativação de EMT/WNT empurram o TET2 para o núcleo, e o TET2 nuclear, por sua vez, contém esses mesmos programas agressivos.
O que isso significa para tratamentos futuros do câncer
Para não especialistas, a mensagem principal é que a progressão do câncer colorretal não é um simples interruptor “ligado/desligado” entre comportamento bom e ruim. Em vez disso, existe um mecanismo de segurança embutido e retardado: à medida que as células tumorais se tornam mais invasivas, elas também ativam o TET2 em seus núcleos, o que as freia parcialmente. Com o tempo, muitos tumores escapam disso perdendo o TET2 nuclear ou suplantando seus efeitos. Ao encontrar maneiras de manter o TET2 no núcleo ou aumentar sua atividade — possivelmente em combinação com drogas que modulam EMT ou WNT — os médicos poderiam fortalecer esse freio natural e desacelerar a disseminação do câncer. Em vez de apenas atacar as células cancerosas de fora, terapias futuras poderiam agir restaurando e amplificando esse sistema de controle interno.
Citação: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Palavras-chave: câncer colorretal, TET2, epigenética, EMT sinalização WNT, progressão do câncer