Clear Sky Science · pt
Manutenção aberrante do fator de transcrição do desenvolvimento PAX6 promove morte de células neuronais via sinalização JNK3
Por que esta pesquisa importa para a visão
O glaucoma é uma das principais causas de cegueira permanente, em grande parte porque as células nervosas que transportam informações visuais do olho para o cérebro morrem lentamente. Muitos tratamentos reduzem a pressão intraocular, mas pessoas ainda podem perder a visão mesmo quando a pressão está bem controlada. Este estudo faz uma pergunta mais profunda: o que leva essas células nervosas retinianas a decidir pela morte quando estão sob estresse, e podemos desligar essa decisão no nível do controle gênico dentro do núcleo celular?
Uma retina estressada sob ataque
No cerne do glaucoma e de doenças oculares relacionadas está a perda lenta das células ganglionares da retina (CGR), os neurônios de saída do olho. Essas células são vulneráveis a muitos tipos de estresse, inclusive níveis tóxicos do mensageiro cerebral glutamato, que superestimula receptores NMDA e desencadeia uma sobrecarga de cálcio danosa. Os pesquisadores usaram um modelo bem estabelecido em camundongos no qual uma pequena quantidade de NMDA é injetada no olho, lesionando seletivamente as CGR enquanto deixa outras camadas retinianas em grande parte intactas. Eles confirmaram que esse tratamento não alterou a pressão ocular, mas causou sinais típicos de morte celular programada nas CGR, como a liberação de citocromo c das mitocôndrias e o aparecimento de núcleos positivos em TUNEL.
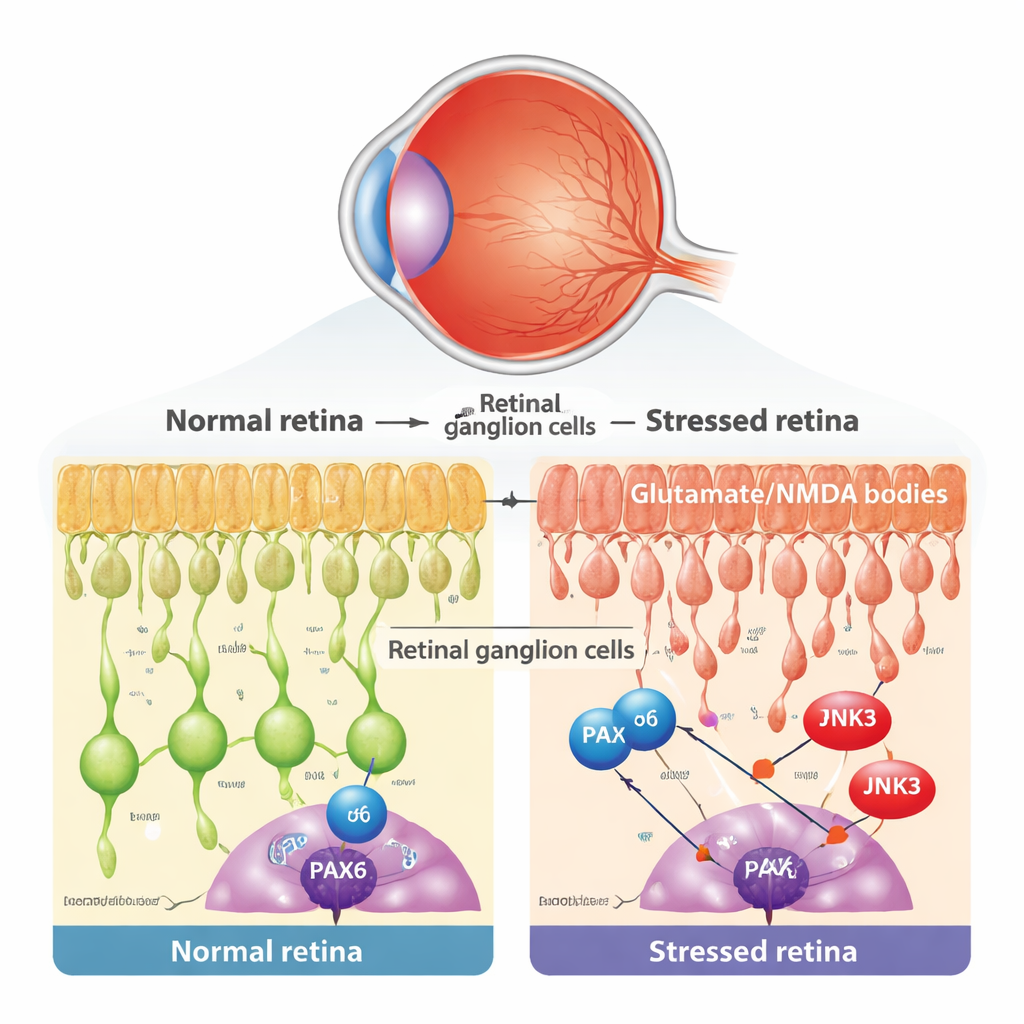
Um gene de desenvolvimento que se recusa a aposentar
Durante o desenvolvimento precoce, um regulador gênico chamado PAX6 atua como um arquiteto mestre do olho, orientando como diferentes células retinianas nascem e se conectam. A sabedoria convencional diz que tais programas de desenvolvimento tendem a se desligar na idade adulta. Ao reanalisar dados de RNA-seq de célula única de retinas de camundongo e humanas, a equipe descobriu que PAX6, na verdade, é fortemente e seletivamente mantido em CGR maduras e em certos interneurônios. Usando coloração microscópica, eles mostraram que, na camada onde as CGR residem, PAX6 está presente em grande parte nas células ganglionares, e não nas células amácrinas vizinhas. Isso levantou uma possibilidade intrigante: em doença adulta, um antigo programa de desenvolvimento pode ser apropriado e transformado em um motor de degeneração.
De guardião a executor: PAX6 troca de papel
Para testar se PAX6 ajuda as CGR a sobreviver ou morrer sob estresse, os cientistas usaram uma abordagem semelhante à terapia gênica. Eles entregaram um vetor viral carregando um pequeno RNA que reduz especificamente PAX6 na retina e então expuseram os olhos ao NMDA. Em comparação com olhos tratados com controle, retinas com PAX6 reduzido mostraram muito menos CGR apoptóticas e muito menos dano mitocondrial, indicando que PAX6 é necessário para a morte celular plena nesse modelo. O sequenciamento de RNA em escala genômica revelou que muitos genes pró-morte, particularmente aqueles envolvidos em dano mitocondrial e ativação de caspases, foram fortemente induzidos pelo NMDA em camundongos normais, mas foram atenuados quando PAX6 foi silenciado. Em outras palavras, PAX6 ajuda a ligar uma rede de genes que empurram as CGR além do limite.
A quinase de estresse que aciona o interruptor PAX6
Como o estresse ativa PAX6 sem aumentar sua quantidade? A equipe concentrou-se na JNK3, uma enzima responsiva ao estresse encontrada principalmente em neurônios. Sob lesão por NMDA, a JNK3 deslocou-se para o núcleo das CGR e associou-se fisicamente ao PAX6. Experimentos bioquímicos "em tubo de ensaio" usando proteínas purificadas mostraram que a JNK3 pode adicionar diretamente grupos fosfato ao PAX6, e essa reação foi bloqueada por um inibidor de JNK. Em camundongos sem o gene Jnk3, o NMDA deixou de produzir o mesmo padrão de fosforilação de PAX6. Mapeamento de cromatina (ChIP-seq) e ensaios direcionados de ligação ao DNA revelaram que, sob estresse, o PAX6 fosforilado, juntamente com a JNK3, fica mais fortemente ligado às regiões de controle de genes pró-apoptóticos chave, como Bax e Gadd45a, aumentando sua atividade. Quando PAX6 foi silenciado ou JNK3 foi geneticamente removida, essa ligação e a correspondente ativação de genes pró-morte foram fortemente reduzidas.
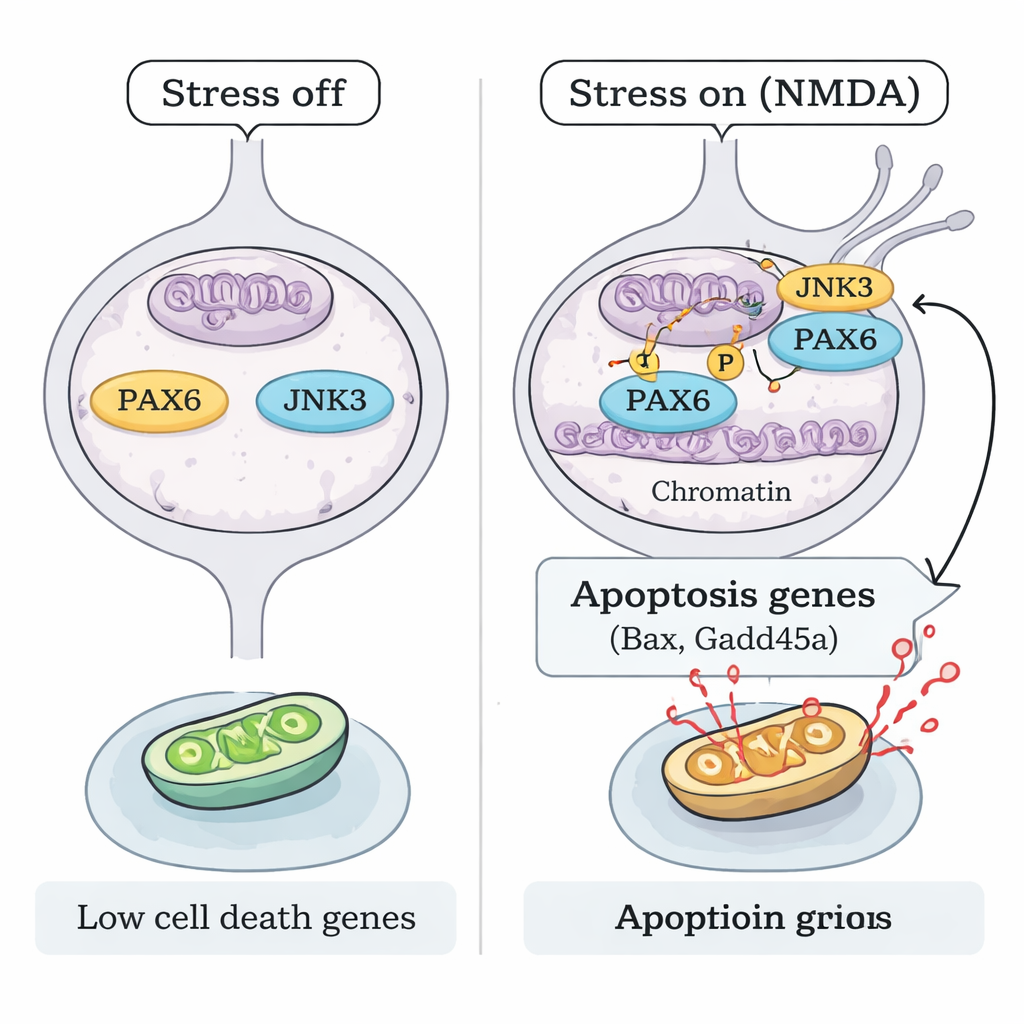
Desligando o programa de morte para proteger a visão
Finalmente, os pesquisadores perguntaram se bloquear esse eixo JNK3–PAX6 é suficiente para proteger células críticas para a visão. Tanto em camundongos com redução de PAX6 quanto em camundongos deficientes em JNK3, as CGR foram significativamente preservadas após a exposição ao NMDA, com menos células morrendo e uma estrutura retiniana mais saudável. Isso aponta para um modelo mecânico claro: sob estresse excitotóxico, a JNK3 fosforila o PAX6 persistentemente expresso, convertendo-o de um construtor de desenvolvimento em um potente ativador de um programa gênico de morte celular nas CGR adultas. Interromper essa ligação — silenciando PAX6 ou desabilitando JNK3 — mantém muitos desses neurônios vivos. Para pacientes, este trabalho sugere que futuras terapias para glaucoma poderiam ir além da redução da pressão ocular e mirar diretamente nos interruptores genéticos que decidem se neurônios retinais vivem ou morrem.
Citação: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Palavras-chave: glaucoma, células ganglionares da retina, PAX6, JNK3, neurodegeneração