Clear Sky Science · pt
Sec8: um novo regulador positivo de RIG-I na defesa contra vírus de RNA
Como Nossas Células Detectam Vírus Astutos
Muitos vírus perigosos, incluindo o influenza e vírus emergentes de animais, carregam seu material genético como RNA. Nossas células dependem de sistemas de alarme internos para perceber rapidamente esses invasores e desencadear uma resposta antiviral. Este artigo explora uma proteína celular pouco conhecida chamada Sec8 e mostra que ela desempenha discretamente um papel central em manter um de nossos sensores virais chave, RIG‑I, estável e ativo tempo suficiente para nos proteger.
Um Alarme Celular Sob Ameaça
RIG‑I é um “alarme de ladrão” molecular que patrulha o interior das células em busca de fragmentos de RNA viral. Quando detecta RNA suspeito, muda de conformação, é ativado e envia sinais que, em última instância, desencadeiam interferons tipo I — moléculas de alerta potentes que ajudam células vizinhas a resistir à infecção e ativam defesas imunes. Como um alarme excessivamente ativo pode causar inflamação prejudicial ou doenças autoimunes, as células controlam rigidamente os níveis de RIG‑I. Várias outras proteínas podem marcar RIG‑I para destruição ao anexar pequenas cadeias de ubiquitina, direcionando‑o ao “triturador” celular chamado proteassoma. Até agora, não estava claro quais fatores celulares adicionais protegiam o RIG‑I de ser destruído prematuramente, especialmente durante infecção ativa por vírus de RNA.
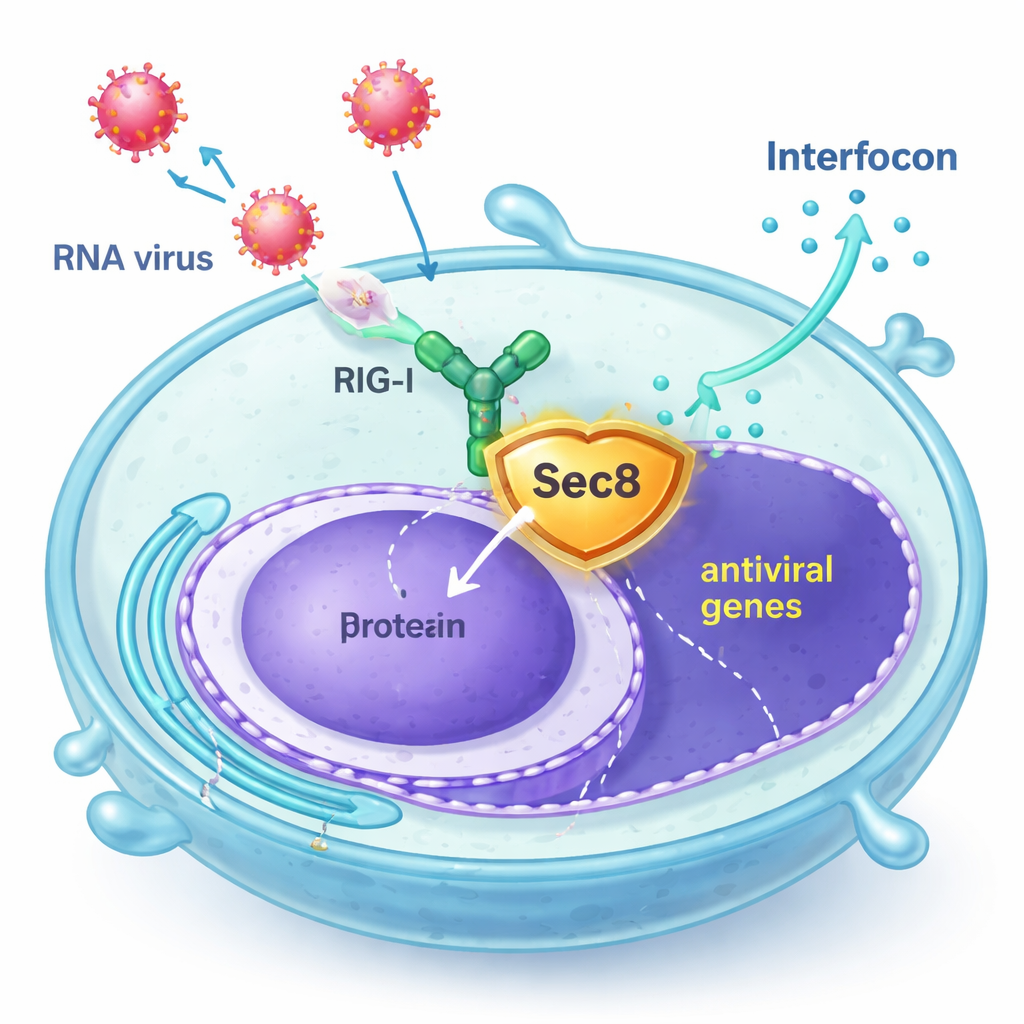
Sec8 Entra em Cena como Segurança
Os autores descobriram que Sec8, mais conhecido por integrar um complexo de oito proteínas que ajuda vesículas secretoras a se fundirem com a superfície celular, na verdade potencializa a sinalização antiviral. Em linhagens celulares humanas e em células imunes primárias de camundongos, o aumento dos níveis de Sec8 levou a uma ativação mais forte de genes relacionados ao interferon após infecção com vírus de RNA como o vírus da estomatite vesicular (VSV) e o vírus Sendai, ou após exposição a RNA viral sintético. Por outro lado, a redução de Sec8 diminuiu a produção de interferon e de genes estimulados por interferon, deixando as células menos capazes de conter a replicação viral. Esses achados sugerem que Sec8 atua não apenas na secreção, mas como um regulador positivo dentro da via do alarme antiviral.
Bloqueando o Triturador Celular
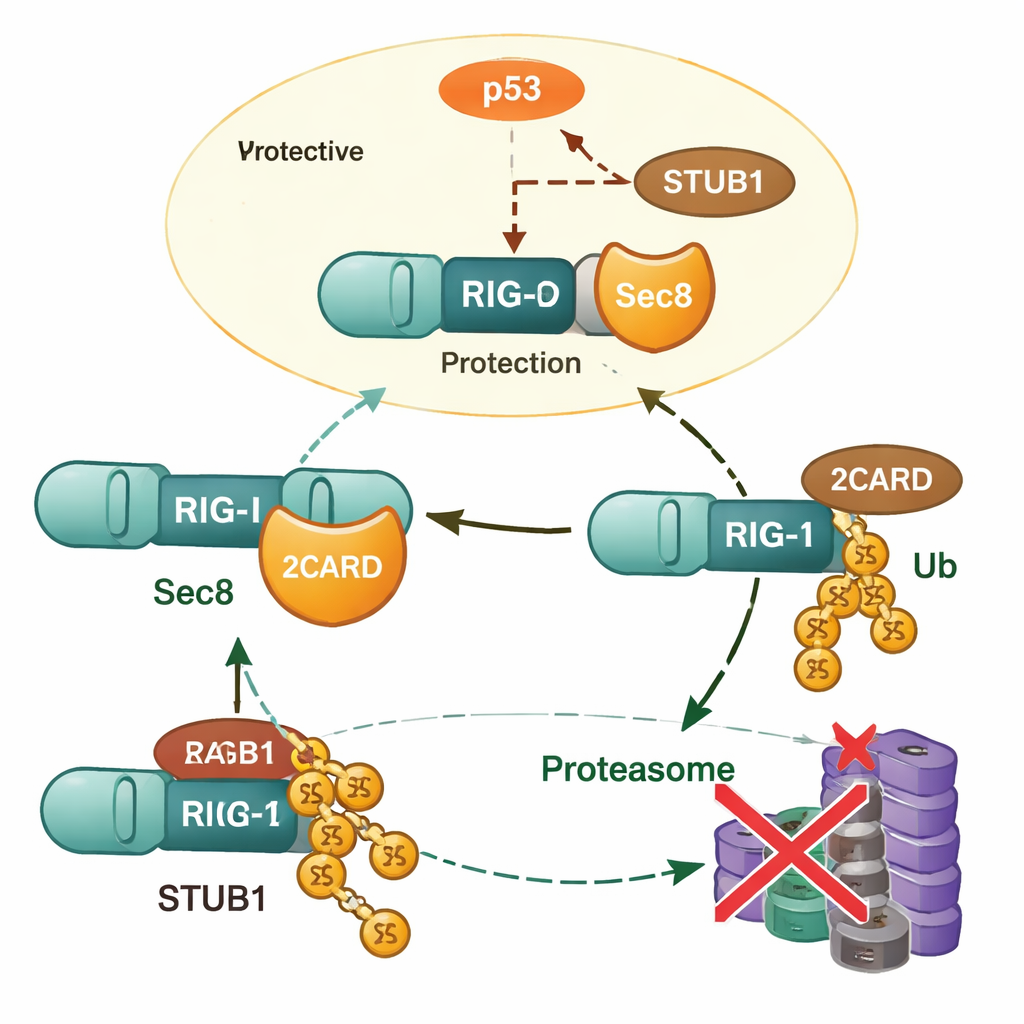
Aprofundando, os pesquisadores descobriram que Sec8 não aumenta a expressão gênica de RIG‑I; em vez disso, preserva a proteína RIG‑I da degradação. Quando Sec8 foi removido, os níveis de RIG‑I caíram mais rápido, e essa perda pôde ser prevenida por drogas que bloqueiam o proteassoma, implicando a máquina de reciclagem de proteínas da célula. A equipe identificou outra proteína, STUB1, como um “marcador” chave que anexa um tipo específico de cadeia de ubiquitina (ligada em K48) ao RIG‑I no aminoácido lisina 190. Essa marca sinaliza RIG‑I para destruição. Sec8 interfere nesse processo de duas maneiras: compete fisicamente com STUB1 pela ligação à mesma região de ativação em RIG‑I, e reduz a quantidade de STUB1 que a célula produz em primeiro lugar.
Sec8, p53 e o Controle do Marcador
Para explicar como Sec8 reduz a produção de STUB1, os autores investigaram a regulação gênica. Eles localizaram um curto trecho de DNA que atua como o núcleo do comutador ligante (promotor) do gene STUB1 e mostraram que a famosa proteína supressora de tumor p53 se liga a essa região e aumenta os níveis de STUB1. Sec8 atenua tanto a quantidade quanto a fosforilação ativadora de p53, de modo que p53 não consegue mais impulsionar a produção de STUB1 com a mesma eficiência. Quando p53 foi bloqueado ou STUB1 silenciado, os efeitos nocivos da perda de Sec8 sobre a produção de interferon e o crescimento viral foram em grande parte revertidos. Isso coloca Sec8 no topo de uma cadeia regulatória que vai de p53 a STUB1 e, finalmente, à estabilidade de RIG‑I.
Do Prato de Cultura a Animais Vivos
O grupo então testou a importância de Sec8 em camundongos geneticamente modificados para não expressarem o gene Sec8 especificamente em certas células imunes. Após infecção com VSV, esses animais produziram menos interferon, tiveram maiores quantidades de vírus em órgãos como baço, fígado e pulmões, e apresentaram pior dano pulmonar, maior perda de peso e menor sobrevida do que os camundongos controle. Esses resultados in vivo confirmaram que Sec8 não é um ator secundário, mas um protetor significativo contra infecção por vírus de RNA em um organismo completo.
Por Que Isso Importa para Terapias Futuras
Em termos simples, este estudo mostra que Sec8 atua como um guarda‑costas para o sensor antiviral RIG‑I. Ao manter a proteína “marcadora” STUB1 sob controle e proteger diretamente RIG‑I de ser enviado ao triturador celular, Sec8 permite que as células montem uma resposta de interferon oportuna e controlem melhor os vírus de RNA. Compreender esse recém‑descrito eixo p53–STUB1–RIG‑I abre a porta para futuras estratégias antivirais que estabilizem RIG‑I ou imitem as ações protetoras de Sec8, potencialmente reforçando nossas defesas contra uma ampla gama de infecções virais baseadas em RNA.
Citação: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Palavras-chave: imunidade inata, vírus de RNA, RIG-I, ubiquitinação, sinalização por interferon